
题目列表(包括答案和解析)
26、A-H是中学化学常见的物质,已知常温下E为无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。
请回答下列问题:
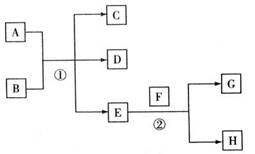 (1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出稀溶液中①的离子方程式:
(1)若A、C、D均含有氯元素,且A的化合价介于C与D之间,写出稀溶液中①的离子方程式:
。
(2)若C、D均为气体且都能使澄清石
灰水变浑浊,则A与B分别为
。(写化学式)
(3)若A与B均为固体化合物,该反应是实验室制备D气体的反应,且C是一种常见的中性干燥剂,则反应①的化学方程式为 ;写出A、B的电子式A ,B 。
(4)若A为红褐色难溶于水的固体,B为第(1)题中的某一产物,两者在浓碱溶液中发生反应生成了高效环保的净水剂Na2FeO4,请写出此反应的离子方程式:
。
13、电解100ml含CH+=0.30mol·L-1的下列溶液,当电路通过0.04mol电子时,理论上析出金属质量最大的是 ( )
A、0.10 mol·L-1 Ag+ B、0.20 mol·L-1 Zn2+
C、0.20 mol·L-1 Cu2+ D、0.20 mol·L-1 Pb2+
12、下列各组中的两种物质相互反应时,无论哪种反应物过量,都可以用同一离子方程式表示的是 ( )
A、碳酸钠和盐酸 B、氨水和硝酸银
C、CO2通入澄清石灰水 D、苯酚溶液和CO2
11、下列物质不能通过化合反应得到的是 ( )
①Fe(OH)3 ②Al2S3 ③FeCl2 ④FeCl3 ⑤SO3
⑥CO ⑦H2SiO3 ⑧NaHCO3 ⑨CaCO3
A、③⑥⑦⑨ B、⑦⑨ C、仅⑦ D、③⑤⑥⑦⑧⑨
10、下列物质甲、乙以2:1物质的量比混合,同时通入过量丙溶液中,一定产生沉淀的组合是 ( )
|
序号 |
甲 |
乙 |
丙 |
|
① |
CO2 |
SO2 |
BaCl2 |
|
② |
NH3 |
CO3 |
CaCl2 |
|
③ |
SO2 |
Cl2 |
Na2S2O3 |
|
④ |
HCl |
CO2 |
Ba(OH)2 |
|
⑤ |
H2S |
CO2 |
饱和Na2CO3 |
A、①②③④ B、②③④⑤ C、①②③⑤ D、①③④⑤
9、现有一包铝热剂是铝粉和氧化铁粉末的混合物,在高温下使之充分反应,将反应后的固体分为两等份,进行如下实验(计算pH时假定溶液体积没有变化):
①向其中一份固体中加入100mL 2.0mol·L-1的NaOH溶液,加热使其充分反应后过滤,测得滤液的pH=14;
②向另一份固体中加入100mL 4.0 mol·L-1的HCl溶液,使固体全部溶解,测得反应后所得溶液中只有H+、Fe2+和Al3+三种阳离子且pH=1。
则②产生气体的体积(标准状况)为 ( )
A、2.352L B、2.448L C、2.688L D、2.856L
8、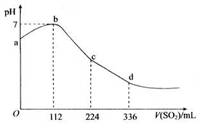 标准状况下,某同学向100mL
H2S饱和溶液中通入
标准状况下,某同学向100mL
H2S饱和溶液中通入
SO2,所得溶液pH变化如图所示。下列分析中,正
确的是 ( )
A、b点对应的溶液导电性最强
B、亚硫酸是比氢硫酸更弱的酸
C、原H2S溶液的物质的量浓度为0.05mol·L-1
D、ab段反应是:SO2+2H2S====3S↓+2H2O
7、下列实验操作完全正确的是 ( )
A、配制100mL 0.1mol·L-1的NaCl溶液时,先量取10mL 1mol·L-1的NaCl溶液倒入容量瓶中,再加水稀释至刻度线
B、配制氯化铁溶液时,将一定量氯化铁溶解在少量浓盐酸中,再用水稀释
C、制备乙酸乙酯时,将乙醇和乙酸依次加入到浓硫酸中
D、乙醇与金属钠的反应,在盛有少量乙醇溶液的试管中,加入一小块新切的、用滤纸擦干表面煤油的金属钠
6、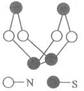 现代无机化学对硫一氮化合物的研究是最为活跃的领域之一。其中如图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是 ( )
现代无机化学对硫一氮化合物的研究是最为活跃的领域之一。其中如图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是 ( )
A、该物质的分子式为SN
B、该物质的分子中既有极性键又有非极性键
C、该物质具有很高的熔、沸点
D、该物质与化合物S2N2互为同素异形体
32.(8分)氧化还原滴定实验同中和滴定关系(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液 或反之).现有0.001mol·L-1酸性KMnO4和未知浓度的无色NaHSO3溶液.反应离子方程式是:2MnO-4+5HSO-3+H+=2Mn2++5SO2-4+3H 2O,填空回答问题.
(1)该滴定实验所需仪器有下列中的 (填序号)
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(10mL) D.锥形瓶 E.铁架台 F.滴定 管夹 G.烧杯 H.白纸 I.胶头滴管 J.漏斗.
(2)不用 (酸、碱)式滴定管盛放高锰酸钾溶液.试分析原因:
(3)选何种指示剂,说明理由
(4)滴定前平视KMnO4液面,刻度为amL,滴定后俯视液面刻度为bmL,则(b-a)mL比实际消 耗KMnO4溶液体积 (多、少).根据(b-a)mL计算,得到的待测液浓度,比实际浓度 (大、小)
哈尔滨市第六中学2008-2009学年度上学期期末考试
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com