
题目列表(包括答案和解析)
21、(4分)在实验室中电解500ml浓度为0.03mol/L的NaCl溶液,通电一段时间后溶液的PH值从7增至12时(设电解时溶液体积变化忽略不计),
标准状况下阴极产生的气体 ml。
此时溶液中NaCl的物质的量的浓度为 mol/L
10.4g,在该含氧酸盐中金属的化合价为 ,在该实验中,若不考虑能
量的损失,电池中消耗丁烷的质量最少是 g( 结果精确至0.01g)。
20、(14分)燃料电池是使气体燃料氧化直接产生电流的装置,这是本世纪最具挑战性的课题之一,最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入丁烷,电池的电解质是参杂了Y2O3(三氧化二钇)的ZrO2(二氧化锆)晶体,它在高温下能传导O2-。试回答下列问题:
(1)该燃料电池的电极反应式:
正极
负极
则固体电解质中的O2-向 极移动(填正或负)。
(2)该燃料电池放电时的总反应方程式为:
。
(3)某金属的相对原子质量为52.00,用上述电池电解该金属的一种含氧酸盐的酸性水溶液时,阳极每放出3360ml(标准状况)氧气,阴极析出金属
19、(6分)草酸晶体的化学式可表示为H2C2O4·XH2O,为了测定X值进行下列实验:
(1)称取Wg草酸晶体,配成100.0ml溶液。
(2)取25.0ml所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为amol/L的KMnO4溶液滴定。KMnO4+H2C2O4·XH2O+H2SO4→K2SO4+MnSO4+CO2+H2O请回答:
实验(1)中,为配制准确的草酸溶液,必须使用的仪器是 ;
实验(2)中滴定时,KMnO4溶液应盛在 中;若滴定用的KMnO4
溶液因放置而变质,浓度偏低,则根椐实验求出的X值 (填
偏高、偏低、无影响);滴定终点时,锥形瓶内溶液颜色变化
是 。
18.(10分)在10℃和2×105Pa的条件下,反应aA(g)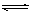 dD(g)+eE(g)建立平衡后再逐步增大体系的压强(温度不变)。下表列出了不同压强下反应建立平衡时物质D的浓度:
dD(g)+eE(g)建立平衡后再逐步增大体系的压强(温度不变)。下表列出了不同压强下反应建立平衡时物质D的浓度:
根据表中数据回答:
(1)压强从2×105Pa增加到5×105Pa时,平衡向 反应方向移动(填“正”、“逆”)。
判断依据 。
(2)压强从5×105Pa增加到1×106Pa时,平衡向 反应方向移动(填“正”、“逆”),判断依据是
。
可能的原因是 。
17、(4分)向50ml0.018mol/L的AgNO3溶液中加入50ml0.020mol/L的盐酸,生成沉淀。如果此温度下的KSP=1×10-10(mol/L)2试求沉淀后溶液中C(Ag+)
= ,沉淀后溶液的PH= 。(溶液混合过程中体积变化忽略不计)
|
压强(Pa) |
2×105 |
5×105 |
1×106 |
|
D的浓度(mol/L) |
0.085 |
0.20 |
0.44 |
16、(5分)电解1L 1mol/L的CuSO4溶液(惰性电极),当电路中通过0.5mol
电子时,溶液中Cu2+的浓度为 ,H+的浓度为 。然后
将电源反接,又通过了1mol电子后,溶液中Cu2+的浓度为 ,H+
的浓度为 ,SO42-的浓度为 。
15.如图所示,下列叙述正确的是 ( )
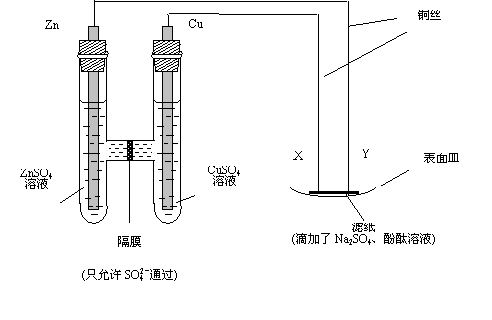

A.Y为阴极,发生还原反应
B.X为正极,发生氧化反应
C.Y与滤纸接触处有氧气生成
D.X与滤纸接触处变红
班级 姓名 学号 分数
第Ⅱ卷(共55分)
14.在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为Amol/L与Bmol/L,则A和B关系为
A. A>B B. A=10-4 B
C. B=10-4 A D. A=B
13.在容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g);△H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
2C(g);△H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
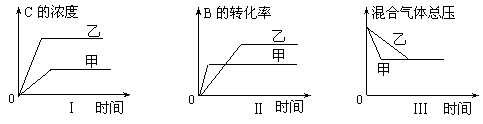
下列判断一定错误的是( )
A.图I研究的是压强对反应的影响,且乙的压强较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com