
题目列表(包括答案和解析)
13.某酸性溶液中只有Na+、CH3COO-、H+、OH-四种离子。则下列描述正确的是( )
A.该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量的NaOH,溶液中离子浓度为c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
D.加入适量氨水,c(CH3COO-)一定大于c(Na+)、c(NH4+)之和
12.下列说法正确的是 ( )
A.某二元弱酸的酸式盐NaHA溶液中:
c(H+)十c(Na+)=c(OH-)+c(HA-)+c(A2-)
B.一定量的(NH4)2SO4与NH3·H2O混合所得的碱性溶液中:c(NH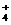 )>2c(SO
)>2c(SO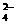 )
)
C.在物质的量浓度均为0.01mol/L的CH3COOH和CH3COONa的混合溶液中:
c(CH3COOH)+c(CH3COO一)=0.01mol/L
D.相同温度下物质的量浓度相等的NH4HSO4溶液、NH4HCO3溶液、NH4Cl溶液中
c(NH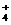 ):c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl)
):c(NH4HSO4)>c(NH4HCO3)>c(NH4Cl)
11.在l体积pH=12的Ba(OH)2溶液中,逐滴加入某H 2SO4溶液,当溶液中的Ba2+恰好完全沉淀时,H2SO4溶液恰为1体积。若反应后溶液的体积为两溶液体积之和,则反应后溶液pH为 ( )
A.1 B.7 C.8 D.0
10.关于铅蓄电池的说法正确的是 ( )
A.在放电时,正极发生的反应是 Pb(s) +SO42-(aq)= PbSO4(s) +2e-
|
C.在充电时,电池中硫酸的浓度不断变小
D.在充电时,阳极发生的反应是 PbSO4(s)+2e-= Pb(s)+ SO42-(aq)
9.某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不
考虑水解),且SO4-的物质的量浓度为6mol·L-1,则此溶液最多溶解铁粉的质量为( )
A.5.6g B.11.2g C.22.4g D.33.6g
8.下列叙述正确的是 ( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO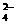 )>c(NH
)>c(NH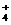 )
)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中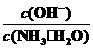 增大
增大
7.将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液。然后用
l mol·L-1的盐酸滴定至沉淀量最大时,消耗盐酸40 mL。原合金中钠的质量为( )
A.0.92 g B.0.69 g C.0.46 g D.0.23 g
6.下列有关金属腐蚀与防护的说法正确的是 ( )
A.纯银器表面在空气中因化学腐蚀渐渐变暗
B.当镀锡铁制品的镀层破损时,镶层仍能对铁制品起保护作用
C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀
5.实验室现有3种酸碱指示剂,其pH的变色范围如下:
甲基橙:3.1-4.4 石蕊:50-8.0 酚酞:8.2-10.0
用0.1000mol·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙
述正确的是 ( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
4.下列叙述正确的是 ( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后PH=4
C.氯化钙溶液中通二氧化碳气体可产生白色沉淀
D.水中加入某固体单质如钠,经化学反应能够促进水的电离
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com