
题目列表(包括答案和解析)
2.A CH3COONa溶液中存在CH3COO-
+ H2O CH3COOH + OH-的水解平衡,加入的
CH3COOH + OH-的水解平衡,加入的
NH4NO3和FeCl2显酸性,故促进其平衡正向移动,则CH3COO-浓度减小;加入的Na2SO3
水解显碱性,对其平衡有抑制,故CH3COO- 浓度增大。
1.A 浓H2SO4使Al钝化,Mg、Al和HNO3反应不产生H2,Mg、Al都可与HCl发生反
应,故答案为A。
21.(10分)小苏打、胃舒、平达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.5gNaHCO3,2片小苏打片和胃酸完全中和,被中和的H+是___________mol。
(2)胃舒平每片含0.245gAl(OH)3。中和胃酸时,6片小苏打片相当于胃舒平_____片。
(3)达喜的化学成分是铝和镁的碱式盐。
①取该碱式盐3.01g,加入2.0mol·L-1盐酸使其溶解,当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时正好反应完全,计算该碱式盐样品中氢氧根与碳酸根的物质的量之比。
②在上述碱式盐溶于盐酸后的溶液中加入过量的氢氧化钠,过滤,沉淀物进行干燥后重1.74g,若该碱式盐中氢元素的质量分数为0.040,试推测该碱式盐的化学式。
|
20.(10分)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________________。
(2)若将(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应___________________________
负极反应___________________________
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10 mol·L-1。,请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤________。
|
|
氢氧化物开始 沉淀时的pH |
氢氧化物沉淀 完全时的pH |
|
Fe3+ Fe2+ Cu2+ |
1.9 7.0 4.7 |
3.2 9.0 6.7 |
|
提供的药品:Cl2
浓H2SO4 NaOH溶液 CuO Cu |
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式:___________________________________;
劣质不锈钢腐蚀的实验现象:_______________________________。
19.(8分)海水的综合利用可以制备金属镁,其流程如下图所示:

(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出相应反应的化学方程式。________________________________________________________
用电解法制取金属镁时,需要元水氯化镁。在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_________________________。
(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?写出实验步骤。
_______________________________________________________________________
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:____________________________________________________。
过滤时:_____________________________________________________。
蒸发时:____________________________________________________。
18.(8分)下列物质(均为中学化学常见物质)转化关系如图所示,已知D为红棕色粉末
(反应条件及部分反应物、产物未全部标出)。
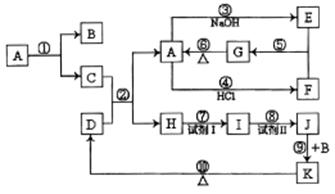
根据图示转化关系填写下列空白:
(1)写出下列物质的化学式:
A:______________;B:______________;E:_______________;K:______________。
(2)C与D的混合物通常叫做_______________(填名称)。
(3)写出下列反应的化学方程式(注明反应条件,若是离子反应的与离子方程式):
②:____________________________________________________________
⑤:____________________________________________________________
⑨:____________________________________________________________
17.(10分)某学习小组用题27图装置测定铝镁合金中铝的质量分数和铝的相对原子质量.
(1)A中试剂为 .
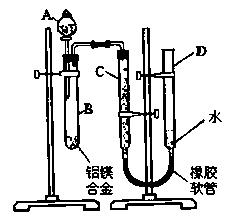
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是 .
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:①记录C的液面位置;②将B中剩余固体过滤,洗涤,干燥,称重;③待B中不再有气体产生并恢复至室温后,记录C的液面位置;④由A向B中滴加足量试剂;⑤检查气密性,上述操作的顺序是 ;(填序号)记录C的液面位置时,除视线平视外,还应 .
(4)B中发生反应的化学方程式为 .
(5)若实验用铝镁合金的质量为a g,测得氢气体积为b ml(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为 .
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将 .
(填“偏大”、“偏小”、“不受影响”)
16.(9分)某课外活动小组拟用下列装置做炼铁原理的实验,同时检测氧化铁的纯度(假设矿石中不含其它与CO反应的成分),并除去尾气。CO使用乙二酸分解:
H2C2O4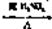 CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
CO2↑+CO↑+H2O来制取,与Fe2O3反应的CO需纯净、干燥。
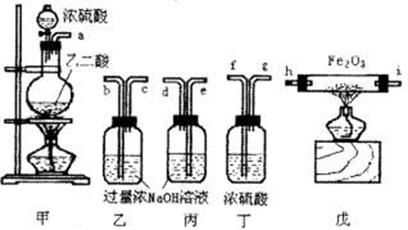
(1)若所制气体从左向右流向时,上述仪器组装连接的顺序是(用a,b…表示)
a接b,c接 , 接 , 接 ;
(2)装置丙的作用是
(3)怎样除去尾气中的CO气体
(4)实验前氧化铁矿粉末为x g,经充分反应实验后测得乙、丙质量分别增加y g和z g,则该矿石中氧化铁的质量分数为 。
15.MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如右图所示.下列叙述中正确的是 ( )
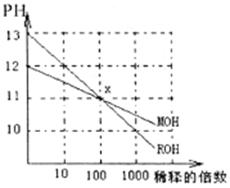
A.MOH和.ROH都是强碱
B.稀释前,c(ROH)=10c(MOH)
C.常温下pH之和为14的醋酸和ROH溶液等体积混合,所得溶液呈碱性
D.在x点,c(M+)=c(R+)
第Ⅱ卷(55分)
14.常温时,V1mL c1 mol/L的醋酸滴加到V2 mL c2 mol/L的烧碱溶液中,下列结论正确的是
( )
A.若V1=V2,且混合溶液pH<7,则有c1<c2
B.若V1=V2,c1=c2,则混合溶液中c(Na+)=c(CH3COO-)
C.若混合溶液的pH=7,则有c1V1>c2V2
D.若混合溶液的pH=7,则混合溶液中c(Na+)>c(CH3COO-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com