
题目列表(包括答案和解析)
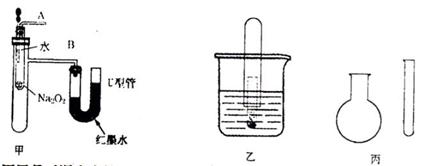 20.(16分)“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验。因其具有许多优点,已被广泛应用于化学实验中。下列三个实验均为“套管实验”,请观察、分析,回答下列问题:
20.(16分)“套管实验”是将一支较小的玻璃仪器装入另一支玻璃仪器中,经组装来完成原来需要较多仪器进行的实验。因其具有许多优点,已被广泛应用于化学实验中。下列三个实验均为“套管实验”,请观察、分析,回答下列问题:
18.(8分)不同元素的原子在分子内吸引电子的能力大小可用一定数值x来表示,若x越大 ,其原子吸引电子能力越强,在的形成的化学键中成为带负电荷的一方,下面是某些短周期元素的x值;
|
元素素素素 |
Li |
Be |
B |
C |
O |
F |
|
x值 |
0.98 |
1.57 |
2.04 |
2.55 |
3.44 |
3.98 |
|
元素 |
Na |
Al |
Si |
P |
S |
Cl |
|
x值 |
0.93 |
1.61 |
1.90 |
2.19 |
2.58 |
3.16 |
(1)推测x值与原子半径的关系是 ;
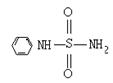
(2)某有机化合物结构式为H2N ,其中S-N中,你认为共用电子对偏向 。
(3)经验规律告诉我们:当成键的两原子相应元素的x差值(Δx)即Δx>1.7时,一般为离子键,Δx < 1.7,一般为共价键,试推断:BeCl3中化学键类型是 。
(4)预测元素周期表中x值最小的元素的位置 (放射性元素除外)。
|
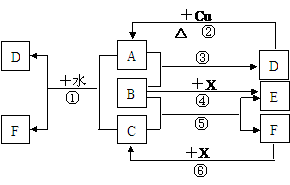 19.(12分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。试回答下列问题:
19.(12分)已知A-F是中学化学中常见物质,其中A、C、E、F为气体,B、D为液体,D的消费量常作为一个国家工业发达水平的一种标志,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子。反应中部分生成物已略去。试回答下列问题:
(1)根据图中信息,B、C、D、X氧化性从强到弱的顺序是(用化学式表示)
。
(2)B物质在生活中的一种用途 。
(3)写出反应③的化学方程式: 。
(4)写出反应⑥的离子方程式: 。
17.(6分)某化学反应的反应物和产物如下:
KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O
(1)该反应的氧化产物是 。
(2)如果该反应方程式中I2和KIO3的化学计量数都是5,请配平该反应化学方程式并标 明电子转移的方向和数目
16.氯化溴是由两种卤素互相结合而成的卤素互化物。其化学性质与Cl2相似,能与金属和非金属反应生成卤化物,能与水反应:BrCl+H2O HCl+HBrO,下列有关BrCl的性质的叙述中不正确的是 ( )
A.是较强的氧化剂
B.BrCl含极性共价键
C.能使润湿的淀粉碘化钾试纸变蓝
D.BrCl与水反应中,BrCl既是氧化剂,又是还原剂
第Ⅱ卷(非选择题 52分)
15.同一主族X、Y、Z三元素,已知,其同浓度最高价含氧酸的钠盐溶液的pH值由大到小的顺序为Na3XO4>Na3YO4>Na3ZO3,下列关系正确的是 ( )
A.元素的非金属性强弱X>Y>Z B.相对原子质量X<Y<Z
C.阴离子还原性X3->Y3->Z3- D.气态氢化物的稳定性XH3>YH3>ZH3
12.若以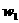 和
和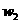 分别表示浓度为amol·L-1和bmol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小) ( )
分别表示浓度为amol·L-1和bmol·L-1氨水的质量分数,且知2a=b,则下列推断正确的是(氨水的密度比纯水的小) ( )
A.2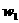 =
=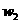 B.2
B.2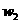 =
=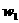 C.
C.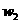 >2
>2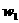 D.
D.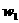 <
<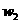 <2
<2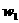
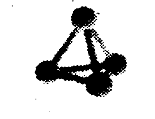 13.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量,根据以上信息和数据,下列说法正确的是 ( )
13.最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1molN-N键吸收167kJ热量,生成1molN≡N键放出942kJ热量,根据以上信息和数据,下列说法正确的是 ( )
A.N4属于一种新型的化合物
B.N4分子是非极性分子
C.N4沸点比P4(白磷)高
D.0.1molN4气体转变为N2将放出882kJ热量
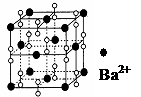 14.钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如下图所示,有关说法正确的是
14.钡在氧气中燃烧时得到一种钡的氧化物晶体,其结构如下图所示,有关说法正确的是
( )
A.该晶体为分子晶体
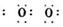 B.晶体的化学式为Ba2O2
B.晶体的化学式为Ba2O2
C.该氧化物的电子式为Ba2+[ ]2-
D.与每个Ba2+距离相等且最近的Ba2+共有6个
11.在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c,则下列说法正确的是 ( )
A.残余固体是铜和铁
B.最后得到的溶液中一定含有Cu2+
C.将残余固体加入到稀H2SO4中,有气泡产生
D.最后得到的溶液中可能含有Fe3+
10.下列离子方程式书写正确且表示的是复分解反应的是 ( )
A.向硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-=S↓+SO2↑+H2O
B.等物质的量浓度的氯化铝溶液与烧碱溶液按体积比1:4混合:
Al3++4OH-=AlO2-+2H2O
|
D.向硫酸铵溶液中滴加氢氧化钡溶液:Ba2++SO42-=BaSO4↓
9.下列实验操作错误的是 ( )
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.测定中和热的实验中,记录NaOH溶液与盐酸均匀混合后溶液的最高温度
C.测定硫酸铜晶体中结晶水的含量时,小火缓慢加热,防止晶体飞溅
D.配制0.1mol·L-1H2SO4溶液时,将浓硫酸直接注入容量瓶中 ,加水稀释至刻度线
8.下列各组离子在溶液中既可以大量共存,且加入氨水后,也不产生沉淀的是 ( )
A.Na+、Mg2+、Cl-、HCO3- B.H+、NH4+、Al3+、SO42-
C.H+、Cl-、CH3COO-、NO3- D.K+、AlO2-、NO3-、OH-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com