
题目列表(包括答案和解析)
2、现有CuO和Fe2O3组成的混合物a g,向其中加入4.0 mol•L–1硫酸溶液25 mL时恰好完全反应。若将a g原混合物在足量CO中加热,使其充分反应,冷却后剩余固体质量为
A.1.6 g B.1.6a g C.(a-0.8) g D.(a-1.6) g
1、下列是某学生自己总结的一些规律,其中正确的是:( )
A 氧化物不可能是还原产物,只可能是氧化产物
B 有些化学反应不属于化合、分解、置换、复分解中的任何一种反应
C 一种元素可能有多种氧化物,但同种化合价只对应一种氧化物
D 饱和溶液一定比不饱和溶液的浓度大
6.测定铜合金中铜的含量,可以用稀硝酸来溶解样品,也可以用双氧水和稀盐酸溶解样品,其反应的化学方程式为: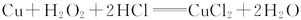 。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
①写出铜与稀硝酸反应的离子方程式并标出电子转移的方向和数目____________________。
②在铜与双氧水、盐酸的反应中氧化剂是______________________________,若有2 mol的H2O2参加反应,则电子转移的物质的量是_______________。
③用双氧水和稀盐酸溶解样品与用稀硝酸溶解样品相比较,哪种更好?为什么?
④若称取样品的质量为a g,用足量的双氧水溶解后,剩余残渣经过洗涤干燥称得质量是b g,则样品中含铜的质量分数为__________。
5.双氧水在常温时能缓慢地分解生成氧气,反应的化学方程式是______________________________;(1)若将反应的温度升高,则反应的速率会__________;(2)若向其中加入少量的MnO2,则反应速率会__________,说明MnO2在该反应中起__________作用。实验室如果用双氧水来制备氧气,你选择上述两种方案的__________(填序号1或2),理由是____________________。
4.实验室制取氯气的反应原理是_______________________________;氯气具有较强的__________性,可以与_____________等反应,分别写出这些反应的化学方程式______________________________。
3.实验室进行下列有关物质的准备中,理论上正确、操作上可行、经济上合理的是( )。
A.
B.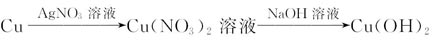
C.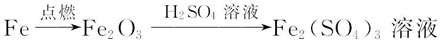
D.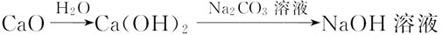
2.通过对本单元的学习,谈谈你对绿色化学的理解。在化学学习中,哪些实验或事实体现了绿色化学的思想?
1.微型实验有哪些特点?实验室里的哪些实验可以改成微型实验?试设计1-2个微型实验。
19.某一氯代烷1.85 g与足量的Na0H水溶液混合后加热,用稀HN03酸化,再加入足量的AgN03溶液,生成白色沉淀2.87 g,试通过计算确定该一氯代烷的分子式,并写出各种同分异构体的结构简式。
18.(6分)根据下面的反应路线及所给信息填空。

(1)A的结构简式 ,B的结构简式 。
(2)反应④所用的试剂和条件是 。
(3)反应⑥的化学方程式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com