
题目列表(包括答案和解析)
23、能正确表示下列反应的离子方程式是
A.氨水中通入过量CO2:2NH3·H2O + CO2 = 2NH4+ + CO32- + H2O
B.氯化亚铁溶液中加入硝酸:Fe2+ + 4H+ + NO3- = Fe3+ + 2H2O + NO↑
C.将标准状况下112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中:
2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 6Cl- + 2Br2
D.用小苏打治疗胃酸过多:HCO-3+H+ = CO2↑+H2O
22、常温下,下列溶液可能大量共存的离子组是
A.含有大量S2-的溶液:Na+、C1O-、C1-、CO32-
B.含有大量Fe3+的溶液:K+、Na+、A1O2-、SO42-
C.能使pH试纸变红的溶液:NH4+、Na+、NO3-、HCO3-
D.水电离产生的c(H+)=1×10-12mol·L-1的溶液:Mg2+、SO42-、NO3-、C1-
21、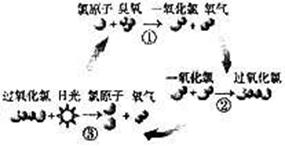 1995年三位美国科学家因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究揭示了大气中臭氧层被破坏的机理,由图可知(
)
1995年三位美国科学家因在氟利昂和臭氧层方面的工作获得诺贝尔化学奖,他们的研究揭示了大气中臭氧层被破坏的机理,由图可知(
)
A.日光在反应中做催化剂
B.过氧化氯是一种很稳定的物质
C.过氧化氯的结构式为O-Cl-Cl-O
D.臭氧分子最终转变为氧气分子
20、灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s、白)+2HCl(aq)=SnCl2(aq)+H2(g) △H1
②Sn(s、灰)+2HCl(aq)=SnCl2(aq)+H2(g) △H2
③Sn(s、灰)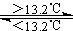 Sn(s、白)
△H3=+2.1kJ/mol
Sn(s、白)
△H3=+2.1kJ/mol
下列说法正确的是
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
19、下表为4种常见溶液中溶质的质量分数和物质的量浓度:
|
溶 质 |
HCl |
NaOH |
CH3COOH |
HNO3 |
|
溶质的质量分数/% |
36.5 |
40 |
60 |
63 |
|
物质的量浓度/mol·L-1 |
11.8 |
14.3 |
10.6 |
13.8 |
这4种溶液中密度最小的是( )
A.HCl B.NaOH C.CH3COOH D.HNO3
18、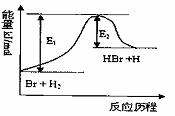 参照反应Br+H2
参照反应Br+H2  HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
A. 该反应的△H=+(E1-E2)kJ/mol
B. 加入催化剂,该化学反应的反应热变大
C. 反应物总能量高于生成物总能量
D. 升高温度可增大正反应速率,降低逆反应速率
17、氯酸质量分数超过40%时会发生分解,反应可表示为:8 HClO3 = 3 O2↑+ 2 Cl2↑+ 4 HClO4 + 2 H2O,下列说法正确的是
A.氧化性比较HClO4 > HClO3 B.氧化产物只有HClO4
C.氯酸分解后的混合气体平均相对分子质量为47.6 D.该反应转移电子数为12e-
16、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3+3ClO―+4OH―=2FeO42-+3Cl―+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4
下列有关说法不正确的是( )
A.高铁酸钾中铁显+3价
B.湿法中每生成1mol Na2FeO4转移3 mol电子
C.干法中每生成1mol Na2FeO4转移4 mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质
15、将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )
A.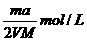 B.
B.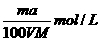 C.
C.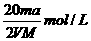 D.
D.
14、只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
|
|
A |
B |
C |
D |
|
甲 |
物质中的粒子数 |
标准状况下的气体摩尔体积 |
固体的体积 |
溶液中溶质的物质的量浓度 |
|
乙 |
阿伏加德罗常数 |
标准状况下的气体的体积 |
固体的密度 |
溶液体积 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com