
题目列表(包括答案和解析)
27.(4分)恒温恒容下lmolO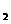 和2molSO
和2molSO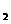 在一个密闭容器中发生反应:
在一个密闭容器中发生反应:
 ,一段时间后反应达到平衡,生成
,一段时间后反应达到平衡,生成
(1)原混合气体与平衡混合气体的压强之比为__________________________________。
(2)达到平衡时,S02和02的转化率之比为_____________________________________。
26.(13分)某化学活动小组设计以下装置,进行不同的实验。其中a为用于鼓入空气的
气囊, b为铜丝螺旋,c为喷有少量碱液的棉花,d中盛有冰水。

(1)若用A装置做乙醛与新制氢氧化铜悬浊液反应的实验,需去掉的仪器是____________。
. 乙醛与新制氢氧化铜悬浊液反应的化学方程式为:
__________________________________________________________________________。
(2)若用A装置做乙醇与乙酸酯化反应的实验,则还需连接的仪器是(填序号)__________,
该仪器中应加入的试剂是____________________。从实验安全角度考虑A装置试管中除加入反应液外,还需加入的物质是_____________________。
(3)该小组同学欲做浓硫酸与铜反应的实验,并检验产生的二氧化硫。他们应选用的装置是(填序号)__________,用于检验产物二氧化硫应选用的试剂是_____________,在所选装置中(填序号)_____________部分是为了减少二氧化硫对空气的污染。
(4)该小组同学欲做乙醇氧化成乙醛的实验,他们应选用的装置是(填序号)______________。
用制得的乙醛溶液再进行银镜反应,正确的操作顺序是(填写序号)____________。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管里加入1 mL 2%的AgNO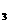 溶液
溶液
写出乙醇催化氧化生成乙醛的化学方程式
______________________________________________________________________________。
(5)该小组同学欲用A装置做铜与浓硝酸反应的实验,请你判断该实验是否可行
(填“是”或“否”),其原因是___________________________________________________。
25.(4分)下列实验能达到预期目的是___________________(填写序号)。
①95%的酒精加入生石灰再蒸馏制得无水乙醇
②配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,至产生沉淀为止
③制乙烯时,温度计应插入反应混合液中并控制温度在140℃
④测定硫酸铜晶体结晶水的质量分数时用潮湿的坩埚
⑤检验C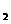 H
H C1中氯元素时,将C
C1中氯元素时,将C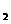 H
H C1与NaOH水溶液混合加热,再加入AgNO
C1与NaOH水溶液混合加热,再加入AgNO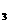 溶液
溶液
⑥蔗糖水解用稀硫酸作催化剂
24.(10分)有机物A为芳香族化合物,能发生如下图所示的变化,其中C能使溴的四
氯化碳溶液褪色,D不含甲基,在一定条件下能发生消去反应。

请填写下列空白:
(1) A分子所含官能团的名称是____________________;C的结构简式是_____________。
(2) C→D的反应类型是_________________(填标号)。
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(3) D+E→F反应的化学方程式是______________________________。
(4) D有多种同分异构体,除D外,其中能与金属钠反应且苯环上只有一个取代基的同
分异构体还有___________________种。
23.(6分)己知A-G有如下转化关系。其中:A为芳香族化合物且苯环上的一溴代
物只有两种,D能使FeCl3溶液显紫色,E、F、G能发生银镜反应。

(1)A的结构简式____________,G的结构简式_______________。
(2)反应①一⑤中可看成取代反应的有_____________(填代号)。
(3)写出B-D反应的化学方程式:
__________________________________________________________________________。
22.(8分)中国的载人飞船“神舟”七号2008年9月25日在酒泉卫星发射中心发射升空。
已知:肼(N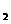 H
H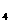 )又称联氨,是具有强还原性的液体化合物,主要用作火箭和喷气发
)又称联氨,是具有强还原性的液体化合物,主要用作火箭和喷气发
动机的燃料部分。
(1)已知在25"C、101kPa时,32.0g N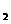 H
H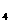 地在氧气中完全燃烧生成氮气,放出热量624kJ,
地在氧气中完全燃烧生成氮气,放出热量624kJ,
N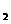 H
H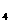 完全燃烧反应的热化学方程式是:
完全燃烧反应的热化学方程式是:
 ____________________________________________________________________________。(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空
____________________________________________________________________________。(2)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼-空
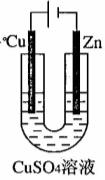
气燃料电池放电时负极的电极反应式是________________________________________。 (3)下图是一个电化学过程示意图。
①锌片上发生的电极反应是_________________________________________________
②假设使用肼一空气燃料电池作为本过程中的电源,当铜片的质量
减少128g时该燃料电池理论上需要标准状况下的空气_______
L(假设空气中氧气体积含量为20%)。
(4)传统制备肼的方法,是以NaCIO氧化NH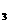 ,制得肼的稀溶液。该
,制得肼的稀溶液。该
反应的离子方程式为:____________________________________
四,有机推断(本题包括2小题,共16分)
21.(8分)下图所示物质转化中,常温下E为无色无味的液体,F为淡黄色粉末,G为
常见的无色气体(反应条件均已省略)。
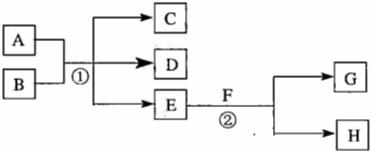
(1)在反应②中,每生成2.24L气体G(标准状况)时,该反应转移电子的物质的量
是____________。
(2)若反应①在加热条件下进行,且C、D是两种均能使澄清石灰水变浑浊的无色气体
则反应①的化学方程式是______________________________________________。
(3)若反应①在溶液中进行,A是一种强碱,B是一种酸式盐,D是一种气体,且B遇盐酸有气体产生。在加热条件下,当A过量时反应①的离子方程式是:
______________________________________________________________________。
(4)若反应①在溶液中进行,A是一种强酸,B是一种含有两种金属元素的盐,且.B的
水溶液显碱性,A、B均由短周期元素构成。则A过量时反应①的离子方程式是:
_______________________________________________________________________。
20.常温下, ,下列叙述正确的是
,下列叙述正确的是
A.该溶液中由水电离出的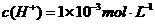
B.由pH=3的HA与pH=1l的NaOH溶液等体积混合,溶液中
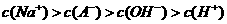
C.浓度均为 的HA和NaA溶液等体积混合后,若溶液呈酸性,则
的HA和NaA溶液等体积混合后,若溶液呈酸性,则

D. 溶液等体积混合后所得溶液中
溶液等体积混合后所得溶液中

唐山市2008'--2009学年度高三年级第一学期期末考试
化学试卷
第Ⅱ卷(非选择题,共60分)
|
三 |
四 |
五 |
六 |
总分 |
||||
|
21 |
22 |
23 |
24 |
25 |
26 |
27 |
28 |
|
|
|
|
|
|
|
|
|
|
19.工业上以CuO和H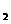 SO
SO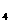 为原料制备CuS O
为原料制备CuS O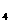 .5H
.5H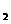 O晶体。为确保制备过程中既不补充水,也无多余的水分,所用硫酸溶液溶质的质量分数应为
O晶体。为确保制备过程中既不补充水,也无多余的水分,所用硫酸溶液溶质的质量分数应为
A.45.8% B.57.6% C.72.3% D.无法确定
18.相同状况下,等体积的下列溶液,阴离子的总浓度最大的是
A.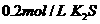 B.
B.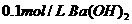
C. D.
D.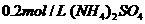
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com