
题目列表(包括答案和解析)
___________从自然界取得的能源称为一次能源,如流水、风力、原煤、石油、天然气等,一次能源经过加工,转换得到的能源为二次能源,如电力、蒸汽、氢能等。
6.选择适宜的材料和试剂设计一个原电池,以便完成下列反应:
2FeCl3 + Cu == 2 FeCl2 + 2CuCl2
(1)画出装置图(标明电极材料和电解质溶液)(2)写出电极反应式。
5. (10分)将洁净的金属片Fe、Zn 、A、B 分别与Cu用导线连结浸在合适的电解质溶液里。实验并记录电压指针的移动方向和电压表的读数如下表所示:
(10分)将洁净的金属片Fe、Zn 、A、B 分别与Cu用导线连结浸在合适的电解质溶液里。实验并记录电压指针的移动方向和电压表的读数如下表所示:
|
金属 |
电子流动方向 |
电压/V |
|
Fe |
Fe
→ Cu |
+0.78 |
|
Zn |
Zn
→ Cu |
+1.10 |
|
A |
Cu
→ A |
-0.15 |
|
B |
B
→ Cu |
+0.3 |
根据以上实验记录,完成以下填空:
(1)构成两电极的金属活动性相差越大,电压表的读数越 (填“大”、“小”)。Zn、A、B三种金属活动性由强到弱的顺序是 。
(2)Cu与A组成的原电池, 为负极,此电极反应式为 。
(3)A、B形成合金,露置在潮湿空气中, 先被腐蚀。
4.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是 ( )。
A. 在熔融电解质中,O2-由负极移向正极
B. 电池的总反应是:2C4H10+13O2 ® 8CO2+10H2O
C. 通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH_
D. 通入丁烷的一极是正极,电极反应为:2C4H10+26e-+13O2-==4CO2+5H2O
3.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)
下列说法错误的是( )。
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e-→Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g
2.镍-镉(Ni-Cd)可充电电池,可以发生如下反应:
Cd(OH)2 +2Ni(OH)2 ===== Cd+2NiO(OH)+2H2O,
由此可知,该电池的负极材料是( )。
A. Cd B. NiO(OH) C. Cd(OH)2 D. Ni(OH)2
1. 锌锰干电池在放电时,电池总反应方程式可以表示为:
Zn+2MnO2+2NH4+ ==== Zn2++Mn2O3+2NH3+H2O
在此电池放电时,正极(碳棒)上发生反应的物质是( )。
A.Zn B.碳棒 C.MnO2和NH4+ D.Zn2+和NH4+
15.(12分)化学电池在通讯、交通及日常生活中有着广泛的应用,目前常用的镍(Ni)镉(Cd)电池,其电池总反应可以表示为:

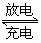

(1)下列有关镍镉电池总反应的说法中,正确的是________(填序号);
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
 (2)已知
(2)已知 和
和 均难溶于水。有资料表明,一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重。这是因为_ _____
__________;
均难溶于水。有资料表明,一节废镍镉电池可以使一平方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重。这是因为_ _____
__________;
(3)另一种常用的电池是锂电池(锂是一种碱金属元素,其相对原子质量为7),由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为 .试回答:
.试回答:
 ①锂电池比容量特别大的原因是__________________________________________;
①锂电池比容量特别大的原因是__________________________________________;
②锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因_______________________________________。
B 卷
(能力提高)
(时间:30分钟 满分:50分)
14.(12分)熔融盐燃料电池具有高的发电效率,因而受到重视。可用Li2CO3和Na2CO3的熔融盐混合物做电解质,CO为负极燃气,空气与CO2的混合气体为正极助燃气,制得在650℃下工作的燃料电池。完成上述有关的电池反应式:
正极反应式:____________________________________________;
负极反应式:____________________________________________;
总电池反应式:__________________________________________。
13.(8分) 我国首创的以铝-空气-海水电池为能源的新型海水标志灯已研制成功。这种灯以取之不尽的海水为电解质溶液,靠空气中的氧使铝不断氧化而源源产生电流。只要把灯放入海水中,数分钟后就会发出耀眼的闪光,其能量比干电池高20-50倍。试推测此种新型电池可能的基本结构及电极反应式:
(1)__________是负极,电极反应式为___________________________。
(2)__________是正极,电极反应式为___________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com