
题目列表(包括答案和解析)
1. 我国成功地发射了嫦娥一号探测卫星,确定对月球土壤中14种元素的分布及含量进行探测等。月球的矿产资源极为丰富,仅月面表层5cm厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8] 和橄榄石[(Mg,Fe)2SiO4]等,下列说法或分析不正确的是 ( )
我国成功地发射了嫦娥一号探测卫星,确定对月球土壤中14种元素的分布及含量进行探测等。月球的矿产资源极为丰富,仅月面表层5cm厚的沙土就含铁单质有上亿吨,月球上的主要矿物有辉石[CaMgSi2O6]、斜长石[KAlSi3O8] 和橄榄石[(Mg,Fe)2SiO4]等,下列说法或分析不正确的是 ( )
A.辉石、斜长石及橄榄石均属于硅酸盐矿
B.斜长石的氧化物形式可表示为:K2O·Al2O3·6SiO2
C.橄榄石中铁为+2价
D.月球上有游离态铁是因为月球上铁的活动性比地球上铁的活动性弱
2.下列有关铁及其化合物的说法中不正确的是 ( )
A.工业上在高温下用CO还原含Fe2O3的铁矿石炼铁
B.铁在纯氧中燃烧或高温下和水蒸气反应均能得到Fe3O4
C.工业上可用铁质容器储存、运输浓硝酸、浓硫酸
D.氯化铁溶液有较强氧化性,故可用作净水剂
3.美国“海狼”核潜艇上的核反应堆内使用了液体铝合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是 ( )
A.原子半径:Na>Al
B.铝钠合金若投入一定水中可得无色溶液,则n(Al)≤n(Na)
C.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出
D.若mg不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越少
4.设计下列实验方案鉴别Na2CO3和NaHCO3两种白色粉末,不能达到预期目的的是( )
A.分别向等量的白色粉末中加等体积、等浓度的稀盐酸,比较生成气体的快慢
B.分别向等量的白色粉末中加等体积适量的水,比较固体溶解量的多少
 C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
C.分别将等量的白色粉末配成溶液,然后加入澄清石灰水,比较是否有沉淀生成
D.分别将等量的白色粉末用右图装置进行实验,比较澄清石灰水是否变混浊
5.按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法 正确的是 ( )
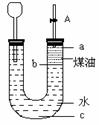 A.打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处
A.打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处
 B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升,进入长颈漏斗,a处有无色气体产生
D.若用苯或酒精来代替煤油,可观察到相同的实验现象
6.钙和钠相似,也能形成含O22-离子的过氧化物,下列叙述不正确的是 ( )
A.过氧化钙的化学式是CaO2
B.1 mol过氧化钙或过氧化钠跟足量的水反应都生成1mol氧气
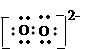
C.O22-离子的电子式为
D.过氧化钙在未开放的花朵旁边,可以延缓花朵的开放.
7.化学中常用类比的方法可预测许多物质的性质。如根据H2+Cl2=2HCl推测:H2+Br2=2HBr。但类比是相对的,如根据2Na2O2+2CO2= Na2CO3+ O2, 类推2Na2O2+2SO2= Na2SO3+ O2是错误的,应该是Na2O2+SO2= Na2SO4。 下列各组类比中正确的是 ( )
A.由NH4Cl NH3↑+HCl↑,推测:NH4I
NH3↑+HCl↑,推测:NH4I NH3↑+HI↑
NH3↑+HI↑
B.由CO2+Ca(ClO)2+H2O=CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O=CaSO3↓+2HClO
C.由2CO2+Ca(ClO)2+2H2O=Ca(HCO3)2+2HClO,
推测:CO2+NaClO+H2O=NaHCO3+HClO
D.由Na2SO3+2HCl=2NaCl+H2O+ SO2↑,推测:Na2SO3+2HNO3=2NaNO3+H2O+ SO2↑
8.近年来,科学家试图探索利用铝粉作为新能源的可能性。假如铝作为一种普遍使用的新型能源被开发利用,下列关于其有利因素的说法中,肯定不成立的是 ( )
 A.铝矿资源比较丰富
A.铝矿资源比较丰富
B.铝燃烧时热值高
C.铝质轻,有利于运输和贮存
D.用电解法冶炼铝的工业技术是铝作为新能源的重要基础
9.铝、铍(Be)及其化合物具有相似的化学性质,如其氯化物分子内键型相同,故其氯化物晶体的熔点都较低。已知反应:BeCl2+Na2BeO2+2H2O=2NaCl+2Be(OH)2↓能完全进行,则下列推断正确的是 ( )
 A.Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO
A.Na2BeO2溶液的pH>7,将其蒸干并灼烧后得到的残留物为BeO
B.BeCl2溶液的pH<7,将其蒸干并灼烧后得到的残留物可能是BeCl2
C.Be(OH)2既能溶于盐酸,又能溶于NaOH溶液
D.BeCl2水溶液的导电性强,故BeCl2是离子化合物

|
A.铝与硝酸汞反应属放热反应
B.铝是一种较活泼的金属,
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
11.将下列四种铁的化合物溶于稀HCl,滴加KSCN溶液没有颜色变化,再加入氯水呈红色的是 ( )
A.FeO B.Fe2O3 C.FeCl3 D.Fe2(SO4)3
12.要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作的最佳顺序为( )
①加入足量氯水 ②加入足量KMnO4(H+)溶液 ③加入少量NH4SCN溶液
A.①③ B.③② C.③① D.①②③
13.把铝粉和某铁氧化物xFeO·yFe2O3粉末配成铝热剂,再分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是8:11,则x:y为 ( )
A.1:2 B.2:3 C.5:7 D.7:5
14. 某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部投50mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部投50mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
下列说法正确的是 ( )
A.若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解
B.若金属全部溶解,则溶液中一定含有Fe3+
C.若金属全部溶解,且产生336mL气体(标准状况),则b=0.3
D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b>80y(1-a/3)
15. 现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质可以发生反应,下列判断不合理的是 ( )
现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质可以发生反应,下列判断不合理的是 ( )
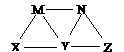 A.X一定是碳酸钠溶液
A.X一定是碳酸钠溶液
B.Y一定是氯化铁溶液
C.Z可能为碳酸氢钠溶液
D.M、N必定各为苯酚、氢氧化钠溶液中的某一种
第Ⅱ卷(非选择题 共55分)

|
19. (8分)将Na2CO3和NaHCO3混合物19g,充分加热后,收集到CO2有1.12L(标准状况),冷却后将剩余固体溶于300ml水中,求:
(8分)将Na2CO3和NaHCO3混合物19g,充分加热后,收集到CO2有1.12L(标准状况),冷却后将剩余固体溶于300ml水中,求:
(1)原混合物中Na2CO3的质量。
(2) 配制的溶液的物质的量浓度
18.(10分)在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下"Fe与水蒸气反应的实验"。
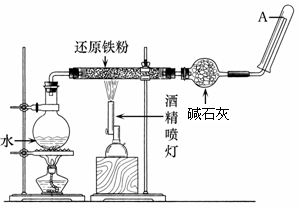 请回答该实验中的问题。
请回答该实验中的问题。
(1)写出该反应的化学方程式 ;
(2)实验前必须对整套装置进行的操作是 ;
(3)碱石灰的作用是
;
(4) 试管中收集到的气体是 ,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行,检验这一操作的目的是
。
(5)如果改用排水集气法收集产生的气体,是否还需要用到碱石灰?
,理由是 。

17.(6分)有一瓶存放时间较长的硫酸亚铁,外观上并无明显变化,但某学生怀疑其有部分因氧化而变质,请你设计1个检验硫酸亚铁是否变质的实验方案:
。
如果有变质,当配制硫酸亚铁溶液时,应如何除去变质的杂质?
。
16.(10分)解释钠投入滴有酚酞试液的水中,产生下列现象的原因:
(1) 钠浮在水面
(2) 钠熔化成闪亮的小球
(3)
 钠小球在水面四处游动,并发出“嘶嘶”声
钠小球在水面四处游动,并发出“嘶嘶”声
(4) 钠逐渐变小,最后完全消失
(5)
 滴有酚酞试液的水变红
滴有酚酞试液的水变红
15.(10分)某固体化合物A,按下图所示发生系列变化,已知E溶液中加入氨水后产生的白色沉淀很快变为灰绿色,最后变为红褐色

写出上述变化中各步反应的化学方程式
①
②
③
④
14.下列各组物质的溶液中,分别加入足量氨水,观察到的现象相同的是
A. FeCl3, AlCl3 B. NaCl, BaCl2 C. MgCl2, CuCl2 D. FeCl2, FeCl3
13. 镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应, 过滤后向滤液中加入过量烧碱溶液, 再过滤, 滤液中存在的离子有
镁、铝、铜三种金属粉末混合物, 加入过量盐酸充分反应, 过滤后向滤液中加入过量烧碱溶液, 再过滤, 滤液中存在的离子有
A.Cu2+ B.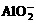 C.Al3+ D.Mg2+
C.Al3+ D.Mg2+
12.下列操作中,溶液的颜色不发生变化的是
A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液
C.铁丝置于氯化铜溶液中一段时间 D.氯化铁溶液中加入还原性铁粉
11.铝在人体中积累可使人慢性中毒,世界卫生组织将铝确定为食品污染源之一而加以控制。铝在下列使用场合中,必须加以控制的是
A.制造炊具 B.制防锈油漆 C.制铝合金窗 D.炼铝厂制造铝锭
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com