
题目列表(包括答案和解析)
13.4:3:2
解析:由题意,可知混合物与足量水反应生成的H2、O2总物质的量为 ,且其中H20.02mol,O20.01mol。根据2Na-H2和2Na2O2-O2可知,原混合物中含Na0.04mol,含Na2O2为0.02mol,所以Na2O的物质的量应为:
,且其中H20.02mol,O20.01mol。根据2Na-H2和2Na2O2-O2可知,原混合物中含Na0.04mol,含Na2O2为0.02mol,所以Na2O的物质的量应为: ,因此原混合物中Na、Na2O、Na2O2的物质的量之比为4:3:2。
,因此原混合物中Na、Na2O、Na2O2的物质的量之比为4:3:2。
12.(1)⑤③④⑥⑦②①⑧(⑥、⑦可换位) (2)大理石盐酸 (3)除去混在O2中未反应的CO2吸收CO2中混有的HCl(4)ac
解析:C中产生的CO2气体须通过NaHCO3溶液除去,其中混有的HCl气体,CO2气体与Na2O2固体反应后产生的O2中不可避免地混有CO2气体,须通过NaOH溶液除去。洗气装置中气流的方向注意应为长管进、短管出。为准确量得生成O2的体积,在反应前后读取甲管中液面的读数时,应上下移动乙管使甲乙两管液面相平,以保证甲管液面上方为1个大气压。读数时视线应与凹液面最低处相平。
点评:此实验题设计新颖,既考查了重点的化学知识、实验能力,又体现了学科间综合的精神。解答此类题目时思考要周密,叙述要简洁规范。
11.B解析:钠在铁盐溶液中先与H2O发生反应,故不能置换出铁。
2Na+2H2O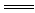 2NaOH+H2↑
2NaOH+H2↑
铁可置换出铜盐溶液中的铜,如:Fe+CuSO4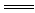 FeSO4+Cu。Fe在高温下可以与H2O(g)发生反应而生成Fe3O4和H2。在金属活动性顺序表中Al排在Fe的前面,故Al比Fe活泼。
FeSO4+Cu。Fe在高温下可以与H2O(g)发生反应而生成Fe3O4和H2。在金属活动性顺序表中Al排在Fe的前面,故Al比Fe活泼。
10.C解析:设18.4g铝锌合金中含铝 mol,含锌
mol,含锌 mol,则由:
mol,则由:
 2Al-3H2↑,Zn-H2↑
2Al-3H2↑,Zn-H2↑

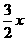


 得
得 解之,得
解之,得
则铝、锌分别产生的氢气体积比为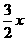 :
: =3:2。
=3:2。
9.D解析:A、B、C中都是钠与酸(或水)反应,它与放出的氢气的关系式为2Na-H2;而D中除了Na与水反应放出H2外,铝还会与生成的NaOH反应放出一定量的H2即2Al+2NaOH+2H2O 2NaAlO2+3H2↑,故D中放出的氢气最多。
2NaAlO2+3H2↑,故D中放出的氢气最多。
8.A解析:根据铝与酸、碱反应的化学方程式:
2Al+6HCl=2A1C13+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
可以发现:等量的铝分别与足量的酸、碱反应会产生等量的H2(同温同压),故题中答案选A。
7.A解析:由题意知Na2O和Na2O2物质的量相等且由方程式易知,Na2O放在溶液中增加的质量为Na2O2中的Na2O部分。
由此可知两溶液的质量相同,则a=b,选A。
6.C解析:Na2O是白色固体,Na2O2是淡黄色固体;Na2O是碱性氧化物,Na2O2不是碱性氧化物;Na2O2是强氧化剂,Na2O不是,因此只有C是正确的。
5.D解析:2.3g钠与100g水完全反应后生成4gNaOH,同时放出0.1gH2,故反应后溶液的质量分数为 (NaOH)=
(NaOH)= 100%。
100%。
4.C解析:水的密度为lg·cm-3,而煤油的密度为0.8g·cm-3,钠可浮在水面上,说明其密度比水的小,而沉在煤油中说明其密度比煤油大,则其密度应介于0.8g·cm-3-1.0g·cm-3之间。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com