
题目列表(包括答案和解析)
9.下列各组离子能在指定溶液中,可能大量共存的是
①无色溶液中:K+、Na+、CO32-、SO42- ②pH=11的溶液中:Na+、Na+、AlO2-、ClO-
③水电离出的c(H+) =10-12mol·L-1的溶液中:Mg2+、NH4+、HCO3-、S2-
④加入Al放出H2的溶液中:Cu2+、NH4+、Cl-、NO3-
⑤使甲基橙变红的溶液中:K+、Fe3+、ClO3-、NO3-
⑥酸性溶液中:Fe2+、Al3+、NO3-、Cl-
A.①②⑤ B.①③⑥ C.②④⑤ D.①②④
8.下列排列顺序正确的是
① 固体的热稳定性:CaCO3>Na2CO3>NaHCO3 ② 还原性:SO32->I->Br-
③ 微粒半径:K>Na+>O2- ④ 结合H+的能力:OH->AlO2->HCO3-
⑤ 氢化物的沸点: H2O>NH3>HF
A.①③ B.②④ C.①② D.③⑤
7.三聚氰酸C3N3(OH)3可用于消除汽车尾气中的氮氧化物。当加热至一定温度时,它分解产生的HNCO(异氰酸,其结构是H-N=C=O)能和NO2反应:HNCO+NO2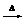 N2+CO2+H2O(未配平)。下列关于该反应的叙述正确的是
N2+CO2+H2O(未配平)。下列关于该反应的叙述正确的是
A.N2是还原产物,CO2是氧化产物质 B.每生成1 mol CO2需转移12 mol电子
C.反应中氧化剂和还原剂的物质的量之比为3∶2网 D.N元素既被氧化也被还原
6.下列关于反应类型的判断正确的是
A.2Al+2NaOH+2H2O===2NaAlO2+3H2↑ 置换反应
B.FeCl3溶于水发生的反应 复分解反应
C.C2H5OH+HBrC2H5Br+H2O 复分解反应
D.IBr+H2O HBr+HIO
氧化还原反应
HBr+HIO
氧化还原反应
5.关于ⅠA族和ⅡA族元素的下列说法中正确的是
A.加热时,Na2CO3比MgCO3易分解
B.浓度都是0.01 mol·L-1时,KOH溶液的pH比Ba(OH) 2的小
C.Na的熔点比Mg高,Na2O的熔点比MgO的高
D.NaOH是一元碱,Mg (OH) 2是二元碱,后者碱性强
4.下列叙述中正确的是
A.在碱金属元素中,所有碱金属的氧化物均属于碱性氧化物
B.由于碱金属形成的碱均为强碱,所以碱金属形成的盐均不会水解
C.金属锂不能保存于煤油中,金属钾可以保存于煤油中
D.做焰色反应时应用硫酸洗铂丝
3.在一定温度下,向饱和的烧碱溶液中加入一定量的Na2O2,充分反应后,恢复到原来的温度,下列说法中正确的是
A.溶液的pH不变,有H2放出 B.溶液的pH值增大,有O2放出
C.溶液中c(Na+)增大,有O2放出 D.溶液中Na+数目减少,有O2放出
2.以下说法中能证明无色透明液体是纯净水的是
A.测得该液体pH=7 B.电解该液体得到氢气和氧气,且其体积比为2:1
C.向其中投入金属钠,钠于液面上迅速游动,并发出丝丝声
D.在l.0l×105Pa压强下测得沸点为373.15K
1.关于Na2CO3溶液和NaHCO3溶液,下列说法正确的是
A.用加热的方法区别两种溶液 B.用澄清的石灰水区别两种溶液
C.浓度相同时,Na2CO3溶液的pH大 D.浓度相同时,两溶液的pH相等
14.方法一:可以使用NaOH溶液洗涤混合物,铁与NaOH溶液不发生反应,而Al可溶于NaOH溶液。
2Al+2NaOH+2H2O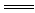 2NaAlO2+3H2↑
2NaAlO2+3H2↑
经过滤、洗涤可以得到铁。
 方法二:可以使用磁铁将混合物中的铁吸引出来而留下杂质铝。
方法二:可以使用磁铁将混合物中的铁吸引出来而留下杂质铝。
 方法三:向混合物中加FeCl3溶液,Al与FeCl3反应:A1+FeCl3
方法三:向混合物中加FeCl3溶液,Al与FeCl3反应:A1+FeCl3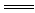 Fe+AlCl3,用水洗涤并干燥。
Fe+AlCl3,用水洗涤并干燥。
点评:本题为设计新颖的开放型题目。铁和铝的性质不同,解答此类题目时要积极调动大脑贮存的知识,抽取相关知识灵活应用作答。当然这也有赖于平时一点一滴、扎扎实实的知识和能力的积累。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com