
题目列表(包括答案和解析)
1、2008年9月27日16时41分,航天员翟志刚身着“飞天”航天服出舱活动,茫茫太空中第一次留下中国人的足迹。“飞天”舱外航天服是我国自行研制的,使用了多种新材料。下列对材料的说法错误的是( )
A.新材料的开发和应用,是社会发展和人类进步的一种标志
B.水泥、玻璃、陶瓷属于新型无机非金属材料
C.传统的无机非金属材料虽有不少优点,但质脆、经不起热冲击
D.新型结构陶瓷具有承受高温、抗氧化、耐磨损、密度小等特点,可应用于宇航事业
16、在标准状况下,进行甲、乙、丙三组实验:三组各取60mL 同浓度盐酸溶液,加入同一种镁铝合金粉末,产生气体,有关数据列表如下:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
510 |
770 |
918 |
|
气体体积/mL |
560 |
672 |
672 |
则下列说法正确的是
A.甲组和乙组的实验中,盐酸均是过量的
B.盐酸的物质的量浓度为0.8 mol·L―1
C.合金中镁铝的物质的量之比为1∶1
D.丙组中铝的物质的量为0.009 mol
株洲市二中2010届高三年级第三次月考
|
座位号 |
|
|
|
|
15、短周期的三种元素X、Y和Z,它们元素原子的最外层电子数分别为1、4、6。则这三种元素所组成的化合物得分子式不可能是
A:XYZ B:X2YZ
C:X2YZ2 D:X2YZ3
14、实验室有一瓶久置的白色K2SO3粉末,为确定其是否被氧化及其成分,元素分析表明粉末中K和S元素的质量比为39∶16,下列结论正确的是
A.根据元素分析结果推测该粉末为纯净物
B.将粉末溶于水,加入氯化钡,有白色沉淀生成,证明原粉末是K2SO4
C.将粉末加入盐酸中,产生气泡,证明原粉末是K2SO3
D.将粉末溶于水,加入氯化钡和过量的盐酸,有白色沉淀和气泡生成 ,证明原粉末是K2SO4和K2SO3的混合物
13、某无色溶液中只可能含有Na+ 、Ba2 +、 Cl一、 Br一、SO32一、SO42一,对该溶液进行下列实验,实验操作和现象如下表:
|
步骤 |
操 作 |
现 象 |
|
(1) |
取少量溶液滴加几滴石蕊试液 |
溶液变蓝 |
|
(2) |
另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 |
上层无色,下层呈橙红色 |
|
(3) |
取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3,过滤 |
有白色沉淀产生 |
|
(4) |
向(3)的滤液中加入过量AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是
A.可能含有 Cl一、 SO32一、SO42一 B.肯定没有 Ba2 +、Cl一、Br一
C.不能确定 Na+ 、 SO32一、SO42一 D.肯定含有 Na+、 Br一、SO32一
12、关于下列四个图像的说法中正确的是
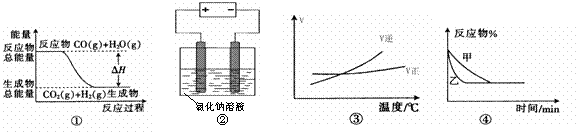
A.图①表示可逆反应“CO(g) + H2O(g) CO2(g)+H2(g)”中的ΔH大于0
CO2(g)+H2(g)”中的ΔH大于0
B.图②是在电解氯化钠稀溶液的电解池中,阴、阳极产生气体体积之比一定为1︰1
C.图③表示可逆反应“A2(g)+3B2(g) 2AB3(g)”的ΔH小于0
2AB3(g)”的ΔH小于0
D.图④表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大
11、 下列各选项中所述的两个量,前者一定大于后者的是
A.将pH=4的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量
B.pH=10的NaOH和Na2CO3溶液中,水的电离程度
C.物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH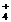 的物质的量浓度
的物质的量浓度
D.相同温度下,10mL 0.1mol/L的醋酸与100mL 0.01mol/L的醋酸中H+的物质的量
10、工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为:
⑴4FeO·Cr2O3+8Na2CO3+7O2 
 8Na2CrO4+2Fe2O3+8CO2
8Na2CrO4+2Fe2O3+8CO2
⑵2Na2CrO4+H2SO4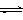 Na2SO4+Na2Cr2O7+H2O
Na2SO4+Na2Cr2O7+H2O
下列说法正确的是
A.反应⑴和⑵均为氧化还原反应
B.反应⑴的氧化剂是O2,还原剂是FeO·Cr2O3
C.高温下,O2的氧化性大于Fe2O3小于Na2CrO4
D.生成1mol的Na2Cr2O7时共转移3 mol电子
9、下列离子方程式书写正确的是
A.金属钠投入CuSO4溶液中: 2Na+Cu2+=2Na++Cu
B.小苏打溶液中加入过量石灰水
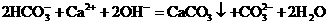
C.Na HSO4溶液中滴加Ba(OH)2至中性:Ba2++SO42-+2H+ +2OH-=Ba SO4↓+2H2O
D.铜跟浓硝酸反应: 3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO↑ + 4H2O
8、在指定环境中,下列各组离子一定可以大量共存的是
A.使pH试纸呈红色的溶液: Fe2+、NO3-、SO42-、Na+
B.使无色酚酞试液显红色的溶液: S2-、K+、HCO3-、AlO2-
C.在加入铝粉放出氢气的溶液: Na+、Cl-、NH4+、NO3-
D.在c(H+)/c(OH-) = 1×1013的溶液: NH4+、Mg2+、Cl-、K+学
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com