
题目列表(包括答案和解析)
2、生物体中细胞膜内的葡萄糖与细胞膜外富氧液体及细胞膜构成微型的生物原电池。下列有关电极反应及产物的判断正确的是:
A.负极反应可能是O2+2H2O+4e- =4OH-
B.负极反应的产物主要是C6H12O6 被氧化生成的CO32-、HCO3-、H2O
C.正极反应可能是6C6H12O6-24e- + 24OH-==6CO2+18H2O
D.正极反应的产物主要是C6H12O6生成的CO2、CO32-、H2O
1、蓄电池在放电时起原电池作用,在充电时起电解池作用,
下列是爱迪生蓄电池分别在充电和放电时的反应:Fe +NiO2+2H2O放电充电Fe(OH)2+ Ni(OH)2,下列有关爱迪生蓄电池的推断中不正确的是( )
A.放电时Fe作负极,NiO2作正极
B.放电时溶液中的阳离子向正极移动
C.充电时的阴极反应是Fe(OH)2 +2e- == Fe + 2OH-
D.该蓄电池既可用KOH溶液又可用稀H2SO4作电解质溶液
4、掌握电解前后溶液的浓度和pH值变化的计算。
典型例题
[例1]⑴今有2H2+O2  2H2O反应,构成燃料电池,则负极通的应是
2H2O反应,构成燃料电池,则负极通的应是
,正极通的应是 ,电极反应式为负极: ,正极: 。
⑵若把KOH改为稀H2SO4作电解质,则电极反应式为负极: ,
正极: 。⑴和⑵的电解质不同,反应进行后,其溶液的pH个有什么变化 。
⑶若把H2改为CH4,用KOH作电解质,则电极反应式为负极: ,
正极 。
[例2] (2003年南通四市联考试题)右图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:
(1)直流电源中,M为 极。
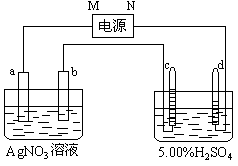 (2)Pt电极上生成的物质是 ,其质量为 __g。
(2)Pt电极上生成的物质是 ,其质量为 __g。
(3)电源输出的电子,其物质的量与电极b、c、d分别生成的物质的物质的量之比为:2∶___∶_ ∶ 。
(4)AgNO3溶液的浓度(填增大、减小或不变。下同) ,AgNO3溶液的pH ,H2SO4溶液的浓度 ,H2SO4溶液的pH ___。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为 g。
课堂练习
3、熟练掌握电解池电极名称、材料、电解质种类等的判断;会书写电极反应式和电解总反应方程式;
2、掌握几种新型燃料电池的工作原理;
1、熟练掌握原电池的电极名称、电子流向、电极反应式及原电池总反应式;
11.将0.05mol/L的盐酸溶液和未知浓度的NaOH溶液以1︰2的体积比混和,所得溶液的pH=12,用上述NaOH溶液滴定pH=3的某一元弱酸溶液20mL,达到终点时消耗NaOH溶液12.5mL,试求:
(1)NaOH溶液的物质的量的浓度 ;
(2)此一元弱酸的物质的量的浓度 ;
10.某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①需配制0.1 mol·L-1 的盐酸和0.1mol·L-1 的氢氧化钠溶液;
②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后加入20.00mL蒸馏水;
③以酚酞为指示剂,用0.1mol·L-1 的氢氧化钠溶液滴定,需用去VmL达滴定终点;
④加入25.00mL0.1mol·L-1 的盐酸溶液。
(1)写出实验过程的步骤(写编号顺序)______________。
(2)下图所示的仪器中配制0.1mol·L-1 盐酸溶液和0.1mol·L-1 氢氧化钠溶液肯定不需要的仪器是(填序号)_________,配制上述溶液还需要的玻璃仪器是(填仪器名称)__________。
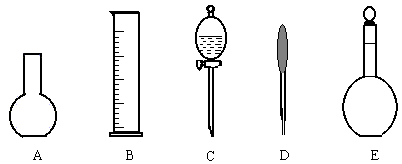
(3)配制上述溶液应选用的容量瓶的规格是(填字母)__________________。
(A)50mL、50mL (B)100mL、100mL
(C)100mL、150mL (D)250mL、250mL
(4)写出有关的化学方程式_____________________________。
(5)胃药中含碳酸钙的质量是________。
9.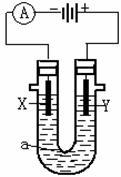 电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两电极板,通过导线与直流电源相连。回答以下问题:
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a;X、Y是两电极板,通过导线与直流电源相连。回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。在X极附近观察到的现象是 。
②Y电极的电极反应式为 ,检验该电极反应产物的方法是 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X的电极材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
8.下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )
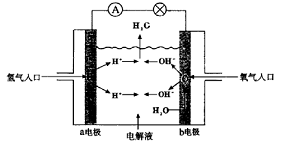
A.a电极是负极
B.b电极的电极反应为:4OH- - 4e-=2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com