
题目列表(包括答案和解析)
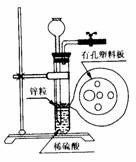
7.右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀 硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中加入的试剂是 ( )
①食盐水 ②KNO3溶液 ③适量硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①②④ B.②⑥ C.②③⑤ D.①③⑤
6.用NA代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
A.78g过氧化钠晶体中,含2NA个阴离子
 B.常温常压下,22.4L氦气含有NA个氦原子
B.常温常压下,22.4L氦气含有NA个氦原子
C.在标准状况下,22.4L SO3含氧原子个数是3NA
D.常温下16g O2与O3的混合气体中含氧原子数为NA
5.在某溶液中加入铝片有氢气产生,则在该溶液中可能大量共存的离子组是 ( )
A.Cl- NO3- Mg2+ Ca2+ B.SO42- CH3COO- Al3+ Mg2+
C.Na+ K+ SO42- Cl- D.NH4+ Ba2+ Cl- HCO3-
4.下列各组溶液中(浓度均为0.1 mol·L-1)只用胶头滴管和试管,不用其他试剂就可以区别的是 ( )
A.CaCl2和Na2CO3 B.稀H2SO4和NaHCO3
C.Ba(OH)2和NaCO3 D.NaA1O2和盐酸
3.下列反应的离子方程式正确的是 ( )
A.次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2===CaCO3↓+2HClO
B.FeSO4溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2O
C.用氨水吸收少量SO2:NH3·H2O+SO2===NH4++HSO3-
D.硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3↓+3NH4+
2.以下物质间的每步转化通过一步反应能实现的是 ( )
A.Al-Al2O3-Al(OH)3-NaAlO2 B.N2-NO-NO2-HNO3
C.S-SO3-H2SO4-MgSO4 D.Fe-FeO-Fe(OH)2-Fe(OH)3
1.目前,工业上冶炼铝通常采用的方法是 ( )
A.CO或氢气还原法 B.铝热反应法 C.电解法 D.热分解法
21、(10分)
将多少克钠投入10g水中,反应后生成的溶液在10°C时刚好饱和?此饱和溶液中溶质的质量分数是多少?(已知10°C时该溶液中溶质的溶解度为22g)
20、(14分)
(1)已知在一定条件下可以发生下列反应:H2O2+2Fe2++2H+?2Fe3++2H2O
H2O2+2Fe3+?2Fe2++O2↑+2H+
在以上反应中Fe2+实际上起着 作用,
总反应式为 。
 (2)I2也与Fe2+一样能发生上述类似反应,类比(1)在下面填入配平的合适的化学反应方程式:
(2)I2也与Fe2+一样能发生上述类似反应,类比(1)在下面填入配平的合适的化学反应方程式:
 H2O2+I2?2HIO,
,总反应式为
。
H2O2+I2?2HIO,
,总反应式为
。
(3)在H2SO4和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,并可以使淀粉变蓝。有学生认为该反应的离子方程式为:H2O2+2I-?I2+O2↑+2H+,这个方程式正确吗?
,理由是 。
(4)若将H2O2滴入酸性高锰酸钾溶液中,产生无色气体,同时溶液的紫色变浅,无沉淀生成,写出反应的离子方程式 。
19、(12分)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)?CO2(g); △H ?E1
途径II:先制水煤气:C(s)+H2O(g)?CO(g)+H2(g); △H ?E2
再燃烧水煤气:H2(g)+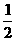 O2(g)?H2O(g); △H ?E3
O2(g)?H2O(g); △H ?E3
CO(g)+ 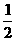 O2(g)?CO2(g); △H ?E4
O2(g)?CO2(g); △H ?E4
试回答:
(1)等质量的煤分别通过以上两条不同途径产生的可利用的总能量的关系正确的是 。
A、I比II多 B、I比II少 C、I与II在理论上相同
(2)E1、E2、E3、E4之间的关系为 。
(3)由于制取水煤气反应里,反应物所具有的总能量 (填“高于”或“低于”)生成物所具有的总能量,所以在化学反应时,反应物就需要 (填“吸收”或“释放”)能量才能转化为生成物,因此该反应的条件为 。
(4)与途径I相比,途径II的优点是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com