
题目列表(包括答案和解析)
11.氮化硅(Si3N4)是一种具有耐高温等优异性能的新型陶瓷。工业上可用下列方法制取:
3SiO2+6C+2N2 Si3N4+6CO。下列说法正确的是( )
 A.氮化硅晶体熔点低
A.氮化硅晶体熔点低
B.氮化硅中氮元素的化合价为―3
C.上述反应中,N2是还原剂,SiO2是氧化剂
D. 反应中,每生成1mol Si3N4,N2得到6mol电子
10.常温下,下列各组离子在所给条件下能够大量共存的是 ( )
A.pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42-
B.水电离出的c(H+)=1×10-10mol/L的溶液中:K+、HCO3-、Na+、S2-
C.使pH试纸显深蓝色的溶液中:Cu2+、Fe3+、NO3-、SO42-
D.能与金属铝反应放出氢气的溶液:Mg2+、SO42-、NO3-、Na+
9.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图装置),下列有关说法正确的是( )
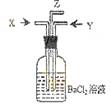 A. 在Z导管口有红棕色气体出现
A. 在Z导管口有红棕色气体出现
B.洗气瓶中产生的沉淀是亚硫酸钡
C. 在Z导管出来的气体中无二氧化碳
D.洗气瓶中产生的沉淀是碳酸钡
8.下列各组中的两种物质作用,反应条件或反应物的用量改变时,对生成物没有影响的是
A.NaOH与 CO2 B. Na2O2 与CO2
C.NaOH与AlCl3 D.Na与O2
7.下列有关铁元素的叙述中正确的是 ( )
A.Fe(OH)2 易被氧化成Fe(OH)3,说明稳定性:Fe(OH)2 < Fe(OH)3
B.铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3
C.氢氧化铁与氢碘酸反应:Fe(OH)3+3HI=FeI3+3H2O
D.铁元素位于周期表的第四周期第VIIIB族
6. 下列叙述中,正确的是( ) A、含金属元素的离子一定都是阳离子 B、在氧化还原反应中,非金属单质一定是氧化剂 C、某元素从化合态变为游离态时,该元素一定被还原 D、金属阳离子被还原不一定得到金属单质
5.北京2008奥运会金牌直径为70mm,厚6mm。三位同学猜想:甲认为金牌是由纯金制造;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金)。为了验证他们的猜想,请你选择一种试剂来证明甲、乙、丙猜想的正误 ( )
A.硫酸铜溶液 B.盐酸 C.稀硝酸 D.硝酸银溶液
4.工业上获得有关物质的方法或途径正确的是
A.将氯气通入澄清石灰水,获得漂白粉
B.工业上,用SiO2+2C Si+2CO↑制得粗硅
Si+2CO↑制得粗硅
C.钠可把钛、锆、铌、钽等金属从它们的卤化物溶液里还原出来
D.将二氧化硫通入过氧化氢溶液,获得硫酸
3.下列除杂质的方法不可行的是( )
A.用过量氨水除去Al3+溶液中的少量Fe3+
B.将混合气体通过灼热的铜网除去N2中的少量O2
C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水
D.用盐酸除去AgCl中少量的Ag2CO3
2.某学生用氯气消毒的自来水配制下列溶液,药品变质的是( )
A.NaNO3 B.FeCl2 C.Na2SO4 D.AlCl3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com