
题目列表(包括答案和解析)
28. (16分)某探究小组的同学设计实验探究铁与水蒸气的反应,并探究反应后生成物的一系列性质。
(16分)某探究小组的同学设计实验探究铁与水蒸气的反应,并探究反应后生成物的一系列性质。
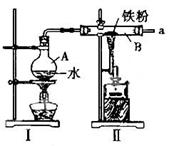
(1)右图为铁与水蒸气反应的实验装置,实验前应先检验装置的气密性,简述其检验的方法_________
____________________________________________________________________。
(2)图I为产生水蒸气的装置,仪器A中除蒸馏水外,还需加入某种固体,其作用是_____________________________________________________________。
(3)图II为铁与水蒸气反应的装置,写出硬质玻璃管B内所发生反应的化学方程式______________________________________________。
(4)为难硬质玻璃管B中反应后的气体产物是H2,还需从下图中选择必要的仪器和药品,设计出一套装置,其连接顺序为:a连_______,_______连_______,_______连________。(填下列装置的接口字母)

(5)反应后,将图II装置中硬质玻璃管B内的全部固体置于试管中,加入60mL1mol/L的稀盐酸,固体恰好完全溶解,再滴加KSCN溶液,发现溶液不显血红色,写出此过程中所有可能发生反应的离子方程式______________________
__________________________________________________________________。反应前硬质玻璃管B中加入Fe粉的质量为__________g.
13.下列叙述正确的是(NA表示阿伏加德罗常数)( )
A.H2O2中加入MnO2,当产生0.1 mol O2时转移电子数为0.4 NA
B.某氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目小于3 NA
C.晶体Na2O2和Na2O各1mol,其含有的离子数分别为4 NA和3NA
D.工业上电解法精炼铜,转移1mol电子时阳极上溶解的铜原子数可能少于0.5 NA
选择题答题表:
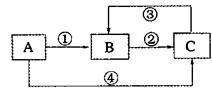 27.(12分)A、B、C三种物质中均含有同一种元素,它们之间有如下图所示的转化关系(部分反应物质已略去)。
27.(12分)A、B、C三种物质中均含有同一种元素,它们之间有如下图所示的转化关系(部分反应物质已略去)。
(1)若A是一种两性氧化物,B的水溶液呈酸
性,请写出反应①和反应④(由A一步转化为B
或C)的离子方程式:反应① _____
__________________ 、反应④ _______________________ ;
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,请写出这两个反应的化学方程式:C→A ;C→B ;
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应②和③可能的离子方程式:② ;③ 。
12.下列操作所得物质为纯净物的是( )
A.将一块带有氧化膜的铝片与过量的浓NaOH溶液完全反应后,取澄清溶液将其蒸干,得纯净的NaAlO2固体
B.向NaAlO2溶液中加入过量的AlCl3溶液,将所得沉淀过滤洗涤,加热灼烧去掉水分,可得纯净的Al(OH) 3固体
C.把铝块与适量的稀盐酸完全反应, 将所得溶液蒸干,可得AlCl3固体
D.把AlCl3溶液与足量氨水反应,将沉淀过滤、洗涤、灼烧去掉水分可得Al2O3固体
11.有Fe2+、NO-3、Fe3+、NH+4、H+和H2O六种粒子,分别属于同一个氧化还原反应中的反应物和生成物。下列叙述正确的是( )
A.反应中NH+4被氧化 B.氧化剂与还原剂的物质的量之比为8:1
B.氧化剂与还原剂的物质的量之比为8:1
C.若有10molH+参加反应,则生成的水的物质的量为5mol
D.生成物中加入KSCN溶液后变红色
10.CuCO3和Cu2(OH)2CO3的混合物34.6g,可恰好完全溶解于300mL2mol·L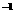 的盐酸溶液中,加热分解等量的这种混合物可得CuO的质量为( )
的盐酸溶液中,加热分解等量的这种混合物可得CuO的质量为( )
A.16.0g B.19.2g C.24.0g D.30.6g
9.向一定量的Fe、FeO和Fe2O3的混合物中加入120mL 4mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24 mol B.0.21 mol C.0.16 mol D.0.14 mol
8.下列实验中,颜色的变化与氧化还原反应有关的是( )
A.往紫色石蕊试液中加入盐酸,溶液变红
B.饱和FeCl3溶液在沸水中变成红褐色胶体
C.向FeSO4溶液中滴加NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
D.向滴有酚酞的NaOH溶液中通人SO2,溶液褪色
7.2007年7月2日,美、德两国成功合成出具有化学特性的氢铝化合物(AlH3)n,最简单的氢铝化合物是Al2H6,它的熔点为150 ℃,燃烧热极高。下列关于氢铝化合物的推测不正确的是( )
A.氢铝化合物与水反应生成氢氧化铝和氢气
B.氢铝化合物中铝显+3价,H显-1价
C.氢铝化合物中不可能存在AlnH2n+2(n为正整数)
D.氢铝化合物具有强还原性
6.在Fe2(SO4)3溶液中,加入ag铜,完全溶解后,再加bg铁,充分反应后得到cg残余固体,且a>c,则下列说法正确的是( )
A.残余固体是铜和铁
B.最后得到的溶液中一定含有Cu2+
C.将残余固体加入到稀H2SO4中,有气泡产生
D.最后得到的溶液中可能含有Fe3+
30. A、B、C、D、E、F六种强电解质,它们在水中电离出的离子如右表所示,其中A、D、F电离产生的阳离子均为K+。另有甲、乙、丙三种固体,它们分别是铁粉、铜粉和Cu(OH)2固体中的某一种,它们与A、B、C、D、E在常温下有如下转化关系:
A、B、C、D、E、F六种强电解质,它们在水中电离出的离子如右表所示,其中A、D、F电离产生的阳离子均为K+。另有甲、乙、丙三种固体,它们分别是铁粉、铜粉和Cu(OH)2固体中的某一种,它们与A、B、C、D、E在常温下有如下转化关系:
①固体乙+B溶液→E溶液+氢气
②固体甲+B溶液→C溶液+水
③A溶液+C溶液→固体甲+D溶液
请回答下列问题:
(1)写出下列物质的化学式:甲 ,乙 ,F 。
(2)写出下列反应的离子方程式:
反应① ;
反应③ 。
(3)用题目所涉及到的物质表示丙→C的化学方程式____________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com