
题目列表(包括答案和解析)
6.一定能在下列溶液中大量共存的离子组是 ( )
A.pH=0的溶液:Fe2+、Mg2+、NO3-,SO42-
B.由水电离出的c(H+)=1×10-13‑mol/L的溶液:HCO3-、K+、SO42-、Cl-
C.含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl-
D.pH=14的溶液:Na+、K+、AlO2-、CO32-
5.下列关于生活中化学叙述不正确的是 ( )
A.废弃的塑料、金属、纸制品及玻璃都是可回收再利用的资源
B.用灼烧并闻气味的方法可以区分纯棉织物和纯毛织物
C.SO2、NO2或CO2都会导致酸雨的形成
D.食用植物油的主要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
27.(14分)
(1)H2SO4………………………………………………………………………………(2分)
①S(s)+O2(g) SO2(g);△H=-297kJ/mol(有“点燃”条件给分)………(3分)
②D………………………………………………………………………………………(2分)
|
|
②SO2+2CO S+2CO2……………………………………………………………(3分)
|
(2)2Al+Fe2O3 AlO2O3+2Fe………………………………………………………(2分)
(3)2H2O+O2+4e- 4OH-…………………………………………………………(2分)
(4)Al-3e- Al3+……………………………………………………………………(2分)
铝表面易被氧化,生成一层致密而坚固的氧化物薄膜,阻止金属继续氧化,使金属具有抗腐蚀性能。…………………………………………………………………………(3分)
(5)27.2………………………………………………………………………………(3分)
理科综合能力试题
26.(17分)
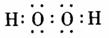 (1)KClO3……………………………………………………………………………(2分)
(1)KClO3……………………………………………………………………………(2分)
…………………………………………………………(2分)
(2)①关闭分液漏斗活塞,在II中加水,没过长导管口,用酒精灯微热圆底烧瓶,若II中有气泡冒出,停止加热后,有水进入II中的长导管,形成一段水柱,则证明I气密性良好。
|
②MnO2+4H++2Cl- Mn2++Cl2↑+2H2O…………………………………………(2分)
③S2-+Cl2=S↓+2 Cl-……………………………………………………………………(2分)
④II III…………………………………………………………………………………(2分)
除去氯气中的水蒸气(或干燥氯气)…………………………………………………(2分)
(3)Cl2+H2O2 2HCl+O2………………………………………………………………(2分)
25.(15分)(1)HOOC-COOH………………………………………………………(2分)
羧基、羟基…………………………………………………………………………(2分)
 (2)①③④…………………………………………………………………………(2分)
(2)①③④…………………………………………………………………………(2分)
(3)HOCH2-CH2OH+O2 OHC-CHO+2H2O…………………………(2分)

 OH
OH
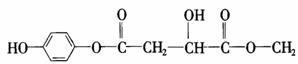 (4)HOOC-CH2-CH-COOH
HOOC-CH=CH-COOH+H2O……(3分)
(4)HOOC-CH2-CH-COOH
HOOC-CH=CH-COOH+H2O……(3分)
(5) -CH2-Br…………………(2分)
(6)2……………………………………………………………………………………(2分)
10.A 11.A 12.C
5.B 6.D 7.D 8.C 9.B
28.(14分)镁、铝、铁是重要的金属,在工业生产中用途广泛。
(1)镁与稀硫酸反应的离子方程式为 ;
(2)铝与氧化铁发生铝热反应的化学方程式为 ;
(3)在潮湿的空气里,钢铁表面有一层水膜,很容易发生电化学腐蚀。其中正极的电极反应为 ;
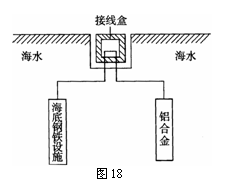 (4)在海洋工程上,通常用铝合金(Al-Zn-Cd)
(4)在海洋工程上,通常用铝合金(Al-Zn-Cd)
保护海底钢铁设施,其原理如图18所示:
其中负极发生的电极反应为
;
在实际应用中,用铝合金而不选用纯铝。
纯铝不能很好地起到保护作用,其原因是
。
(5)将11.9g Mg-Al-Fe组成的合金溶于足量
NaOH溶液中,合金质量减少2.7g。另取等质量的合金溶于过量的稀硝酸中,生成6.72L(标准状况)NO,向反应后的溶液中加入适量的NaOH溶液恰好使Mg2+、Al3+、Fe3+完全转化为沉淀,则沉淀的质量为 g
27.(14分)X、Y、Z为原子序数由小到大排列的三种短周期元素。已知:X、Y的气态氢化物分子具有相同的电数;Y与Z同主族;XY2是非极性分子,其晶体可用作人工降雨。
请回答:
(1)Z的最高价氧化物对应水化物W是重要的化工原料。W的化学式为 ;
工业制造W的生产过程主要分为三个阶段。
①D 101kPa时,3.2g Z的固体单质完全燃烧可放出29.7kJ的热量,写出能够表示该固体单质燃烧热的热化学方程式 ;
②在接触氧化阶段,为提高ZY2的转化率,从理论上判断,应选择的条件是低温和高压。从下表给出不同温度、压强下ZY2平衡转化率的实验数据进行分析,结合工业生产的实际,应选择适合的温度和压强是(选填字母) ;
A.400℃~500℃ 10 MPa B.400℃~500℃ 1 MPa
C.500℃~500℃ 10 MPa D.400℃~500℃ 0.1 MPa
 压强/MPa 压强/MPa转化率/% 温度/℃ |
0.1 |
0.5 |
1 |
10 |
|
400 |
99.2 |
99.6 |
99.7 |
99.9 |
|
500 |
93.5 |
96.9 |
97.8 |
99.3 |
|
600 |
73.7 |
85.8 |
89.5 |
96.4 |
③在吸收阶段,为尽可能提高ZY3的吸收效率,工业上选择的吸收剂是(选填字母)
。
A.水 B.0.5mol/L的硫酸 C.98.3%的硫酸 D.浓氨水
(2)已知X与XY都是工业上常用的还原剂。
①写出X单质与W的浓溶液反应的化学方程式 ;
②500℃,11.2 L(标准状况)ZY2在催化剂作用下与XY发生化学反应。若有2×6.02×1023个电子转移时,该反应的化学方程式是 。
12.在一定温度下,向容积固定不变的密闭容器中充入a mol NO2,发生如下反应:
 2NO2(g) N2O4(g);△H<0。达平衡后再向容器中充入amol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
2NO2(g) N2O4(g);△H<0。达平衡后再向容器中充入amol NO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是 ( )
A.相对平均分子质量增大 B.NO2的转化率提高
C.NO2的质量分数增大 D.反应放出的总热量大于原来的2倍
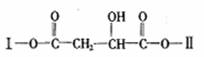 25.(15分)某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为
25.(15分)某有机物X(C12H13O6Br)分子中含有多种官能团,其结构简式为
(其中I、II为未知部分的结构)
为推测X的分子结构,进行如图15的转化:
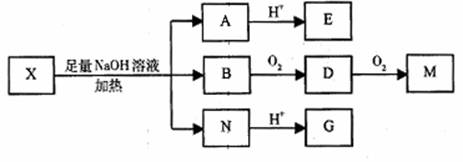
已知向E的水溶液中滴入FeCl3溶液发生显色反应;M(C2H2O4)能使蓝墨水褪色;G、M都能与NaHCO3溶液反应。
请回答:
(1)M的结构简式为 ;G分子所含官能团的名称是 ;
(2)E可以发生的反应有(选填序号) ;
①加成反应 ②消去反应 ③氧化反应 ④取代反应
(3)由B转化成D的化学方程式是 ;
(4)G在一定条件下发生反应生成分子组成为C4H4O4的有机物(该有机物可使溴的四氯化碳溶液褪色),写出G发生此反应的化学方程式
;
(5)已知在X分子结构中,I里含有能与FeCl3溶液发生显色反应的官能团,且E分子中苯环上的一氯代物只有一种,则X的结构简式是
;
(6)F与G互为同分异构体,F的分子中只含有羧基、羟基和醛基三种官能团,且同一个碳原子上不能同时连有两个羟基。则F的分子结构有 种。
 26.(17分)已知A、B、D、E四种物质中均含有同一种短周期元素,D为气体单质,E为黑色粉末,在图16转化中E均起催化作用(某些产物已略去)。
26.(17分)已知A、B、D、E四种物质中均含有同一种短周期元素,D为气体单质,E为黑色粉末,在图16转化中E均起催化作用(某些产物已略去)。
请回答:
(1)A的化学式为 ;B分子的电子式为 。
(2)已知E与含A中某种元素的酸在一定条件下反应,产生一种含有该元素的气体X。某校化学兴趣小组为研究该气体的性质,设计下图所示装置进行实验。装置III中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
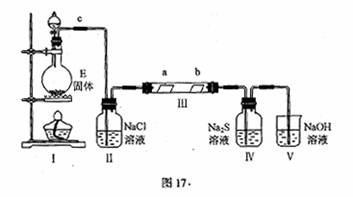
①装入药品前,检查I中气体发生装置气密性的操作是
;
②写出装置I中发生反应的离子方程式 ;
③实验过程中,观察到装置IV中出现淡黄色沉淀,其主要反应的离子方程式为
;
④实验结束后,该组同学在装置III中观察一b的红色褪去,但是并未观察到“a无明显
变化”这一预期现象。为了达到这一实验目的,你认为在装置(选填装置序号)
之间,还需添加洗气瓶,该装置的作用是 ;
(3)气体X能与溶液B反应,生成气体D,写出反应的化学方程式
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com