
题目列表(包括答案和解析)
4.将50%的硫酸溶液和10%的硫酸溶液等体积混合,已知混合前后溶液的密度均大于1g/cm3,则混合溶液中溶质的质量分数为( )
A.大于50% B.小于50% C.等于50% D.无法判断
3.t℃时,将一定量A(不含结晶水)的不饱和溶液均分为三份,分别加热蒸发,然后冷却至t℃,已知三份溶液分别蒸发水的质量为10g、20g、30g,析出晶体质量依次为a g 、b g、 c g,则a、b、c三者的关系为( )
A.c=a+b B.c=2b-a C. c=a+2b D.c=2a-b
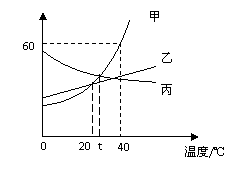
2.甲、乙、丙三种物质(均不含结晶水)的溶解度曲线如右图所示。下列说法不正确的是( )
A.40℃时,100g水中最多溶解甲60g
B.t℃时,甲与丙的溶解度相等
C.分别将40℃时,甲、丙的饱和溶液降温至t℃,所得两溶液中溶质的质量分数相等
D.甲中混有少量乙,可用降温结晶法分离提纯甲
1.
 先用特殊方法把固体物质加工成纳米级(1nm-100nm,1nm=10-9m)的超细粉末粒子,然后再制成纳米材料是制造纳米材料的一种工艺。下列分散系中的分散质的微粒直径比纳米材料中超细粉末粒子还要小的是( )
先用特殊方法把固体物质加工成纳米级(1nm-100nm,1nm=10-9m)的超细粉末粒子,然后再制成纳米材料是制造纳米材料的一种工艺。下列分散系中的分散质的微粒直径比纳米材料中超细粉末粒子还要小的是( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
8.把10 mL密度为1.68 g/cm3的液态S2Cl2 溶于石油醚(一种溶剂)中配制成100 mL溶液,把该溶液慢慢加入50 mL3.2mol/L的SO2水溶液中,振荡使之充分反应,当加入的S2Cl2溶液为64.3 mL时,好反应完全。生成物用含0.32 mol KOH的KOH溶液中和后,恰好完全转化为KCl和一种二元含氧酸的钾盐晶体。试通过计算确定S2Cl2与SO2在溶液中反应的化学方程式。
7.Na2O2是中学化学实验室常备的一种物质,关于在盛有Na2O2的试管中通入CO2和H2O的混合气体时可能发生的反应,某同学写下了以下化学方程式:
①2Na2O2+2H2O=4NaOH+O2↑ ②2Na2O2+2CO2=2Na2CO3+O2↑
③Na2CO3+CO2+H2O=2NaHCO3 ④NaHCO3+NaOH=Na2CO3+H2O
⑤2NaOH(过量)+CO2=Na2CO3+H2O
(1)反应①的还原剂是__________,当反应①中转移1 mol电子时可生成O2 _____g
 (2)当将CO2和H2O的混合气体通入Na2O2时,发生反应的顺序是_______(填序号);当反应后固体中有Na2O2与NaOH共存时一定不能发生的反应是_____(填序号);当反应后固体中有Na2CO3时,________(填“一定”或“可能”,下同)有NaOH;当反应后固体有NaOH时,_________有Na2O2,________有Na2CO3。
(2)当将CO2和H2O的混合气体通入Na2O2时,发生反应的顺序是_______(填序号);当反应后固体中有Na2O2与NaOH共存时一定不能发生的反应是_____(填序号);当反应后固体中有Na2CO3时,________(填“一定”或“可能”,下同)有NaOH;当反应后固体有NaOH时,_________有Na2O2,________有Na2CO3。
(3)当CO和O2以1∶1的体积比和足量Na2O2放在固定容积的密闭容器中用电火花引燃,完全反应后气体压强是反应前的___倍。
6.自然界中存在一种尖晶石,主要成分的化学式可表示为MgAl2O4 ,可作为宝石。已知尖晶石中混有Fe2O3。取一定量样品54 g,恰好完全溶解在一定浓度100 mL盐酸溶液中,则盐酸的浓度可能为( )
A.2.2 mol·L-1 B.2.8 mol·L-1 C.4.3 mol·L-1 D.4.9 mol·L-1
5.单质X都能从盐的溶液中置换出单质Y,由此可知( )
A.当X、Y都是金属时,X一定比Y活泼
B.当X、Y都是非金属时,Y一定比X活泼
C.当X是金属时,Y可能是金属,也可能是非金属
D.当X是非金属时,Y可能是金属,也可能是非金属
4.广义的水解观认为,无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两新组合成新的物质。根据上述观点,下列说法中,不正确的是( )
A.CaO2的水解产物是Ca(OH)2和H2O2 B.NaClO的水解产物之一是HClO
C.PCl3 的水解产物是PH3和HClO D.Mg3N2水解生成NH3和Mg(OH)2
3.下列关于盐的反应规律的说法中,不正确的是(........................................ )
①盐和酸反应一定生成另一种盐和另一种酸;②盐和碱反应一定生成另一种盐和另一种碱;③两种盐反应一定生成另外两种盐;④阳离子相同的两种盐一定不能发生反应。
A.只有② B.只有③ C.只有①④ D.①②③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com