
题目列表(包括答案和解析)
2.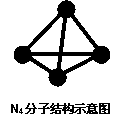 意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1mol N-N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量。
意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1mol N-N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量。
A.N4属于一种新型的化合物
B.N4与N2互为同素异形体
C.N4沸点比P4(白磷)高
D.1 mol N4 气体转变为N2吸收882kJ热量
1.已知25℃ 101 kPa时:H2( g)+1/2O2(g)=H2O(g);△H=-241.8 kJ·mol-1。则下列说法或表达正确的是( )
A.H2的燃烧热为241.8 kJ·mol-1
B.H2(g)+1/2O2(g)=H2O(l);△H<-241.8 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(g);△H>-241.8 kJ·mol-1
D.1 mol H2与1/2mol O2的总能量小于1molH2O(g)的总能量
6.化合物A[KxFe(C2O4)y·zH2O]是一种重要的光化学试剂。化学兴趣小组的同学为测定A的化学式,按下列实验步骤进行探究:
a、取样品溶于水,向其中滴加KSCN试液,溶液呈血红色;
b、准确称取A样品0.491g,在110℃恒温箱中干燥脱水至恒重,残留物质量为0.437g;
c、另取0.491gA置于锥形瓶中,加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,微热且加入0.050mol/L的KMnO4溶液24.0 mL,恰好反应完全;
d、将b所得固体溶于水,加入还要性铁粉至0.028g时,恰好反应完全。
已知:①A中铁元素只呈一种价态;
②2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O。
试填写下列空白:
(1)0.491gA中含结晶水的物质的量为_________。
(2)A的组成中n(Fe)∶n(C2O4) = ________________(注:离子的电荷未标出)。
(3)A的化学式为______________。
5.计算以下两小题,除必须应用所有给出的数据外,还有各缺少一个数据,指出该数据的名称(分别以a和b表示),并列出计算式。
(1)在温度为t℃和压强为p Pa的情况下,19.5g A与11.0 gB恰好完全反应生成固体C和3.00L的D气体,计算生成的C的质量m。
缺少的数据是:_______________;计算式为m=______________。
(2)0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积V(H2)。
 缺少的数据是: _________ 计算式为V(H2)=_________________。
缺少的数据是: _________ 计算式为V(H2)=_________________。
4.下表为4种常见溶液中溶质的质量分数和物质的量浓度:

溶 质 HCl NaOH CH3COOH HNO3
溶质的质量分数/% 36.5 40 60 63
物质的量浓度/mol·L-1 11.8 14.3 10.6 13.8
这4种溶液中密度最小的是( )
A.HCl B.NaOH C.CH3COOH D.HNO3
3.常温下,在密闭容器里分别充入两种气体各0.1 mol,在一定条件下充分反应后,恢复到原温度时,压强降低为开始的1/4,则混合气体可能是( )
A.H2 和O2 B.HCl和NH3 C.H2和Cl2 D.CO和O2
2.只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
|
|
A |
B |
C |
D |
|
甲 |
物质中的 粒子数 |
标准状况下 的气体摩尔 体积 |
固体的体积 |
溶液中溶质 的物质的量 浓度 |
|
乙 |
阿伏加德 罗常数 |
标准状况下 的气体体积 |
固体的密度 |
溶液体积 |
1.14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是( )
①1 mol 14CH4分子中所含中子数为8NA
②14 g 14C原子形成的石墨中所含C-C键的个数为1.5 NA
③17g甲基(-14CH3)所含电子数为8NA
④常温常压下,22.4L14CO2 的分子数为NA
A.①② B.①③ C.①②③ D.③④
6.将标准状况下的aL HCl(气)溶于1000g水中得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为( )
A.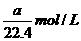 B.
B.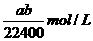
C. D.
D.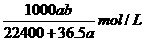
5.将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )
A.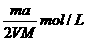 B.
B.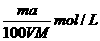 C.
C.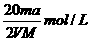 D.
D.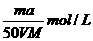
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com