
题目列表(包括答案和解析)
25. (15分)
(1)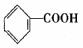 ……………………………………………(2分)
……………………………………………(2分)
(2)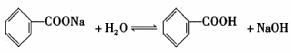 ………………………(2分)
………………………(2分)
(3)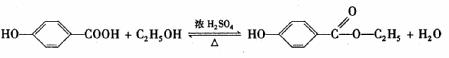
……………………………………………(3分)
(4)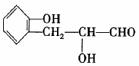 ……………………………………………(2分)
……………………………………………(2分)
(5)
……………………………………………(3分)
(6)酯化反应(1分);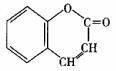 ……………………………………(2分)
……………………………………(2分)
11. B 12. B
5. C 6. D 7. A 8. C 9. D 10. D
28. (18分)氨是一种重要的基础化工原料,可以生产硝酸等一系列化工产品。德国人哈伯在1905年发明的合成氨反应原理为:
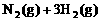
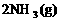 ;
;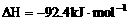
回答下列问题:
(1)将10mol 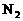 和30mol
和30mol 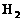 装入密闭容器中,在一定条件下反应达到平衡,若有15%的
装入密闭容器中,在一定条件下反应达到平衡,若有15%的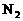 转化,则反应放出的热量是_______________kJ。
转化,则反应放出的热量是_______________kJ。
(2)工业合成氨生产中采取的措施是____________(填序号)
A. 采用较低压强
B. 采用700K左右的高温
C. 用铁触媒作催化剂
D. 将氨液化及时从混合物中分离,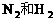 循环到合成塔中,并补充
循环到合成塔中,并补充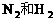
(3)用下图所示装置(夹持固定装置已略去)在实验室中模拟工业制
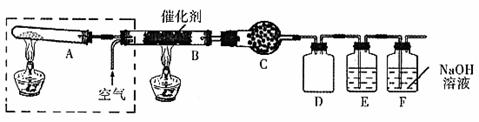
回答下列问题:
①实验时,A装置中盛放的试剂是__________________________;
装置B中反应的化学方程式为_______________________________________;
②C装置中盛放的试剂是_______________________________________;
该物质的主要作用是_______________________________________;
D装置的作用是_______________________________________;
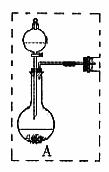
③若将上图所示装置中虚线部分换成下图所示装置进行实验。反应开始前,分液漏斗中盛放的药品是______________________;烧瓶中盛放的药品是_____________________。
27. (14分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据各物质之间的转化关系回答下列问题:
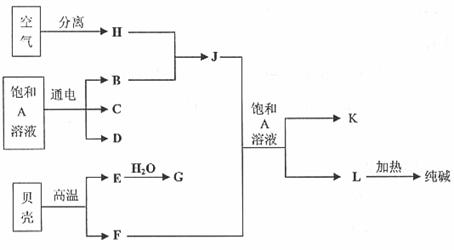
(1)C和D、C和G反应都可以制取消毒剂。C和G反应制取的消毒剂中有效成分的化学式为______________________。
(2)电解A溶液反应的离子方程式为_______________________________
(3)将F和J通入A的饱和溶液中,反应的化学方程式为:
_____________________________________________________________________
(4)图中所示工业制法获得的纯碱中常含有NaCl杂质,用下述方法可以测定样品中NaCl的质量分数。
样品m克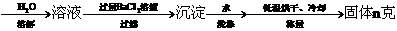
①检验沉淀是否洗涤干净的方法是___________________________________________
______________________________________________________________________________
②样品中NaCl的质量分数的数学表达式为__________________________
26. (13分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,它们的原子序数之和为26;在同周期中W的原子半径最大,W与Z可形成W2Z和W2Z2;X、Y、Z三种元素中的任意两种之间可以组成甲、乙、丙……等许多种化合物。
(1)这四种元素的符号分别是X_______、Y_______、Z_______、W________
用电子式表示W2Z形成过程_______________________________________
(2)甲是一种气体,通入紫色石蕊试液中,溶液变红。甲的分子式为_____________
写出甲与W2Z2反应的化学方程式__________________________
(3)乙是一种植物生长调节剂,乙在一定条件下与O2反应生成一种可与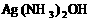 溶液反应的物质,写出乙与
溶液反应的物质,写出乙与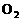 反应的化学方程式________________________________________
反应的化学方程式________________________________________
(4)丙是X和Z按原子个数比1:1组成的化合物。已知丙的溶液能使酸性高锰酸钾溶液褪色。将含有0.5mol丙的溶液滴加到100mL 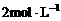 酸性高锰酸钾溶液中,溶液紫色恰好褪色。该反应的离子方程式为
酸性高锰酸钾溶液中,溶液紫色恰好褪色。该反应的离子方程式为
_________________________________________________________________
25. (15分)随着人民生活水平的提高,食品安全问题倍受社会关注。苯甲酸( )是一种比较安全的食品防腐剂。
)是一种比较安全的食品防腐剂。
(1)苯甲酸的结构简式为:_____________
(2)由于苯甲酸在常温下微溶于水,通常食品中加入苯甲酸钠。已知苯甲酸钠水溶液pH>7,原因是(用化学方程式表示)
__________________________________________________________________________
(3)尼泊金酯是一种比苯甲酸更安全的食品防腐剂。在浓硫酸加热条件下,对羟基苯甲酸和乙醇混合反应生成尼泊金酯。该反应的化学方程式是
__________________________________________________________________________
(4)A是尼泊金酯的一种同分异构体。已知:
①A能与新制的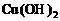 浊液反应(加热),产生红色沉淀,生成有机物B;
浊液反应(加热),产生红色沉淀,生成有机物B;
②1mol A最多能与1mol NaOH反应;
③A分子的苯环上有两个相邻的取代基,且由碳原子构成的侧链无支链。
A的结构简式是:__________________________
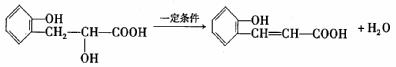
(5)有机物B在一定条件下能发生消去反应生成桂皮酸,化学方程式为:
_________________________________________________________________
(6)桂皮酸在一定条件下可生成香豆素(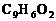 )。
)。
该反应的类型是_______________________________________
香豆素的结构简式为:_______________________________________
12. 原子序数依次相差1,且由小到大排列的A、B、C、D、E五种短周期元素。下列是有关这五种元素的叙述:
①若A的最高价氧化物的水化物是强碱,则E的最高价氧化物的水化物是强酸
②若A的单质既能与强酸又能与强碱反应且都放出氢气,则这五种元素在同一周期
③若A的阳离子比E的阴离子少8个电子,则D一定是非金属元素
④若D的最高价氧化物的水化物是强酸,则E的单质在常温下为气态
⑤若B的单质是原子晶体,则B的氧化物是分子晶体
其中正确的是( )
A. ①②③ B. ②③④ C. ③④⑤ D. ②④⑤
11. 下列有关叙述正确的是( )
A. 1L  的醋酸中有
的醋酸中有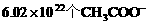
B. 1mol葡萄糖分子中含有
C. 电解1L饱和食盐水,当pH=10时,反应中有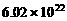 个电子转移
个电子转移
D. 一定条件下将2mol 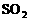 和1mol
和1mol 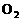 混合充分反应,有
混合充分反应,有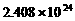 个电子转移
个电子转移
10. 已知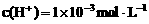 的一元酸HX溶液和
的一元酸HX溶液和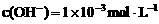 的一元碱YOH溶液混合后溶液呈中性,下列判断正确的是( )
的一元碱YOH溶液混合后溶液呈中性,下列判断正确的是( )
A. 若HX是弱酸,YOH是强碱,则两溶液浓度相等
B. 若HX是强酸,YOH是弱碱,则两溶液体积相等
C. 若HX是弱酸,YOH是强碱,则两溶液体积一定是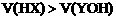
D. 在混合后的中性溶液中,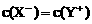
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com