
题目列表(包括答案和解析)
11.能正确表示下列反应的离子方程式是( )
A.醋酸钠的水解反应 CH3COO-+H3O+=CH3COOH + H2O
B.碳酸氢钙与过量的NaOH溶液反应 Ca2++2HCO3-+2OH-=CaCO3↓+ 2H2O+ CO32-
C.苯酚钠溶液与二氧化碳反应 C6H5O-+ CO2+ H2O=C6H5OH+CO32-
D.稀硝酸与过量的铁屑反应 3Fe+8H++2NO3-=3Fe3++2NO↑+ 4H2O
10.下列叙述中正确的是( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
9.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
A.羰基硫属于非极性分子 B.羰基硫的电子式为: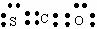
C.羰基硫沸点比CO2低 D.羰基硫分子中三个原子不可能处在同一直线上
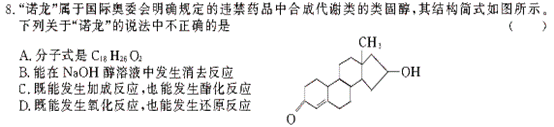
7.2008年北京奥运会主体育场--“鸟巢”,被《泰晤士报》评为全球“最强悍”工程。“鸟巢”运用了高强度、高性能的钒氮合金高新钢和884块ETFE膜,并采用新一代的氮化镓、氮化铟这些高亮度LED材料。有关说法正确的是( )
A.合金的熔点通常比组分金属高,硬度比组分金属小
B.已知Ga处于IIIA族,可推知氮化镓化学式为Ga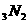
C.用金属铝与V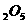 冶炼钒,铝作氧化剂
冶炼钒,铝作氧化剂
D.ETFE膜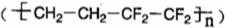 是由两种单体加聚而成的
是由两种单体加聚而成的
6.下列做法中用到物质氧化性的是( )
A.明矾净化水 B.纯碱除去油污 C.臭氧消毒餐具 D.食醋清洗水垢
30.(15分)下图所示为常见气体的制备、除杂、性质验证和尾气处理等实验的仪器装置(加热设备及夹持固定装置均略去)。请根据要求完成下列各题(实验装置可从图中选用)。

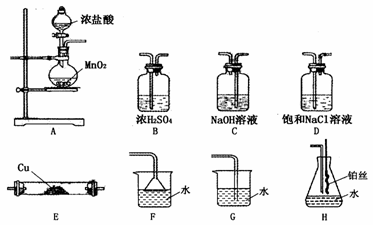
(1)实验室预制取纯净、干燥的Cl2,并验证其和铜的反应,所选装置的顺序依次为(从左向右)__________;需要加热的仪器有_____________,硬质玻璃管E内的现象为_____________________________________。
(2)制取无水MgCl2必须在氯化氢气流中进行。若选择装置A、E和尾气处理装置,实现由MgCl2·6H2O晶体制取无水MgCl2,应将烧瓶中的MnO2试剂改为___________,将E管中的试剂改为MgCl2·6H2O晶体,加热E玻璃管。制取无水MgCl2必须在氯化氢气流中进行的原因是___________________________;尾气处理装置可选用__________________________________________。
(3)若选择装置A和H在实验室模拟氨气的催化氧化实验,应将分液漏斗中的浓盐酸改为浓氨水,圆底烧瓶中的试剂改为_____________,用H装置吸收一段时间氨气后再通入空气,同时将红热的铂丝(催化剂)插入H装置的锥形瓶内,锥形瓶中可观察到的现象是________________________________;可能发生的反应用化学方程式表示为_________________________________________________。
28. I.用仪器A、B和胶管组成装置收集NO气体(①仪器A已经气密性检查;②除水外不能选用其他试剂)。
I.用仪器A、B和胶管组成装置收集NO气体(①仪器A已经气密性检查;②除水外不能选用其他试剂)。
(1)正确的操作步骤是:
II.测定硫酸铜晶体(CuSO4·5H2O)里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量。
请回答下列问题:
(2)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是 。
(3)该实验中哪一步骤需要使用干燥器?使用干燥器的目的是什么?
答: 。
(4)实验步骤⑥的目的是 。
(5)若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有(填入选项的编号): 。
A.被测样品中含有加热不挥发的杂质 B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水 D.加热前所用的坩埚未完全干燥
|
程式为:
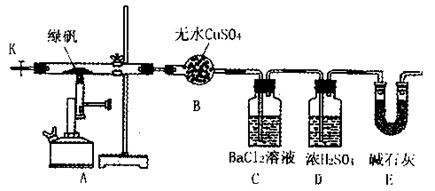 2FeSO4·7H2O====Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验
2FeSO4·7H2O====Fe2O3+SO3↑SO3↑+14H2O↑,就设计了如下实验
装置来验证绿矾受热分解是否发生上述反应。主要实验步骤如下:

①组装仪器并检查装置的气密性;
②称量绿矾样口及U型干燥管E的质量,将称量后的绿矾置于硬质玻璃管内;
③关闭活塞K,加强热使绿矾完全分解;
④打开活塞K,缓缓鼓入一定量的氮气;
⑤再次称量干燥管E的质量;
⑥重复④⑤的操作,直到干燥管E的质量基本不变为止;
⑦称量洗气瓶C中所得沉淀的质量。
试回答:
(1)洗气瓶D中浓H2SO4的作用为: ;
(2)步骤⑦从溶液中获取生成沉淀质量的具体操作为: ;
(3)实验小组的报告如下,请补充完整:
|
|
实验记录 |
分析或计算结果 |
|
现象 |
硬质管内绿色变为红棕色; |
生成物有 |
|
干燥管B中晶体白色变蓝色。 |
生成物有H2O |
|
|
数据 |
称取绿矾样品16.68g; |
反应的绿矾0.06mol |
|
干燥管E最后增重2.24g; |
生成SO2 mol |
|
|
C中生成白色沉淀的质量为4.66g; |
生成DO3
0.02mol |
(4)该实验所得到的数据与所样到的化学方程式中的定量关系不相符合,请分析可能的原因
。
(5)为达到“验证绿矾受热分解是否发生上述反应”的目的,该实验的设计有多处不妥,请提出改进建议(两条即可)
。
27.(16分)某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验室按以下步骤进行:
①称量a g样品,置于烧杯中;
②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;
③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,加热使反应完全;
④趁热迅速加入过量氨水,充分搅拌,使沉淀完全;
⑤过滤,洗涤沉淀;
⑥将沉淀转移到坩埚内,加热、搅拌,直到固体全部由红褐色变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……
请根据上面叙述,回答:
(1)下图所示仪器中,本实验步骤①②③中必须用到的仪器是E和 (填字母)。
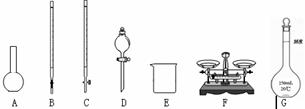
(2)写出步骤③中发生反应的离子方程式 。
(3)洗涤是洗去附着在沉淀上的 (写离子符号),洗涤沉淀的操作是 。
 (4)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1g;再次加热并冷却室温称量其质量为m2g,且m1-m2=0.3,接下来的操作应当是
(4)第⑥步的操作中,将沉淀物加热,冷却至室温,称量其质量为m1g;再次加热并冷却室温称量其质量为m2g,且m1-m2=0.3,接下来的操作应当是
。
(5)若坩埚质量是W1,坩埚与加热后固体总质量是W2,则样品中铁元素的质量分数为 (列出算式,不需化简)。
(6)该兴趣小组中甲学生认为:实验步骤③中不加入氯水,其余步骤不变,仍可达到实验目的。你认为甲学生的观点是否正确? (填“正确”或“错误”),请说明理由: 。
13.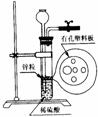 右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使该反应顺利进行,则可以从长颈漏斗中加入的试剂是( )
①食盐水;②KNO3溶液;③适量稀硫酸铜溶液;④Na2CO3溶液;⑤CCl4 ;⑥浓氨水
A.①③⑤ B.①②⑥
C.①②⑤ D.①②④
选择题答题表:
12.为达到预期的实验目的,下列操作正确的是( )
A.欲配制质量分数为10%的ZnS04溶液,将10gZnS04·7H20溶解在90g水中
B.欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸
C.为鉴别KCl、AlCl3和MgCl2溶液,取三种溶液分别滴加NaOH溶液至过量
 D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
D.为减小中和滴定误差,锥形瓶必须洗净并烘干后才能使用
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com