
题目列表(包括答案和解析)
4. 设NA表示阿伏加德罗常数的值,下列叙述中一定正确的是( )
A.常温常压下乙烯和丁烯混合气7克,其中C-H键的数目约为NA
B.1mol FeCl3制成胶体,所得胶体的粒子数为NA
C.0.5mol/L Ba(NO3)2溶液中,NO3-的数目为NA
D.标准状况下,22.4L庚烷中含碳原子数为7NA
3. 下列实验操作或事故处理中,不正确的做法是( )
A. 银镜反应实验后附有银的试管,可用稀HNO3清洗
B. 称量时左盘放被称量物,右盘放砝码。
C. 在250ml烧杯中,加入216ml水和24克NaOH固体,配制100/0NaOH溶液
D. 不慎将浓硫酸粘在皮肤上,立即用干抹布拭去,再用大量水冲洗
2. 一同学欲从量筒中取出部分液体,他先俯视凹液面的最低处,读数为50mL,倒出液体后,他又仰视凹液面的最低处,读数为10mL他实际倒出液体的体积为( )
A.40mL B.大于40mL C.小于40mL D.不一定
1. “生态马路”是运用光触媒技术,即在马路上铺设“光触媒”(如二氧化钛)物质,将空气中的氮氧化物、一氧化碳、二氧化硫等污染物在催化剂表面转化、分解成对人体、环境基本无害的物质。下列有关说法不正确的是( )
A. “生态马路”可将汽车尾气中的CO在催化剂表面氧化生成CO2
B. “生态马路”可将汽车尾气中的NOx在催化剂表面氧化生成N2
C. “生态马路”对道路表面的清洁有较高要求
D. “生态马路”是解决城市空气污染的途径之一
20.(6分)向1LAlCl3 和FeCl3的混合溶液中加入含a mol NaOH的溶液时,产生的沉淀可达到最大值;继续加入NaOH的溶液,沉淀开始溶解,当前后加入的NaOH的物质的量达到b mol时,沉淀量不再变化。求原溶液中Fe3+的物质的量浓度。
2009-2010学年度第一学期高中教学质量监测(一)
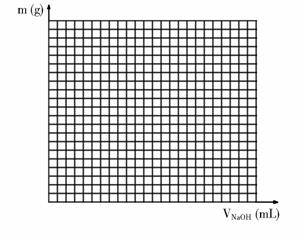
19.(10分)将一定量镁铝合金完全溶于100mL某浓度盐酸中,测得混合液里c(Mg2+)= 2 mol·L-1、c(Al3+)=1mol·L-1、c(Cl-)= 8 mol·L-1,往此混合液加入浓度为5 mol·L-1的NaOH溶液至过量,估算后请在右图画出加入NaOH溶液体积与产生沉淀质量的关系图示。
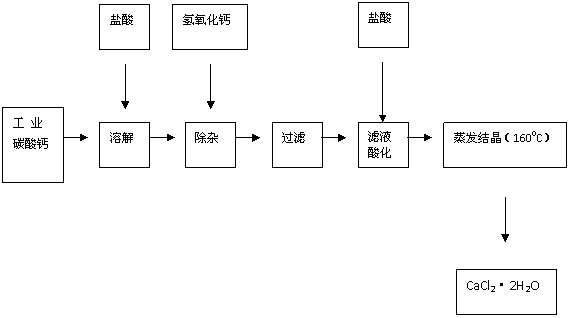
18.(16分)医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~99.9%)的主要流程如下:
(1) 除杂操作是加入氢氧化钙,调节溶液的pH为8.0 - 8.5,以除去溶液中的少量Al3+、
Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
。
(2) 酸化操作是加入盐酸,调节溶液的pH约为4.0,其目的有:将溶液中的少量Ca(OH)2转化为CaCl2;防止溶液吸收空气中的CO2; 。
测定样品中Cl-含量的方法是:
a、取0.75 g样品,溶解,移液(含洗涤液),在250 mL容量瓶中定容、摇匀;
b、取25.00 mL上述待测溶液于锥形瓶中;
c、用0.05 mol·L-1 AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.00 mL。
① 溶解,移液都用到的玻璃仪器除烧杯外还有 。
② 定容的操作是
③ 上述测定过程中需用溶液润洗的仪器有 。
④ 计算上述样品中CaCl2·2H2O的质量分数为 。
⑤ 若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有 ; 。
17.(14分)某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),按要求回答问题。
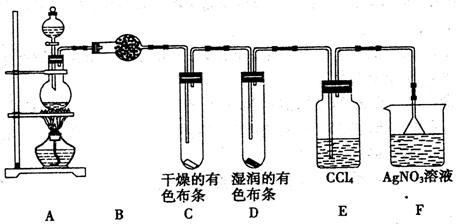
(1)实验室制取氯气的化学方程式是
(2) ①装置B中装入的是无水硫酸铜粉末,其作用是
②装置C和D出现的不同现象说明
③装置F的作用是
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),该装置中应放入 (填试剂或其它物质)。
16.(9分)分类是化学研究中常用的方法。
(1)下列分类方法中,正确的是
A.依据酸分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等
B.依据有否电子转移,将化学反应分为氧化还原反应和非氧化还原反应
C.依据能量的变化,将化学反应分为放热反应和吸热反应
D.依据组成元素的种类,将纯净物分为单质和化合物
(2)Na2CO3、FeSO4、Cu(NO3)2、ZnCl2四种物质中有一种物质的类别与其它三种不同,你选择的是 ,你的根据是 。
15.下列反应的离子方程式书写正确的是 ( )
A.次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
B.澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO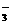 =CaCO3↓+H2O
=CaCO3↓+H2O
C.将1mol Cl2通入含有1mol FeI2 的溶液中:2I-+Cl2=2Cl-+I2
D.氯化铝溶液加入过量氨水:Al3++4NH3·H2O=AlO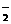 +4NH
+4NH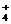 +2H2O
+2H2O
第 Ⅱ 卷(共55分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com