
题目列表(包括答案和解析)
20.(12分)以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出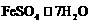 。
。
Ⅱ.将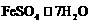 配制成溶液。
配制成溶液。
Ⅲ. 溶液与稍过量的
溶液与稍过量的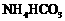 溶液混合,得到含
溶液混合,得到含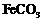 的浊液,同时有CO2气体
的浊液,同时有CO2气体
放出。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到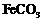 固体。
固体。
Ⅴ.煅烧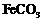 ,得到
,得到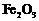 固体。
固体。
已知: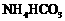 在热水中分解。
在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的 ,该反应的离子方程式是 。
,该反应的离子方程式是 。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用 。
(3)Ⅲ中,生成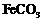 的离子方程式是 。若
的离子方程式是 。若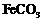 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
(4)Ⅳ中,通过检验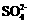 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验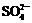 的操作是 。
的操作是 。
(5)已知锻炼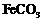 的化学方程式是
的化学方程式是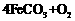

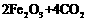 。现锻炼464.0kg
。现锻炼464.0kg
的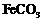 ,得到316.8kg产品。若产品中杂质只有
,得到316.8kg产品。若产品中杂质只有 ,则该产品中
,则该产品中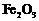 的质量是
的质量是
kg。
19. (6分)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料:
(6分)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料: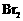 的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
的沸点为59℃,微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图:
请你参与分析讨论:
(1)图中仪器B的名称: 。
(2)整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因为 。
(3)实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
(4)C中液体产物颜色为 ______ ,为除去该产物中仍残留的少量Cl2,可向其中加入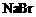 溶液,充分反应后,再进行的分离操作是 。
溶液,充分反应后,再进行的分离操作是 。
18.(4分)完成下列离子方程式(给出物质的计量数不能改变)
(1)1 +6H+ ═ 2Fe3+ + 3
(2)1 + 1Ca2+ + 2 ═ 1 CaCO3↓ + 1
17.(6分)高温下,向1mol 赤热的硫化亚铜中通入足量的水蒸气,生成2mol 氢气,同时还生成金属铜和一种刺激性气味的气体。
(1)该反应的化学方程式是________________________________________________。
(2)该反应中氧化产物是_______________。
(3)每生成1 mol H2氧化剂与还原剂之间转移的电子是______________mol。
16.在密闭容器中充入CO2和CO的混合气体,其密度是相同条件下氦气密度的8倍,这时测得容器内的压强为P1。若控制容器的体积不变,加入足量的Na2O2,充分振荡并不断用电火花点燃至反应完全,恢复到开始时的温度,再次测得容器内的压强为P2。则和P1和P2之间的关系是( )
A.P1=8P2 B.P1=4P2 C.P1=2P2 D.P1=P2
第Ⅱ卷(非选择题,共60分)
15.对反应: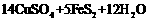 ═
═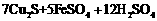 ,下列说法正确的是( )
,下列说法正确的是( )
A.只有硫酸铜作氧化剂
B.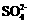 既不是氧化产物又不是还原产物
既不是氧化产物又不是还原产物
C.被氧化的硫和被还原的硫的质量比为3∶7
D.1 mol硫酸铜可以氧化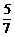 mol的硫
mol的硫
14.含有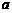 mol
mol  的溶液中,通入
的溶液中,通入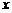 mol
mol 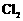 。下列各项为通
。下列各项为通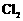 过程中,溶液内发生反应的离子方程式,其中不正确的是( )
过程中,溶液内发生反应的离子方程式,其中不正确的是( )
A.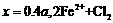 ═
═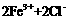
B.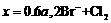 ═
═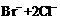
C.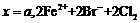 ═
═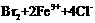
D.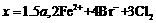 ═
═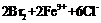
13.将3.72g由金属钠、氧化钠和过氧化钠组成的混合物与足量水反应,在标准状况下得到672mL混合气体。将该混合气体用电火花点燃,恰好完全反应,则原混合物中钠、氧化钠过氧化钠的物质的量之比为( )
A.3∶2∶1 B.4∶2∶1 C.1∶1∶1 D.2∶1∶1
12.将4mol金属Al全部转化为Al(OH)3,共计消耗HCl a mol,NaOH b mol,则a+b的最小值为 ( )
( )
A.4mol B.6mol C.8mol D.16mol
11.下列关于热化学反应的描述中正确的是( )
A.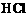 和
和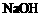 反应的中和热
反应的中和热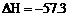 kJ·mol-1,则
kJ·mol-1,则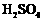 和
和 反应的中和热
反应的中和热
△H=2×(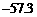 )kJ·mol-1
)kJ·mol-1
B. 的燃烧热是283.0 kJ·mol-1,则
的燃烧热是283.0 kJ·mol-1,则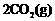 ═
═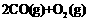 反应的
反应的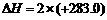 kJ·mol-1
kJ·mol-1
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com