
题目列表(包括答案和解析)
18、某学生鉴定甲盐的发如图所示:

下列结论正确的是( )
A.甲中一定有Fe3+ B.丙中一定有Fe3+
C.乙为AgI沉淀 D.甲一定为FeBr2溶液
17.将a L NH3通过灼热的装有铁触媒的硬质玻璃管后,气体体积变为b L(气体体积均在同温同压下测定),该b L气体中N2的体积分数是 ( )
A.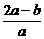 B.
B.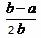 C.
C.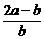 D.
D.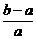
16、已知SO32-+I2+H2O=SO42-+2I-+2H+。某溶液中可能含有I-、NH4+、Cu2+、SO32-,向该无色溶液中加入少量溴水,溶液仍呈无色。则下列关于该溶液组成的判断正确的是( )
A.肯定不含I- B.肯定不含Cu2+ C.可能含有SO32- D.肯定不含有NH4+
15、a、b、c、d、e分别为MgCl2、KHSO4、KOH、NaHCO3、AlCl3五种溶液中的一种,其中a能与其余四种溶液反应,且b、d反应时无明显现象;b与d反应只产生气泡;e只能与a反应。下列推理不正确的是( )
A.a一定为KOH溶液 B.b一定为KHSO4溶液
C.c一定为AlCl3溶液 D.e一定为MgCl2溶液
14. 可用下图装置制取(必要时可加热)、净化、收集的气体是
( )
可用下图装置制取(必要时可加热)、净化、收集的气体是
( )
A. 亚硫酸钠与70%硫酸制二氧化硫B. 铜和稀硝酸制一氧化氮
C.锌和稀硫酸制氢气 D.硫化亚铁与稀硫酸制硫化氢
13、能正确表示下列反应的离子方程式是
A.氨水中通入过量CO2:2NH3·H2O + CO2 = 2NH4+ + CO32- + H2O
B.氯化亚铁溶液中加入硝酸:Fe2+ + 4H+ + NO3- = Fe3+ + 2H2O + NO↑
C.将标准状况下112 mL氯气通入10 mL 1 mol·L-1的溴化亚铁溶液中:
2Fe2+ + 4Br-+ 3Cl2 = 2Fe3+ + 6Cl- + 2Br2
D.用小苏打治疗胃酸过多:HCO-3+H+ = CO2↑+H2O
12、常温下,下列溶液可能大量共存的离子组是
A.含有大量S2-的溶液:Na+、C1O-、C1-、CO32-
B.含有大量Fe3+的溶液:K+、Na+、A1O2-、SO42-
C.能使pH试纸变红的溶液:NH4+、Na+、NO3-、HCO3-
D.水电离产生的c(H+)=1×10-12mol·L-1的溶液:Mg2+、SO42-、NO3-、C1-
11、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色水处理剂。工业上是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。
湿法制备的主要反应方程为:2Fe(OH)3+3ClO―+4OH―=2FeO42-+3Cl―+5H2O
干法制备的主要反应方程为:2FeSO4+4Na2O2=2Na2FeO4 +2Na2SO4
下列有关说法不正确的是( )
A.高铁酸钾中铁显+3价
B.湿法中每生成1mol Na2FeO4转移3 mol电子
C.干法中每生成1mol Na2FeO4转移4 mol电子
D.K2FeO4处理水时,不仅能消毒杀菌,还能吸附水中的悬浮杂质
10、将a%的某物质的水溶液加热蒸发掉m g水(溶质不挥发、且蒸发过程无溶质析出),所得溶液体积为V L,溶质的质量分数为蒸发前的2倍,设溶质的相对分子质量为M,则蒸发后所得溶液的物质的量浓度为( )
A.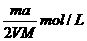 B.
B.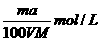 C.
C.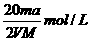 D.
D.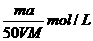
9、下列实验操作会导致实验结果偏低的是 ( )
①配制100 g 10%的CuSO4溶液,称取10 g CuSO4晶体溶于90 g水中
②测定碳酸钠晶体中结晶水的百分含量时,所用的晶体已经受潮
③配制一定物质的量浓度的溶液时,药品与砝码放反了,游码读数为0.2 g,所得溶液的浓度
④用酸式滴定管量取用98%,密度为1.84 g/cm3的浓H2SO4配制200mL 2 mol·L-1的稀H2SO4时,先平视后仰视
A.只有① B.只有② C.②③④ D.①③④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com