
题目列表(包括答案和解析)
13.下列实验操作或药品的保存方法错误的是
A.用水或溴水鉴别苯、乙醇、四氯化碳www.
B.硫酸铜晶体中结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.汽油或NaOH溶液保存在带橡皮塞的玻璃瓶中
D.锂保存在液体石蜡里,硝酸银溶液保存在棕色试剂瓶里
12.早在1807年化学家戴维用电解熔融氢氧化钠制得钠4NaOH(熔)  4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
4Na + O2↑+ 2H2O;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠,反应原理为:
3Fe+4NaOH Fe3O44+2H2↑十4Na↑。
Fe3O44+2H2↑十4Na↑。
下列有关说法正确的是
A.电解熔融氢氧化钠制钠,阳极发生电极反应为:
2OH--2e-=H2↑+O2↑
B.盖·吕萨克法制钠原理是利用铁的还原性比钠强
C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数也相同
D.目前工业上常用电解熔融氯化钠法制钠,电解槽中石墨极为阳极,铁为阴极
11.一些烷烃的燃烧热如下表:
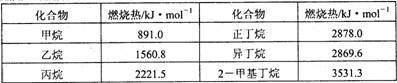
下列表达正确的是
A.乙烷燃烧的热化学方程式为: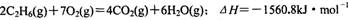
B.正丁烷转化为异丁烷的反应为吸热反应
C.正戊烷的燃烧热大约在3540 kJ·mol-1左右
D.相同质量的烷烃,碳的质量分数越大,燃烧放出的热量越多
10. 下列有关工业生产的叙述正确的是
A.硫酸工业中,三个设备分别是:沸腾炉、接触室、合成塔
B.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热
C.电解饱和食盐水制烧碱采用离子交换膜,可防止阴极室产生的Cl2进入阳极室
D.电解精练铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
9.下列反应的离子方程式书写正确的是
A.过氧化钠固体与水反应:2O22-+2H2O=4OH-+O2↑
B.氨水中通入过量二氧化硫:2NH3•H2O + SO2 = 2NH4+ +SO32- +H2O
C.澄清的石灰水中加人过量的NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
D.将2mol/LAlCl3溶液和7mol/LNaOH溶液等体积混合:
2Al3++7OH-=Al(OH)3↓+AlO2-+2H2O
8.铜的冶炼大致可分为:
⑴ 富集:将硫化物矿进行浮选;
⑵ 焙烧:主要反应为:2CuFeS2+4O2==Cu2S+3SO2+2FeO(炉渣);
⑶ 制粗铜:在1200℃发生的主要反应为:
2Cu2S+3O2 ==2Cu2O+2SO2;2Cu2O+ Cu2S==6 Cu+SO2↑;
⑷ 电解精炼铜。
下列说法正确的是
A.上述灼烧过程的尾气均可直接排入空气中
B.由6mol CuFeS2生成6molCu,共消耗15molO2
C.在反应2Cu2O+ Cu2S==6 Cu+SO2↑中,作氧化剂的只有Cu2O
D.上述所有反应均应在过量O2环境中进行
7.下列关于胶体的叙述正确的是
A.向煮沸的NaOH溶液中滴加FeCl3溶液可制备Fe(OH) 3胶体
B.利用丁达尔现象区别NaCl溶液和K2SO4溶液
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来
6.下列叙述不正确的是
A.构成分子晶体的微粒中一定含有共价键
B.熔沸点:SiO2>NaCl>H2O>H2S
C.离子晶体中不一定只含有离子键
D.同主族元素形成的氧化物的晶体类型可能相同
5.下列各组离子在指定条件下,一定能大量共存的是
A.能使红色石蕊试纸显蓝色的溶液:K+、Fe2+、SO42-、NO3-、Cl-
B.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、Br-
C.水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、NO3-、Cl-
D.加入铝条有氢气放出的溶液:Na+、NH4+、HCO3-、NO3-
4.泰雅紫是古代地中海沿岸出产的一种贵重染料,罗马帝王用法律规定,只有皇族与教主可穿这种紫色衣袍。当时人们是从小的紫蜗牛中提取它的,制备1.5g泰雅紫需要多达12000只紫蜗牛,现知其结构如右图所示,下列说法不正确的是
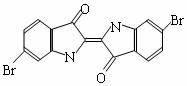 A.泰雅紫分子的分子式为:C16H8N2Br2O2
A.泰雅紫分子的分子式为:C16H8N2Br2O2
B.泰雅紫属于芳香烃
C.1 mol泰雅紫最多可与9 mol H2 加成
D.检验泰雅紫中溴元素不能用直接加入硝酸银溶液,
看是否有浅黄色沉淀
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com