
题目列表(包括答案和解析)
30. 以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略);
I 从废液中提纯并结晶出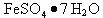 。
。
II将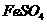 溶液与稍过量的
溶液与稍过量的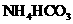 溶液混合,得到含
溶液混合,得到含 的浊液
的浊液
IV 将浊液过滤,用90。C热水洗涤沉淀,干燥后得到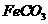 固体
固体
V煅烧 ,得到
,得到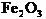 固体
固体
已知: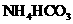 在热水中分解
在热水中分解
(1)
I中,加足量的铁屑除去废液中的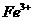 ,该反应的离子方程式是
,该反应的离子方程式是
(2)
II中,生成 的离子方程式是
。若
的离子方程式是
。若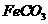 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是
。
(3)
IV中,通过检验 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验 操作是
操作是
(4)
已知煅烧 的化学方程式是
的化学方程式是 ,现煅烧464.0kg的
,现煅烧464.0kg的 ,得到316.8kg产品,若产品中杂质只有
,得到316.8kg产品,若产品中杂质只有 ,则该产品中Fe2O3的质量是
kg(摩尔质量/g·
,则该产品中Fe2O3的质量是
kg(摩尔质量/g·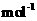 :
: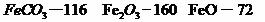 )
)
29. 已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1-2滴液溴,振荡后溶液呈黄色。
 (1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:______ (填粒子的化学式,下同);
(1)甲同学认为这不是发生化学反应所致,则使溶液呈黄色的微粒是:______ (填粒子的化学式,下同);
 乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是_________。
乙同学认为这是发生化学反应所致,则使溶液呈黄色的微粒是_________。
 (2)如果要验证乙同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
(2)如果要验证乙同学判断的正确性,请根据下面所提供的可用试剂,用两种方法加以验证,请将选用的试剂代号及实验中观察到的现象填入下表。
实验可供选用试剂: A.酸性高锰酸钾溶液 B.氢氧化钠溶液 C.四氯化碳 D.硫氰化钾溶液 E.硝酸银溶液 F.碘化钾淀粉溶液
|
实验方案 |
所选用试剂(填代号) |
实验现象 |
|
方案一 |
|
|
|
方案二 |
|
|
(3)根据上述实验推测,若在稀溴化亚铁溶液中通入氯气,则首先被氧化的离子是 ,相应的离子方程式为 ;
28. 有一种由CO、CO2、H2、水蒸气四种气体组成的混合气体,要证明其中含有CO和 H2,可选用的仪器及药品如下:
有一种由CO、CO2、H2、水蒸气四种气体组成的混合气体,要证明其中含有CO和 H2,可选用的仪器及药品如下:
 (1)实验时,导管接口的顺序是
。
(1)实验时,导管接口的顺序是
。
 (2)装置①内发生反应的化学方程式是
(任写一个,并标出电子转移方向和数目)。
(2)装置①内发生反应的化学方程式是
(任写一个,并标出电子转移方向和数目)。

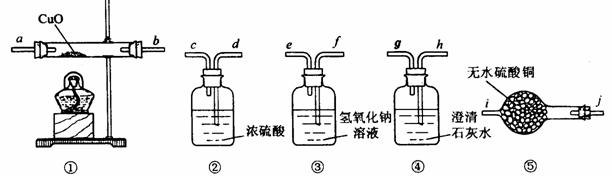 (3)证明混合气体中含有氢气的实验现象是
。(4)证明混合气体中含有CO的实验现象是 。
(3)证明混合气体中含有氢气的实验现象是
。(4)证明混合气体中含有CO的实验现象是 。
27. KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作是:
KMnO4溶液常用做氧化还原反应滴定的标准液,由于KMnO4的强氧化性,它的溶液很容易被空气中或水中某些少量还原性物质还原,生成难溶性物质MnO(OH)2,因此配制KMnO4标准溶液的操作是:
 I. 称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸1 h;
I. 称取稍多于所需量的KMnO4固体溶于水,将溶液加热并保持微沸1 h;
 II. 用微孔玻璃漏斗(无需滤纸)过滤除去难溶的MnO(OH)2;
II. 用微孔玻璃漏斗(无需滤纸)过滤除去难溶的MnO(OH)2;
 III. 过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处;
III. 过滤得到的KMnO4溶液贮存于棕色试剂瓶放在暗处;
 IV. 利用氧化还原滴定方法,在700C-800C条件下用基准试剂(纯度高、相对分子质量较大、稳定性较好的物质,如草酸晶体H2C2O4•2H2O )溶液标定其浓度。已知: MnO4- (H+)→Mn2+ 、 H2C2O4 → CO2 反应中其他元素没有得、失电子。请回答下列问题:
IV. 利用氧化还原滴定方法,在700C-800C条件下用基准试剂(纯度高、相对分子质量较大、稳定性较好的物质,如草酸晶体H2C2O4•2H2O )溶液标定其浓度。已知: MnO4- (H+)→Mn2+ 、 H2C2O4 → CO2 反应中其他元素没有得、失电子。请回答下列问题:
 (1)写出在硫酸酸化的条件下KMnO4 与H2C2O4反应的离子方程式是
;
(1)写出在硫酸酸化的条件下KMnO4 与H2C2O4反应的离子方程式是
;
 (2)如何保证在700C-800C条件下进行滴定操作: ;
(2)如何保证在700C-800C条件下进行滴定操作: ;
 (3)准确量取一定体积(25.00 mL)的KMnO4溶液使用的仪器是
;
(3)准确量取一定体积(25.00 mL)的KMnO4溶液使用的仪器是
;
 (4)若准确称取W g基准试剂溶于水配成500
mL水溶液,取25.00
mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液V mL。问:
(4)若准确称取W g基准试剂溶于水配成500
mL水溶液,取25.00
mL置于锥形瓶中,用高锰酸钾溶液滴定至终点,消耗高锰酸钾溶液V mL。问:
 ①滴定终点标志是
;
①滴定终点标志是
;
 ②KMnO4溶液的物质的量浓度为
mol·L-1;
②KMnO4溶液的物质的量浓度为
mol·L-1;
 (5)若用放置两周的KMnO4标准溶液去滴定水样中Fe2+含量,测得的浓度值将
-------(填“偏高”或“偏低”)
(5)若用放置两周的KMnO4标准溶液去滴定水样中Fe2+含量,测得的浓度值将
-------(填“偏高”或“偏低”)
26. 下列实验操作中,正确的是
下列实验操作中,正确的是
 ①称量固体药品时,将药品直接放在天平托盘上。
①称量固体药品时,将药品直接放在天平托盘上。
 ②实验室用氯酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯
②实验室用氯酸钾制氧气结束时,先从水槽中移出导气管,再熄灭酒精灯
 ③先将pH试纸用蒸馏水润湿后,再测定溶液的pH
③先将pH试纸用蒸馏水润湿后,再测定溶液的pH
 ④在量筒中稀释浓硫酸
④在量筒中稀释浓硫酸
 ⑤金属钠保存在CCl4中
⑤金属钠保存在CCl4中
 ⑥金属钠不慎燃烧立即用沙子覆盖
⑥金属钠不慎燃烧立即用沙子覆盖
 ⑦用100mL量筒量取2.50mL盐酸
⑦用100mL量筒量取2.50mL盐酸
25. 对下列仪器回答问题:
对下列仪器回答问题:
 ①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗⑧玻璃棒
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗⑧玻璃棒
 (1)使用时必须检查是否漏水的有 (填序号)
(1)使用时必须检查是否漏水的有 (填序号)
 (2) 某学生要提纯混有泥沙的食盐,他设计的主要操作有:溶解、过滤、蒸发。在这些操作中都需要使用的仪器是 (填序号)
(2) 某学生要提纯混有泥沙的食盐,他设计的主要操作有:溶解、过滤、蒸发。在这些操作中都需要使用的仪器是 (填序号)
24. 若NA为阿伏加德罗常数,下列说法中正确的是
若NA为阿伏加德罗常数,下列说法中正确的是
 A.常温常压下,11.2LN2和NO的混合气体所含的原子数为NA
A.常温常压下,11.2LN2和NO的混合气体所含的原子数为NA
 B.1 mol C8H18分子中,共价键总数为25NA
B.1 mol C8H18分子中,共价键总数为25NA
 C.在1mol/L碳酸钠溶液中CO32-
、HCO3-、离子总数为NA
C.在1mol/L碳酸钠溶液中CO32-
、HCO3-、离子总数为NA
 D.含0.1 mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数为0.2NA
D.含0.1 mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数为0.2NA
 非选择题
非选择题
23. 下列离子方程式书写正确的是( )
下列离子方程式书写正确的是( )
 A.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:
A.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:
 Ca2++2HCO3-+2OH-=CaCO3+2H2O+CO32-
Ca2++2HCO3-+2OH-=CaCO3+2H2O+CO32-
 B.向NaAlO2溶液中加盐酸至溶液呈酸性:A1O2-+4H+=Al3++2H2O
B.向NaAlO2溶液中加盐酸至溶液呈酸性:A1O2-+4H+=Al3++2H2O
 C.向碳酸氢铵溶液中加入过量的NaOH溶液:HCO3-+OH-=CO32-+H2O
C.向碳酸氢铵溶液中加入过量的NaOH溶液:HCO3-+OH-=CO32-+H2O
 D.Cl2与H2O反应:Cl2+H2O=2H++Cl-+C1O-
D.Cl2与H2O反应:Cl2+H2O=2H++Cl-+C1O-
22. 20℃时碳酸钠、碳酸氢钠的溶解度分别为:21.2g 、9.6g 。现有20℃时的碳酸钠饱和溶液60.6g,向其中通入二氧化碳气体,刚好完全反应。设反应前、后溶液温度不发生变化,溶液密度均近似为1g/cm3,则反应后所得溶液的物质的量浓度约为:
( )
20℃时碳酸钠、碳酸氢钠的溶解度分别为:21.2g 、9.6g 。现有20℃时的碳酸钠饱和溶液60.6g,向其中通入二氧化碳气体,刚好完全反应。设反应前、后溶液温度不发生变化,溶液密度均近似为1g/cm3,则反应后所得溶液的物质的量浓度约为:
( )
 A.3mol/L
B.4mol/L
C.1mol/L
D.无法计算
A.3mol/L
B.4mol/L
C.1mol/L
D.无法计算
21. 含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
 A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
 B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
 C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
 D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com