

题目列表(包括答案和解析)
31. (10分)以石墨做电极电解200mL 0.5mol/L的CuSO4溶液,在标准状况下,阴极上
(10分)以石墨做电极电解200mL 0.5mol/L的CuSO4溶液,在标准状况下,阴极上
 收集到2.24L气体时,停止通电。请回答下列问题:
收集到2.24L气体时,停止通电。请回答下列问题:
 (1)整个电解过程中阴极的电极反应式为
;
(1)整个电解过程中阴极的电极反应式为
;
 (2)电解过程中共收集到气体的体积为
;
(2)电解过程中共收集到气体的体积为
;
 (3)若电解前后溶液的体积变化忽略不计,电解后溶液恢复至室温时的pH值约为
;
(3)若电解前后溶液的体积变化忽略不计,电解后溶液恢复至室温时的pH值约为
;
(4)电解结束后,欲使溶液恢复到电解前溶液的组成和浓度,可加入 mol
(填化学式)。
衡阳市八中2010届高三第一次月考
30. (10分) 现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。
(10分) 现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积(约6mL)和检验氯气的氧化性(不应将多余的氯气排入空气中)。


 (1)炭棒接直流电源的________极。
(1)炭棒接直流电源的________极。
 (2)U型管中反应的化学方程式为
。
(2)U型管中反应的化学方程式为
。
 (3)尾气吸收装置中反应的离子方程式为
,若两者恰好完全反应,所得溶液呈碱性,其原因用离子方程式表示为
;取恰好完全反应后的溶液2mL与2mL一定浓度的FeCl3溶液混合,产生红褐色沉淀,反应的离子方程式为 。
(3)尾气吸收装置中反应的离子方程式为
,若两者恰好完全反应,所得溶液呈碱性,其原因用离子方程式表示为
;取恰好完全反应后的溶液2mL与2mL一定浓度的FeCl3溶液混合,产生红褐色沉淀,反应的离子方程式为 。
29. (8分)(1)仅有下列仪器:烧杯、铁架台(带铁圈)、三脚架、分液漏斗、石棉网、酒精灯、玻璃棒、蒸发皿和圆底烧瓶,从缺少仪器角度分析,不能进行的实验项目是
。
(8分)(1)仅有下列仪器:烧杯、铁架台(带铁圈)、三脚架、分液漏斗、石棉网、酒精灯、玻璃棒、蒸发皿和圆底烧瓶,从缺少仪器角度分析,不能进行的实验项目是
。
 A. 过滤 B.
蒸发 C.
萃取 D.
分馏 E、中和滴定
A. 过滤 B.
蒸发 C.
萃取 D.
分馏 E、中和滴定
 (2)用下列仪器的编号回答问题:
(2)用下列仪器的编号回答问题:
 ①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
①容量瓶 ②蒸馏烧瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
 a. 加热时必须垫石棉网的有___________; b. 使用时必须检查是否漏水的有_
;
a. 加热时必须垫石棉网的有___________; b. 使用时必须检查是否漏水的有_
;
 c. 有零刻度且零刻度在上方的是___________。
c. 有零刻度且零刻度在上方的是___________。
27. (8分)如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、
(8分)如图所示,当关闭K时,向A中充入4molX、14molY,向B中充入2molX、

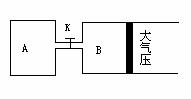 7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)
7molY,起始时V(A)=V(B)=a升,在相同温度和有催化剂存在的条件下,两容器各自发生下列反应:2X(g)+2Y(g)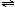 Z(g)+2W(g)
△H<0;达到平衡(Ⅰ)时,B容器体积为原来的0.9倍,试回答:
Z(g)+2W(g)
△H<0;达到平衡(Ⅰ)时,B容器体积为原来的0.9倍,试回答:
 (1)B中X的转化率α(X)为
。
(1)B中X的转化率α(X)为
。
 (2)A中的Z和B中的W的物质的量的关系为:
(2)A中的Z和B中的W的物质的量的关系为:
 n(Z)A n (W)B (填<、>、或=)
n(Z)A n (W)B (填<、>、或=)
 (3)打开K,过一段时间重新达平衡(Ⅱ)时,B容器的体积为 升(用含a的代数式表示,连通管中气体体积忽略不计),在温度不变的情况下,要使B容器恢复原来反应前的体积,可采取的措施是
。
(3)打开K,过一段时间重新达平衡(Ⅱ)时,B容器的体积为 升(用含a的代数式表示,连通管中气体体积忽略不计),在温度不变的情况下,要使B容器恢复原来反应前的体积,可采取的措施是
。

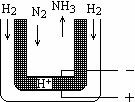 28(8分).在课本里学到的合成氨技术叫哈伯法,近一个世纪,合成氨需要高温高压似乎是天经地义了。然而,最近有两位希腊化学家在《科学》杂志上发表文章说,在常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池(如右图),氢气和氮气便可在电极上合成氨,转化率竟然高达78%。 回答下列问题:
28(8分).在课本里学到的合成氨技术叫哈伯法,近一个世纪,合成氨需要高温高压似乎是天经地义了。然而,最近有两位希腊化学家在《科学》杂志上发表文章说,在常压下把氢气和用氦气稀释的氮气分别通入一个加热到570℃的电解池(如右图),氢气和氮气便可在电极上合成氨,转化率竟然高达78%。 回答下列问题:
 (1)新法合成氨的电解池中能否用水溶液作电解质?_______。
(1)新法合成氨的电解池中能否用水溶液作电解质?_______。
 (2)新法合成氨中所用的电解质(如图中黑细点所示)能传导H+,试写出电极反应式和总反应式。
(2)新法合成氨中所用的电解质(如图中黑细点所示)能传导H+,试写出电极反应式和总反应式。
 阳极:___________; 阴极__________ , 总反应式:_____ ____
阳极:___________; 阴极__________ , 总反应式:_____ ____
26. (6分)(1)将pH=3的醋酸溶液和pH=11的NaOH溶液等体积混合后,溶液呈 性。
(6分)(1)将pH=3的醋酸溶液和pH=11的NaOH溶液等体积混合后,溶液呈 性。
 (2)将0.01mol/L的醋酸溶液和0.01mol/L的NaOH溶液等体积混合后,溶液呈 性。
(2)将0.01mol/L的醋酸溶液和0.01mol/L的NaOH溶液等体积混合后,溶液呈 性。
 (3)若醋酸溶液和NaOH溶液混合后呈中性, 则正确的是 。
(3)若醋酸溶液和NaOH溶液混合后呈中性, 则正确的是 。
 A.溶液中所有离子的浓度关系为c(Na+)= c(CH3COO-)> c(H+)= c(OH-)
A.溶液中所有离子的浓度关系为c(Na+)= c(CH3COO-)> c(H+)= c(OH-)
 B.醋酸溶液的物质的量浓度一定大于NaOH溶液的物质的量浓度
B.醋酸溶液的物质的量浓度一定大于NaOH溶液的物质的量浓度
 C.n(CH3COOH) > n (NaOH)
C.n(CH3COOH) > n (NaOH)
25. 甲酸的下列性质中,可以证明它是弱电解质的是:
甲酸的下列性质中,可以证明它是弱电解质的是:
 A.1mol/L甲酸溶液的pH约为2 B.甲酸能与水以任何比例互溶
A.1mol/L甲酸溶液的pH约为2 B.甲酸能与水以任何比例互溶
 C.10mL 1 moL/L甲酸恰好与10mL 1 mol/LNaOH的溶液完全反应
C.10mL 1 moL/L甲酸恰好与10mL 1 mol/LNaOH的溶液完全反应
 D.在相同条件下,甲酸溶液的导电性与盐酸相同。
D.在相同条件下,甲酸溶液的导电性与盐酸相同。
24. 0.01mol·L-1NaOH 的溶液中的c(H+) 是0.0005mol·L-1Ba(OH)2溶液中c(H+)的:
0.01mol·L-1NaOH 的溶液中的c(H+) 是0.0005mol·L-1Ba(OH)2溶液中c(H+)的:
 A.10倍
B.20倍.
C.
A.10倍
B.20倍.
C.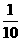 D
D 
23. 下列溶液加热蒸干灼烧后,能得到的溶质固体是
下列溶液加热蒸干灼烧后,能得到的溶质固体是
 A.ALCL3 B. KHCO3
C.Fe2(SO4)3
D.NH4HCO3
A.ALCL3 B. KHCO3
C.Fe2(SO4)3
D.NH4HCO3
22. 把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,则混合液中粒子
把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液以等体积混和,则混合液中粒子
 浓度关系正确的为
浓度关系正确的为
 A.c(CH3COO-)>c(Na+)
B.c(OH-)>c(H+)
A.c(CH3COO-)>c(Na+)
B.c(OH-)>c(H+)
 C.
c(CH3COOH)>c(CH3COO
C.
c(CH3COOH)>c(CH3COO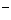 ) D.
c(CH3COOH)+c(CH3COO-)
) D.
c(CH3COOH)+c(CH3COO-)
21. 常温下,下列离子能使纯水中的H+离子数目增加的是
常温下,下列离子能使纯水中的H+离子数目增加的是
 A.S2- B.CO32-
C.NH4+
D.Br-
A.S2- B.CO32-
C.NH4+
D.Br-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com