
题目列表(包括答案和解析)
20.(7分)位于短周期的四种主族元素A.B.C.D原子序数依次增大,已知A.C位于同一主族,A在周期表中原子半径最小。B.D的最外层电子数相等,且B.D的原子序数之和为A.C原子序数之和的两倍。根据你的推断回答下列问题:
(1)写出由上述元素形成的具有漂白作用的四种物质的化学式
, , , 。
(2)C与D形成D的最低价化合物的电子式:______
(3)仅由B.C.D三种元素形成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因:______ 。
19.(6分)可用于分离或提纯物质的方法有:
A.分馏 B.盐析 C.过滤 D.重结晶 E、升华 F、渗析 G、电解
H、加热分解 I、蒸馏 J、灼热氧化。如欲分离或提纯下列各组混合物,请选择上
述方法中最合适者,并将相应字母填入题后空格内:
(1)从石油中分离出汽油和煤油等成分
(2)除去淀粉溶液中的少量碘化钠
(3)从油脂皂化反应后的混合液中分离出高级脂肪酸钠
(4)除去粗铜中锌、银等金属
(5)除去水中的Na+、SO 、Cl-等杂质
、Cl-等杂质
(6)除去KNO3晶体中混有的少量NaCl
18.有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为(还原性I->Fe2+>Br->Cl-)( )
A.7∶1 B.7∶2 C.7∶3 D.7∶4
|
17. 下列各组溶液,不用其他试剂就不能鉴别的是 ( )
下列各组溶液,不用其他试剂就不能鉴别的是 ( )
 A.FeCl3、NaNO3、Na2CO3、NaCl B.NaOH、MgSO4、Na2CO3、NaHSO4
A.FeCl3、NaNO3、Na2CO3、NaCl B.NaOH、MgSO4、Na2CO3、NaHSO4
 C.AgNO3、KNO3、KCl、NaI D.HCl、BaCl2、NaOH、CuSO4
C.AgNO3、KNO3、KCl、NaI D.HCl、BaCl2、NaOH、CuSO4
16. 200C时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法不正确的是 ( )
200C时,饱和KCl溶液的密度为1.174g·cm-3,物质的量浓度为4.0mol·L-1,则下列说法不正确的是 ( )
 A.250C时,饱和KCl溶液的浓度大于4.0 mol·L-1
A.250C时,饱和KCl溶液的浓度大于4.0 mol·L-1
 B.此溶液中KCl的质量分数为
B.此溶液中KCl的质量分数为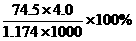
 C.200C时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液
C.200C时,密度小于1.174g·cm-3的KCl溶液是不饱和溶液
 D.将此溶液蒸发部分水,再恢复到200C时,溶液密度一定大于1.174g·cm-3
D.将此溶液蒸发部分水,再恢复到200C时,溶液密度一定大于1.174g·cm-3
15. 下列反应的离子方程式书写正确的是
( )
下列反应的离子方程式书写正确的是
( )
 A.碳酸氢钙溶液中加入过量的NaOH溶液:
A.碳酸氢钙溶液中加入过量的NaOH溶液:
 Ca2++HCO3-+OH-=CaCO3↓+H2O
Ca2++HCO3-+OH-=CaCO3↓+H2O
 B.溶液中NH4HSO3与NaOH等物质的量混合:
B.溶液中NH4HSO3与NaOH等物质的量混合:
 NH4++HSO3-+2OH-=SO32-+NH3·H2O+H2O
NH4++HSO3-+2OH-=SO32-+NH3·H2O+H2O
 C.过量的CO2通入NaAlO2溶液中:
C.过量的CO2通入NaAlO2溶液中:
 CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-
CO2+2H2O+AlO2-=Al(OH)3↓+HCO3-
 D.硫化钠溶于水中:S2-+H2O=HS-+OH-
D.硫化钠溶于水中:S2-+H2O=HS-+OH-
14. 质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
( )
质量分数为a%,物质的量浓度为c mol/L 的KOH溶液,蒸发溶剂,恢复到原来温度,若质量分数变为2a%,则物质的量浓度变为
( )
 A.等于2c mol/L
B.大于2c mol/L
A.等于2c mol/L
B.大于2c mol/L
 C.小于2c mol/L
D.在c mol/L∽2c mol/L之间
C.小于2c mol/L
D.在c mol/L∽2c mol/L之间
13. 下列各项实验操作中,正确的是 ( )
下列各项实验操作中,正确的是 ( )
 A.为使制取H2的速率加快,可向H2SO4中加少量CuSO4溶液
A.为使制取H2的速率加快,可向H2SO4中加少量CuSO4溶液
 B.为加快过滤速度,可用玻璃棒搅拌过滤器中的食盐水
B.为加快过滤速度,可用玻璃棒搅拌过滤器中的食盐水
 C.配制一定物质的量浓度的溶液时,容量瓶用水洗涤后再用所配溶液洗涤
C.配制一定物质的量浓度的溶液时,容量瓶用水洗涤后再用所配溶液洗涤
 D.为除去试管内壁上的“银镜”,可用氨水洗涤
D.为除去试管内壁上的“银镜”,可用氨水洗涤
12. 下列各组离子在相应的条件下可以大量共存的是 ( )
下列各组离子在相应的条件下可以大量共存的是 ( )
 A.在碱性溶液中:CO32-、K+、C1-、Na+
A.在碱性溶液中:CO32-、K+、C1-、Na+
 B.与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+、Na+、SO42-
B.与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+、Na+、SO42-
 C.在c(H+)/c(OH-)==1×1012的溶液中:NH4+、Ca2+、C1-、K+
C.在c(H+)/c(OH-)==1×1012的溶液中:NH4+、Ca2+、C1-、K+
 D.在中性溶液中:Fe3+、S2-、NO3-、A13+
D.在中性溶液中:Fe3+、S2-、NO3-、A13+
11. 设NA代表阿伏加德罗常数,下列说法正确的是 ( )
设NA代表阿伏加德罗常数,下列说法正确的是 ( )
 A.用惰性电极电解500mL饱和食盐水时,若溶液的pH值变为14时,则电极上转移的电子数目为NA
A.用惰性电极电解500mL饱和食盐水时,若溶液的pH值变为14时,则电极上转移的电子数目为NA
 B.在铜与硫的反应中,1mol铜失去的电子数为2 NA
B.在铜与硫的反应中,1mol铜失去的电子数为2 NA
 C.标准状况下,22.4L甲烷和乙炔混合物所含的分子数为NA
C.标准状况下,22.4L甲烷和乙炔混合物所含的分子数为NA
 D.46g 二氧化氮和46g四氧化二氮含有的原子数均为3NA
D.46g 二氧化氮和46g四氧化二氮含有的原子数均为3NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com