
题目列表(包括答案和解析)
25、环保检测中,有害气体的浓度常用1 L有害气体的毫克值(mg/L)来表示,如对某气体样品中所含一氧化碳的浓度进行测定,其方法和实验步骤如下:
①首先将2.00 L的气体样品通过盛有I2O5固体的加热管,反应后生成CO2和I 2;
②用30.0 mL 5.00×10-3mol/L的硫代硫酸钠溶液吸收所产生的碘,发生的反应为:
I2+2S2O32- =2I-+S4O62-
③将②中溶液取出1/5,加入1.00 mL 1.00×10-3mol/L碘水,正好将所取溶液中过量的硫代硫酸钠完全氧化。
(1)写出步骤①中CO通过盛I2O5加热管的有关反应化学方程式。
(2)计算样品中CO的浓度。
广西桂林十八中2010届高三上学期第一次月考
24、(8分) 江苏省东海县矿产丰富,除了水晶制品名扬天下外,蛭石、蛇纹石等矿石储量大,品位高,其相关的耐火、保温隔热材料(主要成分为MgO、Al2O3)工业也较发达。
某中学化学探究小组通过查阅相关资料,对蛭石的组成进行了实验探究。
I、相关资料:①蛭石的成分可看成是由MgO、Fe2O3、Al2O3、SiO2组成
②氢氧化物开始沉淀及沉淀完全时的pH
|
氢氧化物 |
Fe(OH)3 |
Mg(OH)2 |
Al(OH)3 |
|
沉淀的pH范围 |
1.5–4.1 |
9.4–12.4 |
3.3–5.2 |
Ⅱ、相关实验:
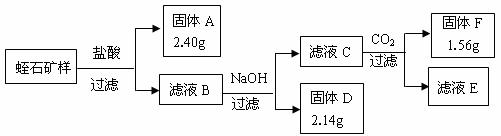
Ⅲ、实验数据:
① 矿石样品质量为:8.22g ② 每次转化所得固体成分只有一种
请你根据以上内容和中学化学知识回答以下问题
(1)写出由D制一种红色颜料的化学方程式:
(2)工业上的耐火材料通常由F及滤液E进一步转化而成,请你分析滤液E中可能含有成分,设计一个从滤液E制取耐火材料的实验方法:
(3)滤液B和NaOH溶液反应时,应控制溶液的pH在7–8之间,这是因为:
(4)通过计算,写出用氧化物的形式表示蛭石组成的化学式
23、(12分)某学生利用以下装置探究氯气和氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气和氨气的反应装置。

请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)
A.碱石灰 B.生石灰 C.二氧化硅 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从上图的备选装置中选择。并将编号填入下列空格。
B__________、D__________、E__________(填编号)
(4)氯气和氨气在常温下相混就会反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体就是氯化铵:
。
22、(6分)(1)现仅有下列仪器:烧杯、铁架台(带铁圈)、三脚架、分液漏斗、石棉网、酒精灯、玻璃棒、蒸发皿和圆底烧瓶,从缺少仪器的角度分析,不能进行的实验项目是__________。
A.过滤 B.蒸发 C.萃取 D.分馏 E.中和滴定
(2)用下列仪器的编号回答问题:
①容量瓶 ②蒸馏瓶 ③滴定管 ④量筒 ⑤烧杯 ⑥蒸发皿 ⑦分液漏斗
a.使用时必须检查是否漏水的有___________;b.标有使用温度的有_______________。
21、(10分)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
 请回答下列问题:
请回答下列问题:
 (1)电池的负极材料为
;
(1)电池的负极材料为
; (2)电池正极发生的电极反应为
;
(2)电池正极发生的电极反应为
;
 (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
 (4)组装该电池必须在无水、无氧的条件下进行,原因是
。
(4)组装该电池必须在无水、无氧的条件下进行,原因是
。
20、(5分)磷在氧气中燃烧,可能生成两种固态氧化物。3.1g的单质磷(P)在3.2g的氧气中燃烧,至反应物耗尽,并放出X KJ热量。
⑴通过计算确定反应产物的组成(用化学式表示)是 。
⑵已知单质磷的燃烧热为Y KJ/mol,则1mol P与O2反应生成固态P2O3的热化学反应方程式:__ _
_ 。
19、(5分)A、B、C三只烧杯中,依次分别盛有NaOH溶液、KSCN溶液、煮沸的蒸馏水,各滴入FeCl3溶液,试根据实验现象分别回答以下问题:⑴分别写出三只烧杯中形成分散系的名称:
A , B ,C 。
⑵写出B中形成分散系的离子方程式 。
⑶写出C中形成分散系的化学方程式 。
18、下列实验中,仪器的下端必须插入液面下的是
①制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备Fe(OH)2操作中的胶头滴管; ④将氨气气体溶于水的导管;
⑤用乙醇制取乙烯时的温度计; ⑥分馏石油时的温度计;
A.①③④⑤ B.①③⑤ C.②④⑥ D.全部
第II卷 (非选择题,共54分)
17、向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A.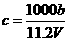 B.
B.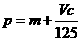 C.n=m+17Vc D.
C.n=m+17Vc D.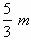 <
< 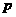 <
<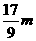
16、镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O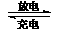 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是
A、充电时阳极反应:Ni(OH)2 -e- + OH- ﹦ NiOOH + H2O
B、充电过程是化学能转化为电能的过程
C、放电时负极附近溶液的碱性不变
D、放电时电解质溶液中的OH-向正极移动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com