
题目列表(包括答案和解析)
3、混合物的分离与提纯
混合物的分离是指用物理化学方法将混合物中各组组分分开,并恢复到原状态,得到比较纯的物质。物质的提纯则只要将杂质除去即可。
(1)常见物质分离提纯的方法
①固-固混合分离型:灼烧、热分解、升华、结晶(或重结晶);
②固-液混合分离型:过滤、盐析、蒸发;
③液-液混合分离型:萃取、分液、蒸馏、渗析;
④气-气混合分离型:洗气。
对多组分的混合物的分离提纯,一般要考虑物理方法和化学方法综合运用。
(2)物质分离提纯的原则
①不能引入新的杂质,即不可“前门驱虎,后门进狼”。
②被提纯物质的量尽量不要减少,即不可“玉石俱焚”。
③实验过程和操作方法简单易行,即被提纯物质与杂质不可“难舍难分”。
典型题点击
2、物质的鉴别
(1)不用任何试剂鉴别多种物质
①先依据外观特征,鉴别出其中的一种或几种,然后再利用它们去鉴别其他的几种物质;
②若均无明显外观特征,可考虑能否用加热或焰色反应区别开来;
③若以上两方法都不能鉴别时,可考虑两两混合法,记录混合后的反应现象,综合分析加以确定;
④若被鉴别物质为两种时,可考虑因试剂加入的顺序不同,现象不同而进行鉴别。
(2)只用一种试剂鉴别多种物质
可根据被鉴别多种物质的水溶性、密度、溶液酸碱性,利用“相反原理”确定试剂进行鉴别。
(3)任选试剂鉴别多种物质
1.物质的检验在中学通常有鉴定、鉴别和推断三类,检验物质包括气体、离子、有机物等。物质的检验需对物质的物理性质、化学性质、实验方法、实验现象、实验基本操作等知识综合运用才能解决,是考查学生实验能力的常见题型。解答物质检验题的方法可归纳为“取试样,加试剂,说操作,由现象,定结论”。
15.已知硫代硫酸钠(Na2S2O3)具有①还原性:
2 Na2S2O3+I2= Na2S4O6+2 NaI;②在酸性条件下能迅速分解:Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O;③BaS2O3难溶于水。市售硫代硫酸钠固体中常含有硫酸钠。
(1)请写出检验市售硫代硫酸钠中含硫酸钠的操作步骤、所用试剂、实验现象和结论。
A.
B.
C.
(2)利用硫代硫酸钠跟I2反应的性质可定量测定市售硫代硫酸钠的纯度。现取Wg硫代硫酸钠固体样品配制成VmL的溶液,加入指示剂,用含I2为amol/L的碘水进行滴定,耗用碘水bmL。回答下列问题:
D.该滴定实验最好是在 (填“强酸性、中性、强碱性”)溶液中进行,理由是
;
E.滴定过程中指示剂应选用 溶液。
F.样品中硫代硫酸钠纯度的表达式是 。
14.亚硝酸钠(NaNO2)可用做水泥施工的抗冻剂,它易溶于水,有咸味,且既有氧化性,又有还原性。在酸性溶液中它能氧化碘离子、亚铁离子,它能将人体血红蛋白里所含的亚铁离子氧化为3价铁离子,使人中毒,亚硝酸钠与酸反应生成亚硝酸,亚硝酸是不稳定的弱酸,它只存在于冷的稀溶液中,易发生如下分解反应:3HNO2=2NO↑+HNO3+H2O。请设计两种简单的实验方案,鉴别亚硝酸钠和氯化钠,可供选用的试剂如下:
a、稀H2SO4 b、稀HNO3 c、纯碱 d、氨水 e、碘化钾淀粉溶液 f、蒸馏水
(1)第一种方案(只用一种试剂)
①选用的试剂___________________________(填序号)
②观察到的现象______________________________;
(2)第二种方案:
①选用的试剂___________________________________
②观察到的现象________________________________。
13.某课外活动小组利用蔗糖溶液、浓氨水、生石灰和硫酸四种药品,设计下列图示的方法从AgN03(含Fe3+和A13+)废液中提取Ag。
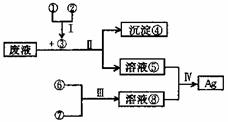 (1)写出下列物质的化学式③ ;④
(1)写出下列物质的化学式③ ;④
。
(2)在I一Ⅳ四步反应中,需要加热的有 。
(3)某同学按照上述方法实验时,最终没有回收到Ag,请你分析其主要原因,并对方法加以改进
。
(4)写出反应的化学方程式:
①+②→③: 。
溶液⑤+溶液⑧→Ag: 。
12.在纯碱溶液中滴入酚酞溶液变红,若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是
其原因是(以离子方程式和简要文字说明):
。
11.某固体混合物可能由KNO3、K2SO4、KI、KCl、NaCl、CuCl2、CaCl2、和Na2CO3中的一种或几种组成。依次进行下列五步实验,观察到的现象记录如下:
(1)混合物加水得无色透明溶液;
(2)向上述溶液中滴加BaCl2溶液,有白色沉淀生成。将该沉淀滤出,并将滤液分成两份;
(3)上述白色沉淀可完全溶于稀盐酸;
(4)将两份滤液中的一份,滴加氯水并加入CCl4,振荡后静置,CCl4层无色;
(5)将另一份滤液中加入AgNO3溶液,有白色沉淀生成。该沉淀不溶于稀硝酸。
根据以上实验,可以判断出混合物中肯定含有 ;但不能判断出是否含有 。
10.要除去(Ⅰ)栏中“甲→己”各物质中所含杂质(括号内为杂质)请从Ⅱ栏中选择所需试剂(不可重复使用),从Ⅲ栏中选择所用的方法或主要仪器,再从Ⅳ栏中选择试剂,检验杂质是否已除净(Ⅲ、Ⅳ可重复使用):

9.化学实验室中常将溶液或试剂进行酸化,下列酸化的处理中正确的是( )
A.定性检验C2H5Cl时,将C2H5Cl和NaOH溶液混合加热后,加H2SO4酸化
B.为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化
C.鉴定待测溶液中是否含有Fe2+时,用硝酸酸化
D.鉴别溶液中是否有SO42-时,在无其他阳离子干扰条件下,所加的BaCl2溶液用盐酸酸化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com