
题目列表(包括答案和解析)
6.短周期元素A、B、C,原子序数依次递增。已知:A、C同主族,而且三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半。下列叙述正确的是
A.原子半径:A<B<C B.沸点:A的氢化物低于C的氢化物
C.B的硫酸盐溶液pH<7 D.5.6 g铁与足量的C化合,转移0.3 mol电子
|
A、B、C、D、E、F六种元素的叙述正确的是
A.常压下六种元素的单质中,F单质的沸点最高
B.晶体E中不存在化学键
C.D元素的非金属性比B元素的非金属性强
D.单质A、C均没有同素异形体
第Ⅱ卷
5.下列说法正确的是
A.某微粒核外电子排布为2,8,8结构,则该微粒一定是氩原子
B.Na+的半径大于F-的半径
C.F-、Na+、Mg2+、Al3+是与He原子具有相同电子层结构的离子
D.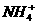 与H3O+具有相同的质子数和电子数
与H3O+具有相同的质子数和电子数
4.某烃有两种或两种以上的同分异构体,其同分异构体中的某一种的一氯代物只有一种,则这种烃可能是
①分子具有7个碳原子的芳香烃 ②分子中具有4个碳原子的烷烃 ③分子中具有12个氢原子的烷烃 ④分子中具有8个碳原子的烷烃
A.①② B.②③ C.③④ D.②④
3.X、Y元素均为主族元素,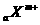 和
和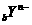 的电子层结构相同,则下列说法中不正确的是
的电子层结构相同,则下列说法中不正确的是
A.Y元素的核电荷数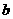 等于
等于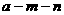
B.Y的原子序数小于X的原子序数
C.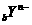 的离子半径小于
的离子半径小于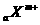 的离子半径
的离子半径
D.若X元素位于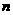 周期,则Y元素位于
周期,则Y元素位于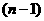 周期
周期
2. 不具有放射性的同位素称之为稳定同位素,近20年来,稳定同位素分析法在植物生理学生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示物。下列说法中正确的是
A.34S原子核内的中子数为16
B.13C和15N原子核内的质子数相差2
C.1H216O在相同条件下比1H218O更易蒸发
D.2H+的酸性比1H+的酸性更强
1. 韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”。下列关于“暖冰”的说法不正确的是
韩国首尔大学科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成了“暖冰”。下列关于“暖冰”的说法不正确的是
A.“暖冰”也是水分子间通过氢键结合而成的固体
B.水凝固形成20℃时的“暖冰”所发生的变化是化学变化
C.形成20℃时的“暖冰”的变化是物理变化
D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”
23.计算以下两小题时,除必须应用所有给出的数据外,还各缺少一个数据,指出该数据的名称(分别以a和b表示),并列出计算式。
⑴在温度为t℃和压强为pPa的情况下,19.5g A 与11.0g B恰好完全反应,生成固体C和3.00L的D气体,计算生成的C的质量(m)。
缺少的数据是:
计算式为m=
⑵0.48g金属镁与10mL盐酸反应,计算生成的H2在标准状况下的体积(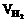 )
)
缺少的数据是:
计算式为:
|
|
A |
B |
C |
D |
E |
F |
G |
|
A |
- |
- |
- |
- |
- |
- |
↓ |
|
B |
- |
- |
- |
- |
↓ |
↓ |
↓ |
|
C |
- |
- |
― |
↓ |
|
↓ |
↓ |
|
D |
- |
|
↓ |
- |
↓ |
↓ |
↓ |
|
E |
- |
↓ |
- |
↓ |
- |
↓ |
- |
|
F |
- |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
|
G |
↓ |
↓ |
↓ |
↓ |
- |
↓ |
- |
22.有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,
“-”表示观察不到明显变化。试回答下面问题。
⑴A的化学式是 ,G的化学式是 。
⑵写出其余几种物质的化学式。B: ,C: ,D: ,E: ,F: 。
21.(6分)在热的稀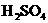 溶液中,溶解了11.4克
溶液中,溶解了11.4克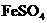 ,当加入50 mL0.5 mol/L
,当加入50 mL0.5 mol/L  溶液后,使其中的
溶液后,使其中的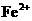 全部转化为
全部转化为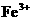 ,
, 也完全反应,并有
也完全反应,并有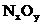 氮氧化物逸出,反应如下:
氮氧化物逸出,反应如下:
( )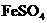 +( )
+( ) +( )
+( )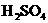
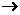
( )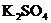 +( )
+( )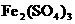 +( )
+( )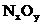 +( )
+( )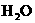
(1)推算出x=____________,y=________.
(2)配平该化学方程式.
20.(9分) 按照下图接通线路,反应一段时间后,回答下列问题(假设所提供的电能可以保证电解反应的顺利进行):
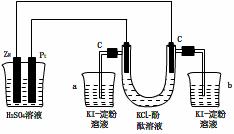
(1)U形管内发生什么现象?
(2)写出有关反应的化学方程式:
(3)在 a、b两烧杯中发生的现象:
(4)如果小烧杯中有0.508g碘析出,大烧杯中负极减轻 g.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com