
题目列表(包括答案和解析)
11、一种甲醇燃料电池的工作原理(如图示)是甲醇在催化剂作用下提供质子(H+)和电子。电子经外电路,质子经内电路到达另一极与氧气反应。电池总反应式:
 2CH3OH+3O2=2CO2+4H2O
2CH3OH+3O2=2CO2+4H2O
下列说法正确的是
A、左边的电极为电池正极 a处通入的是甲醇
B、右边的电极为电池的负极,b处通入的是空气
C、电池负极的反应式为CH3OH+H2O-6e-=CO2↑+6H+
D、电池正极的反应式为O2+2H2O+4e-=4OH-
10、下列所示四种装置中①盛100ml 0.01mol·L-1 CuSO4溶液 ②盛200ml 0.01mol·L-1 H2SO4溶液 ③盛200ml浓ZnCl2溶液 ④盛200ml NaCl饱和溶液
工作一段时间后,测得导线上均通过0.002mol电子,此时溶液的PH由大到小的排列顺序为(不考虑盐的水解和溶液体积的变化)

A、④③②① B、④③①② C、④②③① D、④①③②
9、下列离子方程式书写正确的是
A、明矾溶液中加入过量Ba(OH)2溶液
Ba2++SO42-+Al3++4OH-=BaSO4↓+AlO2-+2H2O
B、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体
Fe3++3H2O Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
C、硫化钠溶液与氯化铝溶液混合 2Al3++3S2-=Al2S3↓
D、碳酸氢钠溶液中加入过量石灰水 HCO3-+Ca2++OH-=CaCO3↓+H2O
8、下列有关晶体结构和性质的说法正确的是
A、晶体硅、金刚石、二氧化硅的晶体类型相同,其晶体立体网状结构中均含有许多六元环
B、石墨晶体中碳原子和碳碳键数之比为2:3,每个碳环平均占有的碳原子数为2
C、NaCl晶体中每个Na+周围最近且等距的Na+有6个
D、HF比HCl稳定是由于HF分子间存在氢键
7、 右图所示晶体结构是一种具有优良电、光功能材料的晶胞。晶体内与每个Ti原子紧邻的氧原子数和这种晶体材料的化学式分别是
右图所示晶体结构是一种具有优良电、光功能材料的晶胞。晶体内与每个Ti原子紧邻的氧原子数和这种晶体材料的化学式分别是
A、3,BaTi8O12 B、6,BaTi4O2
C、6,BaTiO3 D、3, BaTi2O3
6、下列各组热化学方程式中,化学反应的△H前者大于后者的是
(1)C(s)+O2(g)=CO2(g);△H1 C(s)+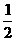 O2(g)=CO(g);△H2
O2(g)=CO(g);△H2
(2)S(s)+O2(g)=SO2(g);△H3 S(g)+O2(g)=SO2(g);△H4
(3)H2(g)+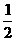 O2(g)=H2O(l);△H5 2H2(g)+O2(g)=2H2O(l);△H6
O2(g)=H2O(l);△H5 2H2(g)+O2(g)=2H2O(l);△H6
(4)CaCO3(s)=CaO(s)+CO2(g);△H7 CaO(s)+H2O(l)=Ca(OH)2(aq);△H8
A、①④ B、②③ C、②③④ D、①②③
5、由水电离产生的H+浓度为1×10-12mol·L-1的溶液中,一定能大量共存的离子组是
①Na+、Cl-、NO3-、S2- ②Fe2+、K+、I-、SO42-
③Na+、NO3-、SO42-、Cl- ④Na+、Cu2+、Cl-、HCO3-
⑤K+、Ba2+、Cl-、NO3-
A、①③ B、③⑤ C、③④ D、②⑤
4、下列做法能达到实验目的的是
A、检验氯乙烷中的氯元素可先将氯乙烷与氢氧化钠溶液共热,再滴入硝酸银溶液,看是否生成白色沉淀
B、蛋白质溶液中混有少量NaCl可用渗析法除去
C、用丁达尔效应可鉴别Fe(OH)3胶体和淀粉溶液
D、用惰性电极电解MgCl2溶液可制得金属镁
3、将0.5mol Cu2S与足量稀HNO3反应生成Cu(NO3)2、S、NO和H2O。下列说法正确的是
A、Cu2S在反应中既是氧化剂又是还原剂
B、反应中转移的电子的物质的量为1.5mol
C、参加反应的硝酸中被还原的HNO3为1mol
D、反应中氧化剂与还原剂的物质的量之比为4:3
2、在硫酸工业的制法中,下列生产操作或说明错误的是
A、从沸腾炉出来的炉气须净化,否则会使催化剂中毒
B、SO3用98.3%的浓H2SO4吸收,目的是防止形成酸雾,提高SO3的吸收效率
C、SO2氧化为SO3时需使用催化剂,这样可提高SO3的产率
D、硫酸厂的选址应首先考虑靠近消费中心,选离人口稠密的地区,兼顾考虑原料产地的远近
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com