
题目列表(包括答案和解析)
21、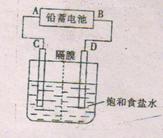 (12分)铅蓄电池是典型的可充电电池,它的正、负极隔板是惰性材料,上面分别覆盖有Pb和PbO2,电池总反应式为: Pb+PbO2+4H++2SO42-
(12分)铅蓄电池是典型的可充电电池,它的正、负极隔板是惰性材料,上面分别覆盖有Pb和PbO2,电池总反应式为: Pb+PbO2+4H++2SO42- 
 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题:
(1)放电时的负极反应式
充电时阳极反应式
(2)用铅蓄电池为电源电解1L饱和食盐水(ρ=1.15g·cm-3),若蓄电池消耗H2SO42mol,则可收集到H2的体积(标准状况下)多少升?(列式计算)
(3)若消耗H2SO4 amol,电解后除去隔膜,所得溶液中NaOH溶液中NaOH的质量分数表达式 (假设Cl2 全部排出)
(4)在完全耗尽PbO2和Pb时,要使电极复原,可对其充电,则原来的Pb极要与电源 极相连。
20、(12分)已知有如下反应
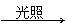 ① CH≡CH+CH2=CH2 |
(环丁烯)
① CH≡CH+CH2=CH2 |
(环丁烯)
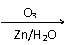
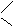
 ② R′ H R′ H
② R′ H R′ H
C=C C=O+O=C
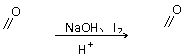 R R″ R R″
R R″ R R″
③ -C-CH3 -C-OH+CHI3

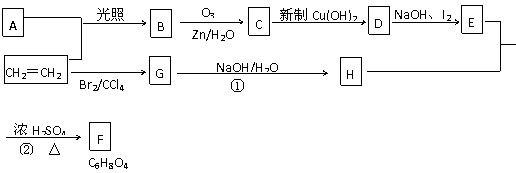
(1)写出A、C、D的结构简式
A C D
(2)写出下列反应方程式
① G→H
② E+H→F
③ 符合下列条件的D的同分异构体共有 种
a 能与金属钠反应生成无色气体
b 能与银氨溶液反应,0.1mol D完全反应可生成43.2gAg
19、(8分)某课外兴趣小组做硫酸铜晶体结晶水含量的测定实验,下面是一次实验数据,完成计算填入表中空格。
|
坩埚质量 |
坩埚与晶体质量 |
加热后坩埚与固体总质量 |
测得晶体中结晶水个数 |
误差(偏高、偏低) |
|
11.7g |
22.7g |
19.1g |
|
|
(1)实验中最少应进行称量操作为 次。
(2)可能造成误差的原因是 (填字母)
A、称量的坩埚不干燥 B、晶体不纯,含有不挥发杂质
C、粉末未完全变白就停止加热 D、加热后在空气中冷却称量
18、 (10分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见补铁药物。该药品不溶于水,但铁溶于人体的胃酸中,某同学为了检测该药片中Fe2+的存在,设计并进行了如下实验:
(10分)铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物。“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见补铁药物。该药品不溶于水,但铁溶于人体的胃酸中,某同学为了检测该药片中Fe2+的存在,设计并进行了如下实验:
.
(1) 试剂1是 ,试剂2是 ,加入新制氯水后,溶液中发生反应的离子方程式是 。
(2)加入试剂2后溶液颜色由淡黄色变为淡红色是因为 ,写出+2价Fe在空气中转变为+3价Fe的离子方程式: 。
(3) 该同学猜想由红色溶液变为无色溶液的原因是溶液中+3价铁还原为+2价铁。若你认为合理,请说明理由(若你认为不合理,该空不作答): 。
若你认为不合理,请设计一个简单实验加以验证: (若你认为合理,该空不作答)
17、(10分)已知X、Y、Z都是短周期元素,它们的原子序数依次增大,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的3倍,Y和Z可形成两种以上气态化合物,则
(1) X是 ,Y是 ,Z是 (填元素符号)
(2) 由Y和Z组成,且Y和Z的质量比为7:20的化合物化学式是 。
(3) 由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子是
和 。
(4) X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子个数比为4:2:3,此盐的化学式是 。
16、检验某未知溶液中是否含有SO42-,下列操作中最合理的是
A、加入硝酸酸化了的硝酸钡溶液 B、先加硝酸酸化,再加硝酸钡溶液
C、先加盐酸酸化,再加氯化钡溶液 D、加入盐酸酸化了的氯化钡溶液
15、某离子晶体结构与食盐晶体相似,已知其密度为ρg·cm-3,摩尔质量为M g·mol-1,阿伏加德罗常数为NA,则在该晶体中阳离子与阴离子的间距是
A、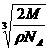 cm B、
cm B、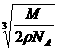 cm C、
cm C、 cm D、
cm D、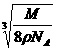 cm
cm
14、工业上用氨制硝酸有三个主要过程,已知氨催化氧化制NO的转化率为a,NO2的吸收率为b,则标况下,10m3氨气可制得质量分数为60%的硝酸质量为
A、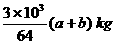 B、
B、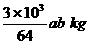
C、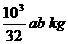 D、
D、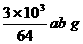
13、强酸与强碱稀溶液发生中和反应的热效应:
H+(aq)+OH-(aq)=H2O(l); △H=-57.3kJ/mol,下列反应的热效应与它相等的是
A、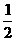 H2SO4(aq)+
H2SO4(aq)+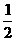 Ba(OH)2(aq)=
Ba(OH)2(aq)=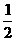 BaSO4(s)+H2O(l)
BaSO4(s)+H2O(l)
B、NaOH(s)+HCl(aq)=NaCl(aq)+H2O(l)
C、CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l)
D、KOH(aq)+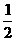 H2SO4(aq)=
H2SO4(aq)=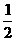 K2SO4(aq)+H2O(l)
K2SO4(aq)+H2O(l)
12、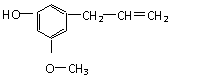 某有机物的结构简式是
某有机物的结构简式是
该物质不应具有的化学性质是
①可以燃烧 ②可以跟溴加成 ③可以使酸性高锰酸钾溶液褪色
④可以跟NaHCO3溶液反应 ⑤可以跟NaOH溶液反应 ⑥可以发生消去反应
A、①③ B、③⑥ C、④⑥ D④⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com