
题目列表(包括答案和解析)
2、下列各组中两物质,互为同系物的是
A.2-甲基-1-丁烯和1,3-丁二烯 B.苯酚和苯甲醇
C.乙酸和乙酸甲酯 D.乙醛和4-甲基戊醛
1、鉴别甲醇和甲酸时不能使用的试剂是
A.银氨溶液 B.钠 C.石蕊试液 D.铁
27、 (12分))A、B、C、D、E、F、G、H、I、J均为有机化合物。根据以下框图,回答问题:
(12分))A、B、C、D、E、F、G、H、I、J均为有机化合物。根据以下框图,回答问题:
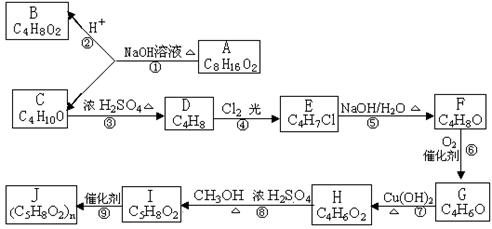
⑴ B和C均为有支链的有机化合物,B的结构简式为 ;C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为 。
⑵ G 能发生银镜反应,也能使溴的四氯化碳溶液褪色,则
G的结构简式 。
⑶ 写出:
⑤的化学方程式是 。
⑨的化学方程式是 。
⑷ ①的反应类型是 ,④的反应类型是 ,⑦的反应类型是 。
⑸ 与H具有相同官能团的H的同分异构体的结构简式为
。
26、(10分)A-L所代表的各物质是中学化学里常见的物质,已知B、J是单质,A是化合物;E的溶液跟苯酚溶液混合,溶液呈紫色。A-L各物质之间相互反应转化的关系如下图所示(未注明必要的反应条件):
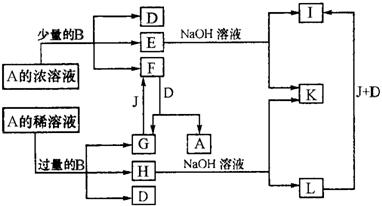
请回答:
⑴ B在A的浓溶液中反应而溶解的条件是 ,而常温下B在A的浓溶液中难以反应而溶解的原因是 。
⑵ 写出下列化学方程式:
F → G + A ;
G → F ;
E → I的离子方程式 。
⑶ L转化成I的现象是 。
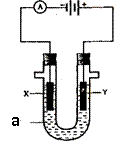
25、(8分)电解原理在化学工业中有广泛应用。右图表示
一个电解池,装有电解液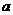 ;X、Y是两块电极板,通过导线与
;X、Y是两块电极板,通过导线与
直流电源相连。请回答以下问题:
⑴ 若X、Y都是惰性电极, 是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
① 电解池中X极上的电极反应式为 ;
在X极附近观察到的现象是 。
② Y电极上的电极反应式为 ;检验该电极反应产物的方法是 。
⑵ 如用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
① X电极的材料是 ,电极反应式为 。
② Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
24、(12分)以黄铁矿为原料生产硫酸的工艺流程图如下:
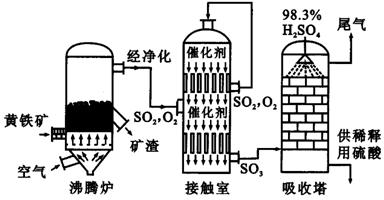
⑴ 将燃烧黄铁矿的化学方程式补充完整
4 + 11O2  2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
⑵ 接触室中发生反应的化学方程式是 。
⑶ 依据工艺流程图判断下列说法正确的是(选填序号字母) 。
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO2的转化率
c.使用催化剂能提高SO2的反应速率和转化率
d.沸腾炉排出的矿渣可供炼铁
⑷ 吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。SO2既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的Br2。SO2吸收Br2的离子方程式是 。
⑸ 将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。则该条件下SO2的平衡转化率为 。
 ⑹ 将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,
⑹ 将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,
可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是
。
23、完成下列各题(10分)
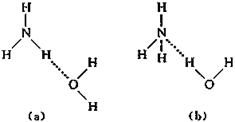
⑴ NH3·H2O的电离方程式为NH3·H2O NH4+ + OH-,试判断NH3溶于水后,形成
NH4+ + OH-,试判断NH3溶于水后,形成
NH3·H2O的合理结构是 (填字母)。
⑵ 沼气是一种很好的能源,它的主要成分是CH4。0.5mol CH4完全燃烧生成CO2和液
态H2O时,放出445kJ热量,则该反应的热化学方程式是
⑶ 下列分子中所有原子都满足最外层8电子结构的单质是( ),是非极性分子的
化合物的是( )(填序号)。
A.氯仿(CHCl3) B.N2 C.BrCl D.NH2D E.CH4 F.H2O G.CO2 H.He
⑷ 近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管,常伴有大量
物质--碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:
 C + K2Cr2O7
+ H2SO4(稀)= CO2 + K2SO4
+ Cr2(SO4)3
+
C + K2Cr2O7
+ H2SO4(稀)= CO2 + K2SO4
+ Cr2(SO4)3
+
① 完成并配平上述反应的化学方程式。
② 此反应的氧化剂是 ,被氧化的元素所对应的产物是 。
③ H2SO4在上述反应中表现出来的性质是 (填选项编号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
第Ⅱ卷(非选择题,共52分)
22、
 市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li 的高分子材料。这种锂离子电池的电池反应为:Li + 2Li0.
35NiO2
2Li0. 85NiO2
的高分子材料。这种锂离子电池的电池反应为:Li + 2Li0.
35NiO2
2Li0. 85NiO2
下列说法不正确的是…………………………………………………………( )
A.放电时,负极的电极反应式:Li - e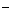 = Li
= Li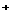
B.充电时,Li0. 85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
 棠湖中学2010届高三上学期9月月考
棠湖中学2010届高三上学期9月月考
化学试题
(2009年9月 命题人:张禄明 审题人:候燕)
总得分:
第Ⅰ卷(选择题,共56分)答案栏
21、一种从植物中提取的天然化合物a-damascone,可用于制作“香水”,其结构为:
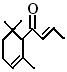 ,有关该化合物的下列说法不正确的是………………………………( )
,有关该化合物的下列说法不正确的是………………………………( )
A.分子式为C13H20O
B.该化合物可发生聚合反应
C.1 mol该化合物完全燃烧消耗19 mol O2
D.与溴的CCl4溶液反应生成的产物经水解、稀硝酸化后可用AgNO3溶液检验
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com