
题目列表(包括答案和解析)
18.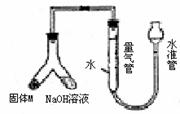 (10分)某课外兴趣小组为探究某种铝合金(合金元素为Mg Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计右图装置进行实验。
(10分)某课外兴趣小组为探究某种铝合金(合金元素为Mg Al)是否符合国家质量标准(国家规定其中铝含量不能低于78%),设计右图装置进行实验。
(1)如何检验该装置的气密性
。
(2)合金样品固体M与氢氧化钠溶液反应的离子方程
式 。
(3)倾斜左边装置使氢氧化钠溶液(足量)与ag合金粉末(固体M)充分反应,待反应停止后,进入量气管气体的体积为VmL(已折算成标准状况)。若量气管最大量程为50mL.,则固体M中铝的质量(mA1)范围为 。
(4)若将装置中的氢氧化钠溶液替换为足量的盐酸,则反应停止后量气管内气体体积 (填“>”“<”“=”)VmL。
(5)若a=38mg,V=44.8mL(标准状况),请通过计算说明该合金是否符合国家标准(不写计算过程) (填“符合”或“不符合”)。
17.27.2g铁粉和氧化铁的混合物,放入500mL稀H2SO4中,发现固体完全溶解,并放出4.48L H2(标况),加入NH4SCN溶液后,无颜色变化,然后向溶液中加入2mol·L-1 NaOH溶液,当溶液呈中性时,用掉NaOH溶液500mL,则原硫酸溶液的物质的量浓度为
A.4 mol·L-1 B.3 mol·L-1 C.2 mol·L-1 D.1 mol·L-1
普通高中阶段性评估练习题
化学试题 2009.11
第Ⅱ卷(非选择题 共60分)
16.硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用:
①Cu与稀硝酸反应制取:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
②Cu与浓硝酸反应制取:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中制取:2Cu+4HNO3+O2=2Cu(NO3)2+2H2O
下列说法正确的是
A.制取相同量的硝酸铜需硝酸的量③最多
B.制取相同量的硝酸铜①产生的有毒气体比②多
C.三种方案中硝酸的利用率③>①>②
D.三种方案的反应都可以在铁制容器中进行
14.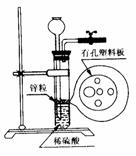 右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中加入的试剂是
右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中加入的试剂是
①食盐水 ②KNO3溶液 ③适量硫酸铜溶液
④Na2CO3溶液 ⑤CCl4 ⑥浓氨水
A.①②④ B.②⑥ C.②③⑤ D.①③⑤
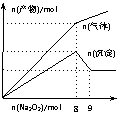 15.将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
15.将Na2O2逐渐加入到含有Al3+、Mg2+、NH4+的混合溶液中并加热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系如图所示。则原溶液中Al3+、Mg2+、NH4+的物质的量分别为
A.2 mol、3 mol、8 mol B.3 mol、2 mol、8 mol
C.2 mol、3 mol、4 mol D.3 mol、2 mol、4 mol
13.下列各组离子在指定溶液中能大量共存的是
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、[Al(OH)4]-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+
④由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3-
⑥酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl-
A.①② B.③⑥ C.②④ D.⑤⑥
12.NO2是导致光化学烟雾的“罪魁祸首”之一。NO2可以用氢氧化钠溶液吸收,或在一定条件下用氨气(NH3)与其反应使之转化为无污染的物质,发生反应的化学方程式分别是:2NO2+2NaOH=M+NaNO3+H2O,8NH3+6NO2=7X+12H2O。则M和X代表的物质的化学式是
A.NaNO2 、N2 B.HNO2、N2 C.NO、HNO3 D.Na3NO4、NO
11.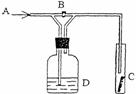 右图是一种试验某气体化学性质的实验装置,图中B为开关。若先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是
右图是一种试验某气体化学性质的实验装置,图中B为开关。若先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是
A.浓H2SO4 B.饱和NaCl溶液
C.浓NaOH溶液 D. 浓NaBr溶液
10.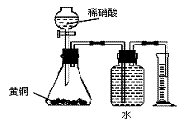 下列实验操作正确的是
下列实验操作正确的是
A.氢氧化钠固体放在滤纸上称量
B.用如右图所示的装置可以测定黄铜(Cu、Zn合金)中 Zn的含量
C.除去粗盐中的Ca2+、Mg2+、SO42-,依次加入的物质可以是H2O、Ba(OH)2、Na2CO3、HCl
D.配制0.184 mol/L H2SO4时,向1000 mL容量瓶中注入10 mL 18.4 mol/L H2SO4然后边加水边振荡,最后定容
9.已知下述三个实验均能发生化学反应
(1)将铁钉放入硫酸铜溶液中;
(2)向硫酸亚铁溶液中滴入几滴浓硝酸;
(3)将铜丝放入氯化铁溶液中
下列判断正确的是
A.上述实验证明氧化性:Fe3+>Fe2+>Cu2+
B.实验(2)中Fe2+既显氧化性又显还原性
C.实验(3)中发生是置换反应
D.实验(1)中铁钉只做还原剂
8.“信息”、“材料”和“能源”被称为新科技革命的三大支柱。下列有关资讯错误的是
A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源
B.目前中美日等国掌握的陶瓷发动机技术,大大提高了发动机的能量转化效率
C.2008年9月25日发射成功的“神舟七号”载人飞船使用了大量的复合材料
D.合成高分子材料的广泛应用是有百利而无一害
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com