
题目列表(包括答案和解析)
25.(12分)X、Y、Z为不同周期(短周期)非金属元素的气态单质。在一定条件下能发生如下反应:Y+X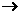 甲(g),Y+Z
甲(g),Y+Z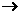 乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
(1)X的化学式是 。
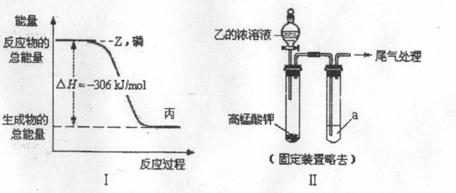
(2)磷在Z气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中备原子最外层均是8电子结构。磷单质和z单质反应生成1mol丙时,反应过程与能量变化如图I所示,该反应的热化学方程式是 。
(3)某同学拟用图Ⅱ所示装置证明氧化性Z>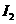 ,已知高锰酸钾与乙的浓溶液反应生成Z,
,已知高锰酸钾与乙的浓溶液反应生成Z,
则a是 的水溶液。若仅将a换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是 。
(4)向一定浓度的BaCl2溶液中通入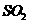 气体,未见沉淀生成,若在通入
气体,未见沉淀生成,若在通入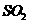 气体的同
气体的同
时加入由甲和乙中的一种或几种元素组成的某纯净物,即可生成白色沉淀,该纯净物可能是
、 。

版权所有:()
版权所有:()

24.(14分)X、Y、Z、 W四种物质有如下相互转化关系(其中X、W为单质,Y、Z为化合物,未列出反应条件)。
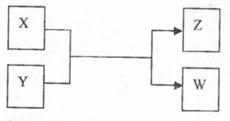
I.若Z是生活中常用的调味品,W遇淀粉溶液变蓝,则:
(1)常温下,X的颜色是 。
(2)工业上Z有多种用途,用化学方程式表示Z的一种工业用途 。
(3)生活中所用的Z加入了碘酸钾,过量X与Y溶液反应时可以得到一种碘酸盐,此反
应的离子方程式是 。
Ⅱ.若X是工业上用量最大的金属单质,Z是一种具有磁性的黑色晶体,则:
(1)X与Y反应的化学方程式是 。
(2)若用下列装置只进行Z+W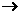 X+Y反应(夹持装置未画出):
X+Y反应(夹持装置未画出):
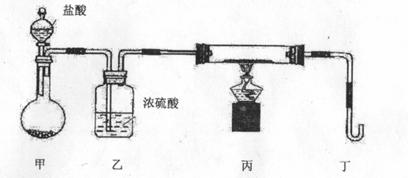
①完成此实验有多步操作,其中三步是:a.点燃酒精灯b.滴加盐酸c.检验气体纯度
这三步操作的先后顺序是 (填字母)。
②为保证实验成功,上述装置需要改进,方法是(用文字叙述) 。
(3)将6.96gZ加入100mL4mol/I。的稀HNO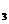 中充分反应,产生224mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀。当沉淀量最多,至少需要加入2
mol/L
中充分反应,产生224mL的NO(标准状况),向反应后的溶液中滴加NaOH溶液能产生沉淀。当沉淀量最多,至少需要加入2
mol/L
的NaOH溶液 mL。
23.(8分)A、B、C、D为中学化学常见的物质,其组成元素均为主族元素。它们间的反
应关系如下图所示。
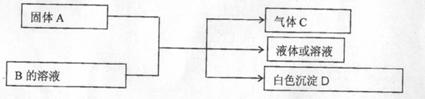
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则A与B共热的化学方程式为
。
(2)若A是碳化钙(CaC2),B是一种盐,A与B的溶液反应时只生成气体C、CaCO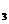
和水,则B的化学式为 。
(3)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,A的相对分子质量与D相同。 向一定量的B溶液中逐渐加入固体粉末A,当A与B以物质的量之比3:1反应时,生成的D的量最多。则A的化学式为 , B的化学式为 。
22.(12分)下图是一个实验室制取氯气并以氯气为原料进行特定反应的装置:
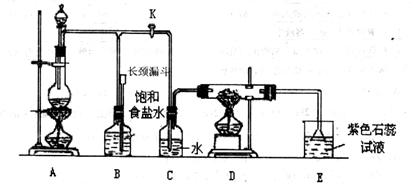
(1)实验开始时,先点燃A处的酒精灯,打开旋塞K,让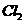 充满整个装置,再点燃D处酒精灯,连接上E装置。
充满整个装置,再点燃D处酒精灯,连接上E装置。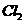 通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为
通过C瓶后再进入D。D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为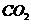 和HCl。试写出D中反应的化学方程式: 。
和HCl。试写出D中反应的化学方程式: 。
(2)装置C的作用是 。
(3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是 。
(4)若将E处烧杯中溶液改为澄清石灰水,反应过程现象为 。(选填标号)
A.有白色沉淀生成 B.无现象 C.先生成白色沉淀,而后白色沉淀消失
(5)D处反应完毕后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有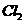 产
产
生,此时B中的现象是 ,B的作用是 。
21.(6分)有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、c的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3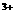 、
、
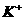 、
、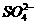 、
、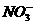 、
、 五种离子。同时生成一种白色沉淀。请回答下列问题:
五种离子。同时生成一种白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是
A.Na+
B.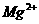 C.
C.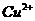 D.
D.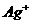
(2)三种正盐的化学式分别是:A ,B ,C 。
(3)不需要加入任何试剂就能将上述三种正盐溶液区分开来,鉴别出来的先后顺序为
(填化学式)
(4)若将A、B、C三种正盐按一定比例溶于水后,所得溶液中只含有Fe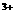 、SO
、SO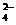 、NO
、NO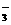 、
、
K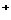 四种离子且物质的量之比依次为1:2:3:4,则A、B、C三种正盐的物质的量
四种离子且物质的量之比依次为1:2:3:4,则A、B、C三种正盐的物质的量
之比为 。
20.已知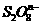 离子和
离子和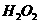 一样含过氧键,因此也有强氧化性,
一样含过氧键,因此也有强氧化性,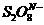 离子在一定条件下可以把
离子在一定条件下可以把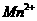 氧化成
氧化成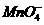 离子,若反应后
离子,若反应后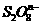 离子变成
离子变成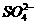 离子;又知反应中氧化剂与还原剂的离子数之比为5:2,则
离子;又知反应中氧化剂与还原剂的离子数之比为5:2,则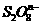 中的
中的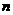 值和S元素的化合价是
值和S元素的化合价是
A.2,+6 B.2,+7 C.4,+7 D.4,+4
第II卷(非选择题,共52分)
19.已知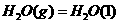
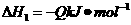
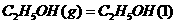


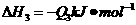
若使23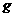 酒精液体完全燃烧,最后恢复到室温,则放出的热量为
酒精液体完全燃烧,最后恢复到室温,则放出的热量为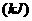
A.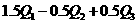 B.
B.
C.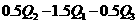 D.
D.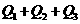
18.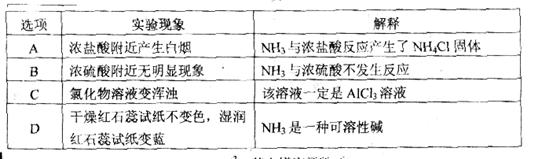 某氯化镁溶液的密度为1.18 g·cm
某氯化镁溶液的密度为1.18 g·cm ,其中镁离子的质量分数为5.1%,300 mL该溶液中氯离子的物质的量约等于( )
,其中镁离子的质量分数为5.1%,300 mL该溶液中氯离子的物质的量约等于( )
A.0.37mol B.0.63mol
C.0.74mol D.1. 5mol
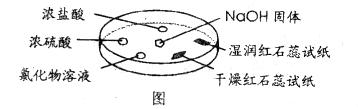
17.如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )
16.下列离子方程式中正确的是( )
A.在漂白粉的溶液中通入一定量的二氧化硫气体
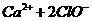
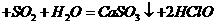
B.2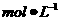 的
的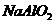 溶液和5
溶液和5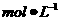 的HCl溶液等体积混合均匀;
的HCl溶液等体积混合均匀;
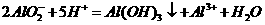
C.纯碱溶液与胆矾溶液混合生成正盐、酸式盐、碱式盐
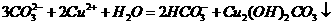
D.在碳酸氢镁溶液中加入足量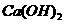 溶液:
溶液:
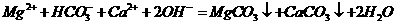
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com