
题目列表(包括答案和解析)
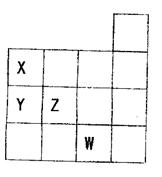
9.右图表示元素周期表前四周期的一部分,关于元素X、Y、Z、W的叙述正确的是
①X、Y的最高价氧化物的水化物酸性为Y<X
②Y、Z的气态氢化物的稳定性Y<Z 

③W的单质常温下呈液态,一定条件下可与铁粉反应
④W的原子序数比Z大9
A.只有③ B.①② C.①②③ D.①②③④
8.某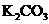 样品中含有
样品中含有 和
和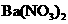 三种杂质中的一种或二种.现将13.8克样品加入足量水,样品全部溶解.再加入过量的
三种杂质中的一种或二种.现将13.8克样品加入足量水,样品全部溶解.再加入过量的 溶液,得到11克沉淀.对样品所含杂质的正确判断是
溶液,得到11克沉淀.对样品所含杂质的正确判断是
A.肯定只有 B.肯定有
B.肯定有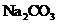 ,可能还含有
,可能还含有
 C.肯定没有
C.肯定没有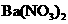 ,可能有
,可能有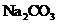 D.肯定没有
D.肯定没有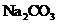 和
和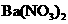
7.下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是
A. 溶液中通入过量
溶液中通入过量 :
: 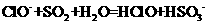


B. 在空气中被氧化:
在空气中被氧化: 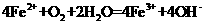
C.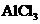 溶液中投入过量Na:
溶液中投入过量Na: 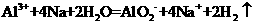
D.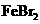 溶液中通入少量
溶液中通入少量 :
: 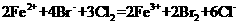
6.某无色溶液中加入过量的盐酸有沉淀生成,过滤后向滤液中加入过量的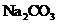 溶液又有沉淀生成,原溶液中能大量存在的离子组是
溶液又有沉淀生成,原溶液中能大量存在的离子组是
① ②
②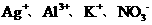 ③
③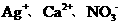
④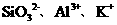 ⑤
⑤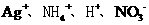 ⑥
⑥
A.①②⑤ B.②③ C.②③④⑥ D.①②③④⑥
5.铜、银、金是人类认识最早的三种金属,因为很早就被人们用作钱货,因而有“货币金属”之称。由于铁的金属性比铜、银、金强,相对而言,人类认识铁稍晚,某研究性学习小组为了证明铁的金属活动性比铜强,他们设计了如下方案
①铁片置于硫酸铜溶液中有铜析出;
②铁、铜和氯气反应分别生成 和
和
③足量的铁粉和铜粉和浓硫酸反应生成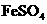 和
和 ;
; 

④铜片置于 溶液中铜片逐渐溶解
溶液中铜片逐渐溶解
⑤把铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接,铁片上无气泡产生,而铜片上有气泡产生。
⑥把铁片和铜片置于盛有浓硝酸的烧杯中,并用导线连接,铁片上有气泡产生,而铜片上无气泡产生。 

以上设计合理的有
A.两种方案 B.三种方案 C.四种方案 D.五种方案
4.下列说法:①质子数相同的粒子一定属于同种素;②电子数相同的粒子不一定是同一种元素;③一种元素只能有一种质量数;④某种元素的相对原子质量取整数,就是其质量数。⑤质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子;⑥同位素的性质几乎完全相同;其中不正确的是
A.①③④⑥ B.①②④⑤ C.②③⑤⑥ D.②⑤
3.下列叙述中,结论和对应的解释均不正确的是
A.金刚石的熔沸点高于晶体硅;因为C-C键能大干Si-Si键能
B.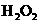 是非极性分子,因为
是非极性分子,因为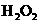 分子的空间构直线型
分子的空间构直线型
C.二氧化硅晶体中不存在简单的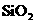 分子,因为其晶体是含有硅氧四面体的空间网状结构
分子,因为其晶体是含有硅氧四面体的空间网状结构
D.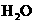 比
比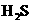 稳定:因为
稳定:因为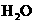 分子之间有氢键,
分子之间有氢键,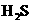 分子之间无氢键
分子之间无氢键 

2.目前人类已发现的非金属元素除稀有气体外共有16种,下列对这16种非金属元素的
相关判断合理的是
①都是主族元素,最外层电子数都大于或等于4;
②单质在反应中都只能作氧化剂; 

③氢化物常温下都是气态,所以又都叫气态氢化物;
④氧化物常温下都可以与水反应生成酸。
A只有①正确 B.只有①③正确 C.只有③正确 D.①②③④均不正确
1.判断下列有关化学基本概念的依据正确的是
A.氧华还原反应;元素化合价是否变化
B.碱性氧化物:是否是金属氧化物
C.电解质和非电解质:溶于水或熔融状态下能否导电
D.同素异形体:是否由同一种原子构成
21.三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。NF3是一种三角锥型分子,键角102°,沸点-129°C;可在铜的催化作用下由F2和过量NH3反应得到。
(1)写出制备NF3的化学反应方程式: 。
(2)NF3的沸点比NH3的沸点(-33°C)低得多的主要原因是 。
(3)与铜属于同一周期,且未成对价电子数最多的元素基态原子核外电子排布式为
。
(4)理论上HF、NaAlO2和NaCl按6:1:2的物质的量之比恰好反应生成HCl、H2O和一种微溶于水的重要原料,该物质含有三种元素,在金属铝的冶炼中有重要作用。该物质为配合物,其中心离子是 ,配位数为 。
(5)根据下列五种元素的第一至第上电离能数据(单位:kJ·mol-1),回答下面各题:
|
元素代号 |
I1 |
I2 |
I3 |
I4 |
|
Q |
2080 |
4000 |
6100 |
9400 |
|
R |
500 |
4600 |
6900 |
9500 |
|
S |
740 |
1500 |
7700 |
10500 |
|
T |
580 |
1800 |
2700 |
11600 |
|
U |
420 |
3100 |
4400 |
5900 |
①在周期表中,最可能处于同一族的是 和 。
②T元素最可能是 (填“s”、“p”、“d”、“ds”等)区元素,位于 族。
若T为第二周期元素,F是第三周期元素中原子半径最小的元素,则T、F形成化合物的空间构型为 ,其中心原子的杂化方式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com