
题目列表(包括答案和解析)
15、(12分)元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
(1)第四周期过渡元素的明显特征是形成多种多样的配合物。
① CO可以和很多过渡金属形成配合物,如羰基铁[Fe(CO)5]、羰基镍[Ni(CO)4]。CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,CO的结构式为 ,与CO互为等电子体的离子为 (填化学式)。
② 金属镍粉在CO气流中轻微加热,生成液态Ni(CO)4分子。423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉。试推测Ni(CO)4易溶于下列 。
a. 水 b. 四氯化碳 c. 苯 d. 硫酸镍溶液
(2)第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。镓的基态原子的电子排布式是 ,Ga的第一电离能却明显低于Zn,原因是 。
(3)用价层电子对互斥理论预测H2Se和BBr3的立体结构,两个结论都正确的是 。
a.直线形;三角锥形 b.V形;三角锥形 c.直线形;平面三角形 d.V形;平面三角形
14.根据下列有关图象,说法正确的是
 A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
A.由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
B.由图Ⅱ知,反应在t6时,NH3体积分数最大
C.由图Ⅱ知,t3时采取降低反应体系压强的措施
D.Ⅲ在10L容器、850℃时反应,由图知,到4min时,反应放出51.6kJ的热量
13.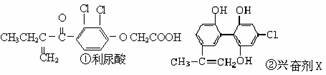 “人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是重要举措之一。以下两种兴奋剂的结构分别为:则关于它们的说法中正确的是
“人文奥运、科技奥运、绿色奥运”是2008年北京奥运会的重要特征。其中禁止运动员使用兴奋剂是重要举措之一。以下两种兴奋剂的结构分别为:则关于它们的说法中正确的是
A.利尿酸分子中有三种含氧官能团,在核磁
共振氢谱上共有六个峰
B.1 mol兴奋剂X与足量浓溴水反应,最多消耗4 mol Br2
C.两种兴奋剂均属于芳香族化合物D.两种分子中的所有碳原子均不可能共平面
12.用NA代表阿伏加德罗常数,下列说法正确的是
A.0℃、2.02×l05帕时,1molCO2的质量为44g
B.7.1g氯气与足量的氢氧化钠溶液反应时,转移电子数为0.2NA个
C.11.2 L HCl气体溶于水,配制成1 L盐酸,其浓度为0.5mol/L
D.足量的铜片与含4 mol HNO3的浓硝酸充分反应生成二氧化氮的分子数为2NA
11.某同学用回收的镁铝合金制取氢气。现有l0.8 g镁铝合金,下列说法正确的是
A.常温下与足量18mol/LH2SO4反应,最多可放出0.6 mol H2
B.常温下与足量2mol/LHNO3反应,最少可放出0.45 mol H2
C.常温下与足量2 mol/L H2SO4反应,放出H2的量在0.45 mol-0.6 mol之间
D.常温下与足量2mol/LNaOH反应,放出H2的量在0.45 mol-0.6 mol之间
10.常温下,下列有关叙述不正确的是
A.足量铁屑溶于稀硝酸所得溶液中:c(NO3-)>c(Fe2+)>c(H+)>c(OH-)
B.pH相同的CH3COONa溶液、C6H5ONa溶液、Na2CO3溶液、NaHCO3溶液:
c(CH3COONa)>c(NaHCO3) >c(C6H5ONa ) >c(Na2CO3 )
C.已知酸性HF>CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F-)] > [c(K+)-c(CH3COO-)]
D.10 mL pH=12的氢氧化钠溶液中加入pH=2的HA溶液至pH刚好等于7,所得溶液体积V(总)≥20 mL
9.下列离子方程式书写正确的是
A.硝酸银溶液中滴加过量氨水:Ag++NH3·H2O==AgOH↓+NH4+
B.NaHS溶液呈碱性:HS-+ H3O+
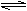
 H2S + H2O
H2S + H2O
C.4 mol/L的KAl(SO4)2溶液与7 mol/L的Ba(OH)2溶液等体积混合:
4Al3++7SO42-+7Ba2++14OH-==2Al(OH)3↓+2AlO2-+7BaSO4↓+4H2O
D.食醋清除热水瓶胆水垢:2H++CaCO3=Ca2++H2O+CO2↑
8.玻璃棒是化学实验中常用的仪器,其作用是用于搅拌、过滤或转移液体时引流。下列有关实验过程中,
般不需要使用玻璃棒进行操作的是
①用pH试纸测定Na 2CO3溶液的pH ②从氯酸钾和二氧化锰制取氧气的剩余固体中提取KCl
③实验室用新制的FeSO4溶液和预处理过的NaOH溶液制备Fe(OH)2白色沉淀
④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验⑤将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体⑥用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
⑦探究Ba(OH)2·8H2O晶体和NH4Cl晶体反应过程中的能量变化
A.②③⑦ B.③④⑤ C.⑤⑥⑦ D.④⑥⑦
7.某碳酸钾样品中的杂质含有纯碱、硝酸钾、硝酸钡中的一种或两种。取7.8g该样品溶于适量水中得到澄清溶液,再加入过量CaCl2溶液得到沉淀5.0g。下列对原样品中所含杂质的判断正确的是:
A.一定没有Na2CO3和Ba(N O3)2 B.一定有Na2CO3而没有Ba(N O3)2
C.没有Ba(N O3)2但有K N O3可能还有Na2CO3 D.没有Na2CO3但有Ba(N O3)2和K N O3
6.下列各组离子中,一定能大量共存的是:
A.pH=0的无色溶液中:Na+、K+、MnO-4、NO-3 B.加入铝粉有氢气产生的溶液中:Na+、SO42-、C1-、K +
C.在由水电离出的c(矿)为10-12mol·L-l的溶液中:AlO2-、SO42-、Na+、Mg2+
D.在0.10mol·L-1的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com