
题目列表(包括答案和解析)
12. 银锌钮扣电池的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应为 Zn+2OH--2e-=ZnO+H2O;
Ag2O+H2O+2e-=2Ag+2OH- ;总反应为:Ag2O+Zn=2Ag+ZnO,下列判断正确的是
A.锌为正极,Ag2O为负极 B.如果有1mol电子转移,就有32.5g Zn参加反应
C.原电池工作时,正极区PH减小 D. 锌为阳极,Ag2O为阴极
11. 家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此过程中不发生反应
A.4Fe(OH)2+2H2O+O2===4Fe(OH)3 B.2Fe+2H2O+O2===2Fe(OH)2
C.2H2O+O2+4e-===4OH- D.Fe-3e-===Fe3+
10. 已知H-H键能为436 KJ/mol,H-N键能为391KJ/mol,根据化学方程式:
N2 + 3H2 = 2NH3 ΔH=-92.4 KJ/mol,则N≡N键的键能是
A.431 KJ/mol B.946 KJ/mol C.649 KJ/mol D.869 KJ/mol
9. 已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是
A.H2O(g)=H2(g)+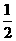 O2(g);
O2(g);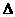 H= +242kJ·mol-1
H= +242kJ·mol-1
B.2H2(g)+O2(g) = 2H2O(l);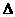 H=
-484kJ·mol-1
H=
-484kJ·mol-1
C.H2(g)+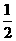 O2(g)=H2O(g);
O2(g)=H2O(g);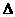 H=
+242kJ·mol-1
H=
+242kJ·mol-1
D.2H2(g)+O2(g)=2H2O(g);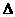 H=+
484kJ·mol-1
H=+
484kJ·mol-1
8. 在5 L的密闭容器中充入2 mol A气体和1 mol B气体,一定条件下发生反应:2A(g)+B(g)==2C(g),达平衡时,在相同温度下测得容器内混合气体的压强是反应前的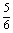 ,则A的转化率为
,则A的转化率为
A.67% B.50% C.25% D.5%
7. 反应 A(g)+B(g)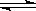 3C(g);△H>0。下列反应条件有利于生成C的是
3C(g);△H>0。下列反应条件有利于生成C的是
A.低温、低压 B.低温、高压 C.高温、高压 D.高温、低压
6. 在一定温度下,可逆反应A(g)+3B(g) 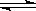
 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.B的浓度和C的浓度相等
B.单位时间生成n mol A,同时生成3n mol B
C.A、B、C的浓度不再变化
D.A、B、C的分子数比为1:3:2
5. 下列说法正确的是
A.钢铁在中性条件下发生吸氧腐蚀.
B.甲醇碱性燃料电池的负极反应式为:O2 +2H2O +4e- = 4OH-
C.铁片镀铜时,铁片与电源正极相连
D.用惰性电极电解硫酸溶液,电解过程中溶液的pH保持不变
4. 燃料电池是燃料(例如CO,H2,CH4等)跟氧气或空气起反应,将此反应的化学能转变为电能的装置,电解质通常是KOH溶液。下列关于甲烷燃料电池的说法不正确的是
A.负极反应式为CH4 + 10OH-- 8 e -= CO32-+ 7H2O
B.正极反应式为O2 + 2H2O + 4 e -= 4OH-
C.随着不断放电,电解质溶液碱性不变
D.甲烷燃料电池的能量利用率比甲烷燃烧的能量利用率大
3. 在恒温恒容条件下,能使A(g)+B(g) C(g)+D(g)正反应速率瞬时增大的措施是
C(g)+D(g)正反应速率瞬时增大的措施是
A.减小C或D的浓度 B.增大D的浓度
C.减小B的浓度 D.增大A或B的浓度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com