
题目列表(包括答案和解析)
7、下列元素的最高价氧化物溶于水,形成的含氧酸的酸性最强的是
A、原子最外层电子数是次外层的2倍的元素
B、原子M层电子数等于另两层电子数之差的元素
C、第三周期ⅦA族的元素
D、其单质有多种同素异形体,其中一种着火点很低、能自燃的元素高
6、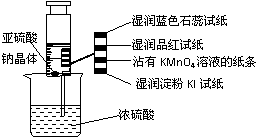 如图所示,在注射器中加入少量Na2SO3晶体,并吸收少量浓硫酸(以不接触纸条为准),则下列有关说法正确的是
如图所示,在注射器中加入少量Na2SO3晶体,并吸收少量浓硫酸(以不接触纸条为准),则下列有关说法正确的是
A.蓝色石蕊试纸先变红后褪色
B.沾有KMnO4溶液的滤纸褪色,
证明了SO2的漂白性
C.湿润淀粉KI试纸变蓝
D.品红试纸褪色证明了SO2的漂白性
5、在一定的温度下,向饱和的烧碱溶液中放入一定量的过氧化钠,充分反应后恢复到原来的温度,下列说法正确的是
A.溶液中Na+浓度增大,有O2放出 B.溶液中OH-总数不变,有O2放出
C.溶液的pH增大,有O2放出 D.溶液中Na+总数减少,有O2放出
4、下列的比较顺序中,不正确的是
A.热稳定性:HF>HCl>HBr>HI B.微粒半径:K+>Na+>Mg2+>Al3+
C.碱性:CsOH>RbOH>KOH>NaOH D.熔点:Li<Na<K<Rb
3、 下列有关0.1 mol·L-1 NaOH 溶液的叙述正确的是
A.1L该溶液中含有NaOH 40g
B.100mL该溶液中含有OH- 0.01mol
C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol·L-1
D.在1L水中溶解4g NaOH即可配制得0.1 mol·L-1NaOH 溶液
2、 “脚印”、“笑脸”、“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色反应”知识相关。下列说法中正确的是
A.非金属单质燃烧时火焰均为无色
B.只有金属单质灼烧时火焰才有颜色
C.焰色反应均应透过蓝色钴玻璃观察
D.NaCl与Na2CO3灼烧时火焰颜色相同
1、
金属钛对体液无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列有关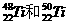 的说法中正确的是
的说法中正确的是
A.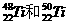 原子中均含有22个中子
原子中均含有22个中子
B.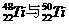 为同一核素
为同一核素
C.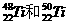 在周期表中位置相同
在周期表中位置相同
D.分别由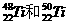 组成的金属钛单质互称为同分异构体
组成的金属钛单质互称为同分异构体
31.将23.9g表面已锈蚀成铜绿[Cu2(OH)2CO3]的铜片投入120mL一定浓度的硝酸中;充分反应后,硝酸被还原成NO2和NO,测得反应后溶液PH值为1。往反应后的溶液中加入过量的NaOH溶液,滤出沉淀,洗涤,干燥后得到29.4g蓝色固体。(假设反应前后溶液的体积不变)
计算:(1)已锈蚀的铜片中的铜元素的质量分数为 。(保留两位小数)
(2)求铜片中单质铜的物质的量。(写出计算过程)高考资源
(3)若生成NO2和NO混合气体共aL(S.P.T)。高考资源
①a的取值范围为 。
②原硝酸的浓度为多少?(只需用a的代数式表示,写出过程)
30.赤铁矿是炼铁的主要原料之一。它的主要成分在一定条件下有下列反应:
|
 Fe2O3+CO
2FeO+CO2
Fe2O3+CO
2FeO+CO2
在反应形成的固体混合物(Fe2O3、FeO)中,元素铁和氧的质量比用m(Fe):m(O)表示。
(1)根据上述反应,固体质量每减烃1.6g,将产生CO2 L(S.T.P)。
(2)上述反应形成的固体混和物中,m(Fe):m(O)不可能是 (多选扣分)。
A.21:9 B.21:7.5 C.21:5 D.21:8
(3)Fe2O3被CO还原的百分率为50%,则m(Fe):m(O)= 。高考资源
29.化合物A是石油化工的一种重要原料,用A和水煤气为原料经下列途径合成化合物D(分子式为C3H6O3)。高考资源
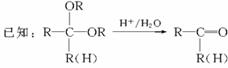
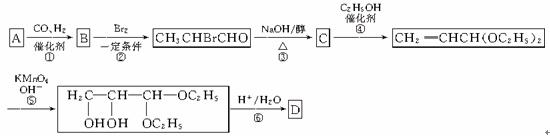
请完成下列问题:(1)写出下列物质的结构简式:高考资源
A:____________,B:____________,C:____________,D:____________。
(2)指出反应②的反应类型________________。高考资源
(3)写出反应③的化学方程式________________________________________________。
(4)反应④的目的是_________________________________________________________。
(5)化合物D′是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物。D′在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4)。请分别写出D′生成E和F的化学方程式:D′→E:__________________________________________________________。高考资源
D′→F:____________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com