
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
3ЁЂвЊЬсДПЯТСаЮяжЪ(РЈКХФкЮяжЪЮЊдгжЪ)ЃЌЪЕбщВйзїКЯРэЕФЪЧЁЁЁЁЁЁЁЁЁЁ
AЃЎСђЫсЬњШмвК(СђЫсбЧЬњ)ЃКЭЈШызуСПТШЦјЃЌГфЗжЗДгІКѓМгШШЃЌЪЙЖргрТШЦјвнГі
BЃЎБН(БНЗг)ЃКМгШызуСПЕФХЈфхЫЎЃЌГфЗжеёЕДЃЌОВжУЗжВуКѓЗжРы
CЃЎCO2(SO2)ЃКЭЈШыЪЂгаNa2CO3ШмвКЕФЯДЦјЦП
DЃЎMg(OH)2[Ca(OH)2]ЃКЗХШыЫЎжаЕїГЩНЌзДЃЌМгШызуСПMgCl2ШмвКЃЌГфЗжНСАшЃЌЙ§ТЫЃЌГСЕэгУеєСѓЫЎЯДЕг
2ЁЂЯТСаЫЕЗЈЛђзіЗЈжае§ШЗЕФЪЧ
AЃЎЗњТШЬўЕФДѓСПХХЗХЪЧдьГЩЫсгъЕФжївЊдвђ
BЃЎЕШжЪСПЕФЭЌжжУКЗлКЭУКПщЭъШЋШМЩеЃЌЗХГіШШСПЧАепДѓгкКѓеп
CЃЎвКТШаЙТЉЪТЙЪЗЂЩњЪБЃЌжмБпЕФШЫгІИУГЏЫГЗчЗНЯђЬгвнЛђЯђБмЗчЕФЙЕЬСЕЭЭнДІзЊвЦ
DЃЎЛ№М§ЗЂЖЏЛњгаЦЋЖўМзыТ(C2H8N2)гыN2O4ЛьКЯКѓГфЗжШМЩеЃЌПЩЩњГЩCO2ЁЂN2КЭH2O
1ЁЂ 2007ФъХЕБДЖћЛЏбЇНБЪкгшЕТЙњЛЏбЇМвGerhard ErtlЃЌвдБэеУЫћдкБэУцЛЏбЇСьгђбаОПЫљШЁЕУЕФПЊЭиадГЩОЭЁЃФГЗДгІдкPt/Al2O3/BaДпЛЏМСБэУцЮќИНгыНтЮќзїгУЕФЛњРэШчЯТЭМЫљЪО(ЭМжаHCБэЪОЬМЧтЛЏКЯЮяЃЌnitrateжИЯѕЫсбЮ)ЃЌИУЛњРэбаОПЪЧжИ
2007ФъХЕБДЖћЛЏбЇНБЪкгшЕТЙњЛЏбЇМвGerhard ErtlЃЌвдБэеУЫћдкБэУцЛЏбЇСьгђбаОПЫљШЁЕУЕФПЊЭиадГЩОЭЁЃФГЗДгІдкPt/Al2O3/BaДпЛЏМСБэУцЮќИНгыНтЮќзїгУЕФЛњРэШчЯТЭМЫљЪО(ЭМжаHCБэЪОЬМЧтЛЏКЯЮяЃЌnitrateжИЯѕЫсбЮ)ЃЌИУЛњРэбаОПЪЧжИ
AЃЎЦћГЕЮВЦјДпЛЏзЊЛЏДІРэ
BЃЎИжЬњЩњатЛњРэ
CЃЎКЯГЩАБЙЄвЕДпЛЏбѕЛЏЛњРэ
DЃЎЧтбѕШМЩеЕчГиЕчМЋЗДгІЛњРэ
16ЁЂЯђФГЯЁHNO3КЭFe(NO3)3ЕФЛьКЯШмвКжаж№НЅМгШыFeЗлЃЌВњЩњЮоЩЋЦјЬхЃЌИУЦјЬхгіПеЦјБфКьзиЩЋЃЌШмвКжаFe2+ХЈЖШКЭМгШыFeЗлЕФЮяжЪЕФСПжЎМфЕФЙиЯЕШчЯТЭМЫљЪО
(1)аДГіЯрЙиЕФЗДгІЕФРызгЗНГЬЪНЁЃ
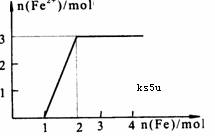 (2)дЯЁШмвКжаHNO3КЭFe(NO3)3ЕФЮяжЪЕФСПХЈЖШжЎБШЮЊЖрЩйЃП
(2)дЯЁШмвКжаHNO3КЭFe(NO3)3ЕФЮяжЪЕФСПХЈЖШжЎБШЮЊЖрЩйЃП
15ЁЂ(1)ЕкШ§жмЦк8жждЊЫиАДЕЅжЪШлЕуИпЕЭЕФЫГађШчгвЭМЃЌЦфжаађКХЁА8ЁБДњБэЁЁЁЁЁЁЁЁ (ЬюдЊЫиЗћКХ)ЃЛЦфжаЕчИКадзюДѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЭМ1жаЕФађКХ)ЁЃ

(2)ЧыаДГіБШдЊЫи1ЕФдзгађЪ§Дѓ8ЕФдЊЫиЕФЛљЬЌдзгЕчзгХХВМЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
(3)дЊЫи7ЕФЕЅжЪОЇЬхжадзгЕФЖбЛ§ЗНЪНШчЭММзЫљЪОЃЌЦфОЇАћЬиеїЭМввЫљЪОЃЌдзгжЎМфЯрЛЅЮЛжУЙиЯЕЕФЦНУцЭМШчЯТЭМЫљЪОЁЃШєвбжЊ7ЕФдзгАыОЖЮЊdЃЌNAДњБэАЂЗќМгЕТТоГЃЪ§ЃЌ7ЕФЯрЖддзгжЪСПЮЊMЃЌЧыЛиД№ЃК
ЂйОЇАћжа7дзгЕФХфЮЛЪ§ЮЊ___ ___ЁЁЁЁ _ ЃЌвЛИіОЇАћжа7дзгЕФЪ§ФПЮЊ_ЁЁЁЁЁЁЁЁЁЁ _ЃЛ
ЂкИУОЇЬхЕФУмЖШЮЊ______ЁЁЁЁЁЁЁЁЁЁЁЁ _ЁЁ (гУзжФИБэЪО)ЁЃ
14ЁЂЯђвЛЖЈСПЕФFeЁЂFeOКЭFe2O3ЕФЛьКЯЮяжаМгШы120mL 4mol/LЕФЯЁЯѕЫсЃЌЧЁКУЪЙЛьКЯЮяЭъШЋШмНтЃЌЗХГі0.06 mol NOЃЌЭљЫљЕУШмвКжаМгШыKSCNШмвКЃЌЮобЊКьЩЋГіЯжЁЃШєгУзуСПЕФЧтЦјдкМгШШЯТЛЙдЯрЭЌжЪСПЕФдЛьКЯЮяЃЌФмЕУЕНЬњЕФЮяжЪЕФСПЮЊ
AЃЎ0.24molЁЁЁЁЁЁЁЁЁЁ BЃЎ0.21molЁЁЁЁЁЁЁЁЁЁ CЃЎ0.16molЁЁЁЁЁЁЁЁЁЁ DЃЎ0.14mol
13ЁЂ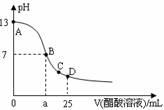 дк25mL 0.1mol/L NaOHШмвКжаж№ЕЮМгШы0.2mol/L CH3COOHШмвКЃЌЧњЯпШчЯТЭМЫљЪОЃЌгаЙиСЃзгХЈЖШЙиЯЕе§ШЗЕФЪЧ
дк25mL 0.1mol/L NaOHШмвКжаж№ЕЮМгШы0.2mol/L CH3COOHШмвКЃЌЧњЯпШчЯТЭМЫљЪОЃЌгаЙиСЃзгХЈЖШЙиЯЕе§ШЗЕФЪЧ
AЃЎдкAЁЂBМфШЮвЛЕуЃЌШмвКжавЛЖЈгаc(Na+)ЃОc(CH3COO-)ЃОc(OH-)ЃОc(H+)
BЃЎдкBЕуЃЌaЃО12.5ЃЌЧвгаc(Na+)ЃНc(CH3COO-)ЃНc(OH-)ЃНc(H+)
CЃЎдкCЕуЃКc(CH3COO-)ЃОc(Na+)ЃОc(H+)ЃОc(OH-)
DЃЎдкDЕуЃКc(CH3COO-)+c(CH3COOH)ЃН2c(Na+)
19.4gАзЩЋЙЬЬхЁЃдђЯТСаЫЕЗЈжае§ШЗЕФЪЧ
AЃЎДЫАзЩЋЙЬЬхЪЧKOHКЭK2CO3ЕФЛьКЯЮя
BЃЎДЫАзЩЋЙЬЬхЪЧK2CO3КЭKHCO3ЕФЛьКЯЮя
CЃЎдKOHШмвКЕФЮяжЪЕФСПХЈЖШЪЧ1 mol/L
DЃЎдKOHШмвКЕФЮяжЪЕФСПХЈЖШЪЧ0.5 mol/L
12ЁЂЯђ300mLKOHШмвКжаЛКТ§ЭЈШы2.24L(БъзМзДПі) CO2ЦјЬхЃЌГфЗжЗДгІКѓЃЌдкМѕбЙЕЭЮТЯТеєЗЂШмвКЃЌЕУЕН
11ЁЂ
 дкШнЛ§ВЛБфЕФУмБеШнЦїжаЕФШчЯТЗДгІЃК2SO2(g)+O2(g)ЁЁЁЁЁЁ 2SO3(g)+196.6kJЁЄmol-1ЃЌ
дкШнЛ§ВЛБфЕФУмБеШнЦїжаЕФШчЯТЗДгІЃК2SO2(g)+O2(g)ЁЁЁЁЁЁ 2SO3(g)+196.6kJЁЄmol-1ЃЌ
ЕБЦфЫћЬѕМўВЛБфЪБЃЌИФБфФГвЛЬѕМўЖдЩЯЪіЗДгІЕФгАЯьЃЌЯТСаЗжЮіе§ШЗЕФЪЧ(ЁЁЁЁ )
AЃЎЭМIбаОПЕФЪЧt0ЪБПЬдіДѓO2ЕФХЈЖШЖдЗДгІЫйТЪЕФгАЯь
BЃЎЭМIIбаОПЕФЪЧt0ЪБПЬМгШыДпЛЏМСКѓЖдЗДгІЫйТЪЕФгАЯь
CЃЎЭМIIIбаОПДпЛЏМСЖдЦНКтЕФгАЯьЃЌЧвМзЕФДпЛЏаЇТЪБШввИп
DЃЎЭМIIIбаОПЕФЪЧЮТЖШЖдЛЏбЇЦНКтЕФгАЯьЃЌЧвввЕФЮТЖШНЯЕЭ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com