
题目列表(包括答案和解析)
4、下列叙述不正确的是
A.常温下浓硫酸可贮存在铁制或铝制容器中,说明常温下铁和铝与浓硫酸不反应
B.将Cl2和SO2分别通入到品红溶液中,均能使品红溶液褪色
C.反应AgCl + NaBr AgBr + NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
AgBr + NaCl能在水溶液中进行,是因为AgBr比AgCl更难溶于水
D.硝酸银溶液通常保存在棕色试剂瓶中,是因为硝酸银见光易分解
3、相互反应时,无论何种试剂过量离子方程式都正确的是
 A.盐酸与NaAlO2溶液:
A.盐酸与NaAlO2溶液: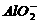 +H++H2O
Al(OH)3↓
+H++H2O
Al(OH)3↓
 B.石灰水与磷酸二氢钠溶液:2H2PO
B.石灰水与磷酸二氢钠溶液:2H2PO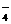 +3Ca2++4OH- Ca3(PO4)2↓+4H2O
+3Ca2++4OH- Ca3(PO4)2↓+4H2O
 C.明矾溶液与小苏打:Al3++3HCO
C.明矾溶液与小苏打:Al3++3HCO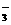 Al(OH)3+3CO2↑
Al(OH)3+3CO2↑
 D.硫酸氢钠溶液和氢氧化钡:SO
D.硫酸氢钠溶液和氢氧化钡:SO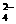 + 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
+ 2H+ +Ba2+ + 2OH- BaSO4↓
+ 2H2O
2、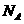 为阿伏加德罗常数,下列叙述正确的是
为阿伏加德罗常数,下列叙述正确的是
A.3.5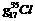 原子中所含中子数为1.7
原子中所含中子数为1.7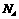 B.一定条件下,1
B.一定条件下,1
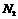 与足量
与足量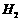 反应,可生成2
反应,可生成2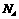 个
个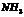 分子
分子
C.在含1 碳原子的石墨中,“C-C”键数为3
碳原子的石墨中,“C-C”键数为3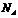 D.
D.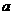

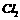 与足量烧碱溶液完全反应转移的电子数为
与足量烧碱溶液完全反应转移的电子数为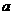
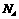
1、化学与生活是紧密相联的,下列关于生活与化学的说法正确的是
A.随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
B.现在用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,前者属于碳氢化合物,后者是烃的衍生物。
C.环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于有机物
D.保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
16、我国规定饮用水质量标准必须符合下表要求:以下是源水处理成自来水的工艺流程示意图

(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式____ _________
(2)凝聚剂除去悬浮固体颗粒的过程_____(填写编号,多选倒扣)①只有物理过程 ②只是化学过程 ③是物理和化学过程 FeSO4·7H2O常用的凝聚剂,它在水中最终生成_____ ______沉淀。
(3)通入二氧化碳的目的是__________ _______和_______ ______。
(4)气体A通常使用氯气,氯气的作用是基于其和水反应的产物之一具有______________性,请写出氯气与水反应的离子反应方程式 。
(5)下列物质中能作为氯气的代用品的是 (填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
15、(1)前四周期元素中,基态原子中未成对电子与其所在周期数相同的元素有 种。
(2)第ⅢA、ⅤA族元素组成的化合物AlN、AlP、AlAs等是人工合成的平等体材料,其晶体结构与单晶硅相似,As原子的电子排布式为 。在AlN晶体中,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(3)在极性分子NCl3中,N原子的化合物为―3,Cl原子的化合价为+1,请推测NCl3水解的主要产物是
(填化学式)
14、室温下,下列混合溶液中,各离子浓度的关系正确的是
A、pH=12的氨水溶液与pH=2的盐酸溶液等体积混合c(NH4+)﹥c(Cl-)﹥c(OH-)﹥c(H+)
B、浓度均为0.1mol/L的硫酸氢铵溶液与氢氧化钠溶液等体积混合
c(Na+)﹥c(SO42-)﹥c(NH4+)﹥c(H+)﹥c(OH-)
C、浓度为0.1mol/L的碳酸钠溶液c(Na+)+ c(H+)=2c(CO32-)+c(OH-)
D、 浓度为0.1mol/L的醋酸钠溶液c(Na+)=c(CH3COO-)﹥c(OH-)= c(H+)
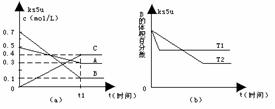
13、T℃时,在密闭容器中,A、B、C三种气体反应浓度变化如图所示(a);若其他条件不变,温度分别为T1和T2时,B的含量变化如图(b)。则下列说法正确的是
A.达到平衡后,升高温度,正、逆反应速率和A的转化率均增大
B.达到平衡后,保持其他条件不变,增大压强,平衡向逆反应方向移动
 C.达到平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动
C.达到平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动
D、T℃时,若在该容器中由0.4mol/LA、0.4mol/LB和0.2mol/LC恒容开始反应,达到平衡后,C的浓度仍为0.4mol/L
12、今有一混合物水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验: (1)第一份加入AgNO3溶液有沉淀产生 (2)第二份加足量NaOH溶液加热后,收集到气体0.04mol (3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是
A.K+一定存在
B.100mL溶液中含0.02mol CO32-
C.Cl-一定存在
D.Ba2+一定不存在,Mg2+可能存在
11、用惰性电极电极2L 1mol/L的硫酸铜溶液,在电路中通过0.5mol电子后,调换电极所接电源正负电极,电路中又通过1mol电子,此时溶液中c(H+)约为(假设通电后溶液体积不变)
A. 0.5mol/L B. 0.75mol/L C. 1.0mol/L D. 1.5mol/L
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com