
题目列表(包括答案和解析)
7.某溶液中大量存在的五种离子: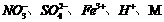 (M代表一种离子),其物质的量之比为:
(M代表一种离子),其物质的量之比为: 则M可能为( )
则M可能为( )
A.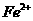 B.
B. C.
C. D.
D.
6.下列离子方程式正确的是 ( )
A.向NaHSO4溶液中滴加过量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
B.用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32-
C.向FeCl3溶液中加入铜片:Fe3++Cu=Fe2++Cu2+
D.向碳酸氢钠溶液中加入氢氧化钠:HCO3-+ OH-==CO2↑+H2O
5.下列各组离子在给定条件下可能大量共存的是 ( )
A.在酸性溶液中:NH4+、K+、S2O32-、Cl-
B.有SO42-存在的溶液中:H+、Mg2+、Ba2+、I--
C.在碱性溶液中:K+、SO32-、Br-、S2-
D.下列无色溶液中:Na+、S2-、AlO2-、CrO42-
4.关于反应:①2C2H2(g) + 5O2(g) = 4CO2 (g) + 2H2O(l) ΔH= -2600kJ/mol ;
②2CO(g)+O2(g)=2CO2(g);△H=-566kJ/mol ;
③CH4(g)+H2O(g) =CO(g)+3H2(g) ΔH=+216 kJ/mol下列叙述正确的是 ( )
A.CO的燃烧热为-283 kJ/mol
B.在③反应时,若加入催化剂,可以使ΔH减小
C.若有3.2g CH4与足量水蒸汽按③反应,则放出热量是43.2 kJ
D.若生成相同质量的CO2,则放出的热量C2H2大于CO
3.下列关于溶液和胶体的叙述,正确的是 ( )
A.一束光线分别通过溶液和胶体时,后者能看到一条光亮的“通路”,前者则没有
B.溶液是电中性的,胶体是带电的
C.溶液中溶质分子可以通过滤纸,胶体中分散质粒子则不能通过滤纸
D.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
2.下列说法中正确的是 ( )
A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.沼气、天然气和水煤气分别属于化石能源、可再生能源和二次能源
1.2009年夏秋季节,甲型H1N1流感出现抬头迹象,为了防控甲型H1N1,下列不属于疾控部门要求使用的用品是 ( )
A.食盐水 B.清洁剂 C.次氯酸钠 D.70%酒精
23、(7分)下表是元素周期表中短周期部分,表中所列字母分别代表一种元素。
|
A |
|
|
|
|
|
|
|
|
|
|
|
B |
C |
D |
E |
|
|
F |
|
|
|
|
|
G |
H |
(1)上述元素的单质中熔点最高的可能是 ,F、G、H中原子半径最小的是 ,
E、F、G离子半径由小到大的顺序是 (本小题用化学用语回答)。
(2)A、B、D、F四种元素组成的受热易分解的化合物,写出少量该化合物溶液与足
量Ba(OH)2溶液反应的离子方程式 。
(3)常温下,ACD3和盐A4C2D3的水溶液pH均为6。则两种水溶液中由水电离出的
H+ 浓度之比是 。
(4)化学反应3A2(g)+C2(g) 2CA3(g)。当反应达到平衡时不断改变条件(不
2CA3(g)。当反应达到平衡时不断改变条件(不
改变A2、 C2和CA3的量),
C2和CA3的量),
图中表示反应速率与反应过程的关系,其中表示平衡混合物中CA3含量最高的
一段时间是 。温度为T℃时,将4mol A2和2mol C2放入1L密闭容器中,
60s后测得C2的转化率为50%,则A2的反应速率为 。
22、(8分)酸跟盐发生的化学反应中,有“较强的酸+较弱酸盐→较强酸盐+较弱酸”的规律,
HA、H2B、H3C分别表示一元、二元、三元弱酸,它们之间有如下反应:
①HA+HC2-(少量)=A-+H2C- ②H2B(少量)+2A-=B2-+2HA
③H2B(少量)+H2C-=HB-+ H3C
(1) 在相同温度和浓度条件下,HA、H2B、H3C三种酸的酸性最弱的是 。
(2) A-、B2-、HB-、H2C-、HC2- 5种离子中最易结合H+的是 。
(3)完成下列反应离子方程式.
①H3C(过量)+Na2B 。
②HA(过量)+C3- .。
21、(8分)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中
通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生
的CO2气体体积与所加的盐酸溶液体积之间关系如图所示,试回答下列问题:
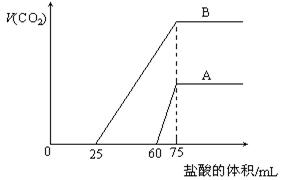
①原NaOH溶液的物质的量浓度为 。
②曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是
。其物质的量之比为 。
③曲线B表明,原NaOH溶液中通入CO2后,所 得溶液加盐酸后产生CO2气体体
积(标准状况)的最大值为 mL。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com