
题目列表(包括答案和解析)
15.已知反应mX(g)+nY(g)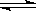 qZ(g),△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列有关说法正确的是
qZ(g),△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列有关说法正确的是
A.如果继续通入一定量某气体使体系压强增大,平衡将正向移动
B.平衡时,X的正反应速率是Y的逆反应速率的m/n倍
C.如果降低温度,且保持物质状态不发生改变,混合气体的平均相对分子质量变小
D.如果增加X的物质的量,平衡正向移动,X的转化率增大
14.下列叙述正确的是
 A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-) =c(NH4+)
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-) =c(NH4+)
B.两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1<10c2
C.室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶
液呈酸性[:高.考.资.源.网W。W。W..CO。M]
D.向冰醋酸中逐渐加水,有如图变化:a、b、c三点中水的电离程度[:W。w。w..co。m]
最大的是b点
13.常温下,在溶液中可发生以下反应:①16H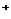 +10Z
+10Z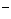 +2XO
+2XO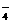 =2X
=2X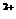 +5Z2 +8H2O,[:高.考.资.源.网]
+5Z2 +8H2O,[:高.考.资.源.网]
②2M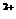 +R2=2M
+R2=2M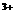 +2R-,③2R-+Z2=R2+2Z-,由此判断下列说法错误的是
+2R-,③2R-+Z2=R2+2Z-,由此判断下列说法错误的是
A.氧化性强弱顺序为: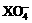 <Z2 <R2 <M
<Z2 <R2 <M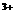
B.还原性强弱顺序为:X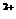 <Z
<Z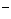 <R
<R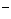 <M
<M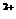
C.Z元素在反应①中被氧化,在③中被还原
D.常温下可发生反应2M2++Z2=2M3++2Z-
|
|
A.X和Y不可能位于同一周期 B.X不可能是非金属
C.X和Y一定位于不同主族 D.化合物XY3溶于水可能显碱性
12.下列各项中的两个量,其比值一定为2:1的是
A.液面在“O”刻度时,50mL碱式滴定管和25mL碱式滴定管所盛液体的体积
B.相同温度下,pH= 1与pH=2的硫酸溶液中的c(H+)
1与pH=2的硫酸溶液中的c(H+)
C.Na2CO3固体中含有Na+与CO32-的个数
D.在碳与浓硫酸(加热)的反应中,参加反应的H2SO4 与被还原的H2SO4 的物质的量
10.有人设想利用原电池原理直接制盐酸的同时,获取电能,假设这种想法可行,下列说法肯定错误的是[:高.考.资.源.网]
A.两极材料都用石墨,用稀盐酸做电解质溶液
B.通入氢气的电极为原电池的负极
C.电解质溶液中的阳离子向通氢气的电极移动
D.通氯气的电极反应式:Cl2+2e-﹦2Cl―
9.为了确定下列物质是否被氧化,所选试剂(括号内物质)达不到实验目的的是
A.FeCl2溶液(KSCN溶液) B.KI溶液(淀粉溶液)
C.HCHO溶液(紫色石蕊试液) D.K2SO3溶液(BaCl2溶液)
8.下列各组离子一定能大量共存的是
A.在含大量Fe3+的溶液中: 、
、 、
、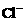 、I―
、I―
B.常温下,pH=12的溶液中:SO32― 、Cl― 、K+ 、SiO32-
C.在pH=1的溶液中: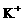 、
、 、
、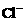 、
、
D.在无色透明溶液中: 、
、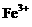 、
、 、
、
7.下列实验操作中,错误的是
A.配制100 g 5%的食盐溶液时,需将5 g食盐放 入烧杯中,加95 mL水搅拌溶解即可
入烧杯中,加95 mL水搅拌溶解即可
B.配制0.1 mol·L-1的硫酸溶液时,将量取的浓硫酸放入盛有水的容量瓶中稀释
C.用中和滴定方法测某NaOH 溶液的浓度,量取待测液时用该溶液润洗碱式滴定管
D.中和热测定实验中,应用环形玻璃搅拌棒轻轻搅动混合液
6.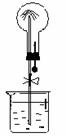 喷泉是一种常见的自然现象,如图是化学教材中常用的喷泉实验装置(夹持仪器已略去)。在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体;下列气体和液体的组合中不可能形成喷泉的是
喷泉是一种常见的自然现象,如图是化学教材中常用的喷泉实验装置(夹持仪器已略去)。在烧瓶中充满干燥气体,而胶头滴管及烧杯中分别盛有液体;下列气体和液体的组合中不可能形成喷泉的是
A.HCl和H2O B.O2和H2O
C.NH3和H2O D.CO2和NaOH溶液
5.阿伏加德罗常数的近似值为6.02×1023,下列说法中正确的是
A.BaO2(过氧化钡)固体中的阳离子和阴离子个数比为1: 2
B.22.4 L的HCl溶于水,溶液中H+离子数为6.02×1023
C.1 mol CO2与含1 mol NaOH的溶液反应后,溶液中 离子数为6.02×1023[:高.考.资.源.网]
离子数为6.02×1023[:高.考.资.源.网]
D.Na2O2与H2O反应,常温常压下生成16 gO2,反应中转移电子数为6.02×1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com