
题目列表(包括答案和解析)
15.(12分)已知稀溴水和氯化铁溶液都呈黄色,现在足量的稀氯化亚铁溶液中,加入1-2 滴液溴,振荡后溶液呈黄色,现对溶液呈黄色的原因进行探究。
14.当向蓝色的CuSO4溶液中逐滴加入氨水时,观察到首先生成蓝色沉淀,而后沉淀又逐渐溶解成为深蓝色的溶液,向深蓝色溶液中通入SO2气体,又生成了白色沉淀:将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色,根据上述实验现象分析推测,下列描述正确的是 ( A )
A.Cu2+和Ag+相似,能与NH3结合生成铜氨络离子
B.白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应
C.白色沉淀为+1价铜的某种亚硫酸盐,在酸性条件下,Cu+只被氧化
D.反应过程中消耗的SO2与生成的SO2的物质的量相等
第Ⅱ卷 非选择题(共72分)
13.根据下列有关图象,判断下列说法不正确的是 (A B )

|
A.由图象Ⅰ可知,该反应在T1、T3处达到平衡,且该反应的△H<0
B.由图象Ⅱ可知,该反应在t5阶段NH3体积分数最大
C.图象Ⅲ是在10L容器中850℃时反应,由图可知到4min时,反应放出51.6kJ的热量
D.由图象Ⅳ可知,相同条件下起始时投入0.3mol/LX、0.1mol/LY和0.4mol/LZ反应,达到平衡后,Z的浓度为0.4mol/L
11.能正确表示下列反应离子方程式的是 ( D )
A.过氧化钠固体与水反应:2O22-+2H2O == 4OH-+O2↑
B.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:
2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
C.向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O=Cl-+SO42-+2H+
D.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O
|
|
 LaNi5+6Ni(OH)2,下列说法正确的是( BD )
LaNi5+6Ni(OH)2,下列说法正确的是( BD )
A.放电时储氢合金作正极
B.放电时负极反应:LaNi5H6+6OH--6e- = LaNi5+6H2O
C.充电时阳极周围c(OH-)增大
D.充电时储氢合金作阴极
10.向5mLNaCl溶液里滴入一滴AgNO3溶液,出现白色沉淀,继续加入一滴KI溶液,沉淀变为黄色,再加入一滴Na2S溶液,沉淀又变为黑色,据此分析此三种沉淀物的KSP的一般关系为 ( C )
A.KSP(AgCl)= KSP (AgI)= KSP (Ag2S) B.KSP (AgCl)<KSP (AgI)<KSP (Ag2S)
C.KSP (AgCl)>KSP (AgI)>KSP (Ag2S) D.因发生特殊反应,无法判断
9.阿伏加德罗常数约为6.02×1023mol-1。下列叙述中正确的是 ( AC )
A.32g含有少量臭氧的氧气中,共含有氧原子数为2×6.02×1023
B.200mL1mol/LAl2(SO4)3溶液中,Al3+和SO42-离子数的总和是6.02×1023
C.5.6g铁粉完全溶于硝酸,失去的电子数介于0.2×6.02×1023∽0.3×6.02×1023之间。
D.在SiO2晶体中,若含有1mol Si原子,则含Si-O键数为2×6.02×1023
8.下列说法中,不正确的是 ( C )
A.在NaAlO2溶液中,HSO3-(H2SO3的电离常数K1=1.5×10-2;K2=1.0×10-7)不能大量存在
B.在0.1mol·L-1的CH3COOH溶液中加入适量的蒸馏水,溶液中的c(OH-)增大
C.在由水电离出的c(OH-)=1×10-12mol·L-1的溶液中,Al3+一定不能大量存在
D.室温下pH=6的酸性溶液中,可能存在NH3·H2O分子
7.通过复习总结,你认为下列对化学知识概括合理的组合是 ( C )
①能与酸反应的氧化物,一定是碱性氧化物
②原子晶体、离子品体、金属晶体、分子晶体中都一定存在化学键
③原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低
④在熔化状态和水溶液中均不能导电的物质称为非电解质
⑤NF3的沸点比NH3的沸点低是因为N-F比N-H键的键能大
⑥过氧化氢和液氮的分子中都有非极性共价键
A.只有①②⑥ B.只有③④ C.只有③⑥ D.只有⑤⑥
6.关于下列各装置图的叙述中,不正确的是 ( A )
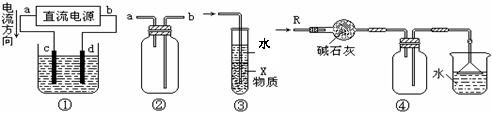
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、CO2、Cl2、HCl、NO2等气体(必要时可添加尾气处理装置)
C.装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并能防止倒吸
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
5.目前人类已发现的非金属元素除稀有气体外,共有16种。下列对这16种非金属元素的相
关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③
氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成对应的酸 ( D )
A.只有②③正确 B.只有①③正确
C.只有④正确 D.①②③④均不正确
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com