
题目列表(包括答案和解析)
8.下列叙述中正确的是 ( )
A.O、S、Se、Te的最外层电子数都是4,次外层电子数都是8
B.O、S、Se、Te的单质都是非极性分子,形成分子晶体,不导电
C.SO2、SeO2和TeO2都是酸性氧化物,既有氧化性,又有还原性
D.H2SO4、H2SeO4和H2TeO4都是强酸,水溶液都有强氧化性
7.A、B、C、D都是短周期元素,原子半径:D>C >A >B。已知A、B同周期,A、C同主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的3倍。下列说法中正确的是( )
A.A、C两元素处在元素周期表中的第ⅥA族
B.B、C、D三种元素可组成化学式为DCB2的化合物
C.B、D两元素组成的化合物中阴、阳离子的个数比为1∶1
D.B、C、D三种元素的简单离子的半径大小顺序为:C > D > B
6.有X、Y两种元素,原子序数≤20,X的原子半径小于Y,且X、Y原子的最外层电子数相同(选项中m、n均为正整数)。下列说法正确的是( )
A.若X(OH)n为强碱,则Y(OH)n也一定为强碱
B.若HnXOm为强酸,则X的氢化物溶于水一定显酸性
C.若X元素形成的单质是X2,则Y元素形成的单质一定是Y2
D.若Y的最高正价为+m,则X的最高正价一定为+m
5.有关晶体的下列说法中正确的是 ( )
A. 晶体中分子间作用力越大,分子越稳定 B. 氯化钠晶体熔化时离子键未被破坏
C. 冰熔化时水分子中共价键发生断裂 D. 原子晶体中共价键越强,熔点越高
4.下列事实不能作为实验判断依据的是( )
A.钠和镁分别与冷水反应,判断金属活动性强弱
B.在MgCl2与AlCl3溶液中分别加入过量的氨水,判断镁与铝的金属活动性强弱
C.碳酸钠溶液显碱性,硫酸钠溶液显中性,判断硫与碳的非金属活动性强弱
D.Br2与I2分别与足量的H2反应,判断溴与碘的非金属活动性强弱
3.下列有关物质性质的比较中,正确的是( )
①热稳定性:CH4>NH3>H2O ②还原性: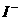 >
>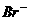 >
>
③酸性:H3PO4>H2SO4>HClO4 ④原子半径:Na>Mg>O
A.①③ B.②④ C.①④ D.②③
2.关于硅及其化合物的叙述中,错误的是( )
A.硅是良好的半导体材料

 B.二氧化硅能与石灰石反应:SiO2+CaCO3 CaSiO3+CO2↑
B.二氧化硅能与石灰石反应:SiO2+CaCO3 CaSiO3+CO2↑
C.可以用焦炭还原二氧化硅生产硅:SiO2+2C Si + 2CO↑
D.水泥的主要成分是Na2SiO3、CaSiO3和SiO2
1.大气中的臭氧层可使人类和其他生物免受紫外线的危害,人为因素可能使臭氧层受到破坏、下列因素可破坏臭氧层的是 ( )
A.SO2的排放 B.制冷剂氟氯烃(商品名氟利昂)的泄漏
C.CO2的排放 D.燃料的不完全燃烧
25、(每空1分,计7分)短周期中的六种元素A、B、C、X、Y、Z,原子序数依次减小,其中X、Y、Z原子核外电子层数之和是5。X元素原子最外层上电子数是Y、Z两元素原子最外层上电子数总和;Y元素原子最外电子层上的电子数是它电子层数的2倍,X和Z可以形成XZ3的化合物;C与X处于同周期,B+和C2—的核外电子排布相同,A与B处于同周期,且形成BA型化合物。请回答:
(1)写出元素符号:B: ;Y: ;
(2)XZ4+的电子式: ;
(3)A、B、C的离子半径由大到小的顺序为: (用元素符号表示)
(4)C和X形成氢化物的稳定性的关系: ;(用分子式表示)
(5)A的最高价氧化物的化学式: ;
(6)化合物XZ5YC3与足量的化合物BCZ的稀溶液反应的离子方程式是:
。
24.(10分)已知M为两种元素组成的离子化合物,其中金属元素的质量分数为35.4%,M在汽车安全气囊中有重要的作用。常温下G为淡黄色固体。H为一种常见的液体,A、B、C、X为单质,其中A、C、X为气体,A、X均为空气中成分。I、J为常见的工业原料。
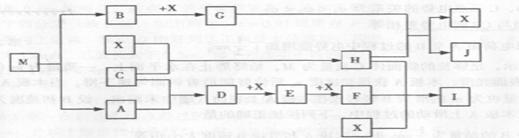
(1)写出下列物质的化学式:X 、I 、M 。(各1分)
(2)写出G与H反应的化学方程式 。(1分)
(3)实验室中I应保存在棕色试剂瓶中,用化学方程式解释原因 。(2分)
(4)常温下M受撞击时可分解,13gM完全分解为A和B时,放出akJ的热量,写出M分解的热化学方程式 。(2分)
(5)M是一种易溶于水的盐,其水溶液显弱碱性,用离子方程式解释原因 。(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com