
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
22ЃЎТШЦјШмгкЫЎДяЕНЦНКтКѓЃЌШєЦфЫћЬѕМўВЛБфЃЌжЛИФБфФГ
вЛЬѕМўЃЌЯТСаа№Ъіе§ШЗЕФЪЧ
AЃЎдйЭЈШыЩйСПТШЦј C(H+) /C(ClO-)ЃЌМѕаЁ
ЁЁЁЁ BЃЎЭЈШыЩйСП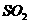 ЃЌШмвКЦЏАзадМѕШѕ
ЃЌШмвКЦЏАзадМѕШѕ
ЁЁЁЁ CЃЎМгШыЩйСПЙЬЬх ЃЌвЛЖЈга
ЃЌвЛЖЈга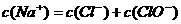
ЁЁЁЁ DЃЎМгШыЩйСПЫЎЃЌЫЎЕФЕчРыЦНКтЯђе§ЗДгІЗНЯђвЦЖЏ
12ЃЎЯТСаа№Ъіе§ШЗЕФЪЧЃК
AЃЎНЋ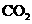 ЭЈШы
ЭЈШы ШмвКжажСБЅКЭЃЌЮоГСЕэВњЩњЃЛдйЭЈШы
ШмвКжажСБЅКЭЃЌЮоГСЕэВњЩњЃЛдйЭЈШы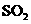 ЃЌВњЩњГСЕэ
ЃЌВњЩњГСЕэ
BЃЎдкЯЁСђЫсжаМгШыЭЗлЃЌЭЗлВЛШмНтЃЛдйМгШы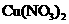 ЙЬЬхЃЌЭЗлШдВЛШмНт
ЙЬЬхЃЌЭЗлШдВЛШмНт
CЃЎДПаПгыЯЁСђЫсЗДгІВњЩњЧтЦјЕФЫйТЪНЯТ§ЃЛдйМгШыЩйСП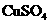 ЙЬЬхЃЌЫйТЪМгПь
ЙЬЬхЃЌЫйТЪМгПь
DЃЎЯђ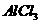 ШмвКжаЕЮМгАБЫЎЃЌВњЩњАзЩЋГСЕэЃЛдйМгШызуСП
ШмвКжаЕЮМгАБЫЎЃЌВњЩњАзЩЋГСЕэЃЛдйМгШызуСП ШмвКЃЌГСЕэВЛЯћЪЇ
ШмвКЃЌГСЕэВЛЯћЪЇ
11ЃЎгУCH4ДпЛЏЛЙдNOxПЩвдЯћГ§ЕЊбѕЛЏЮяЕФЮлШОЁЃвбжЊЃК
Ђй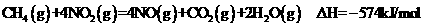
Ђк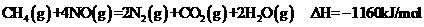
Ђл 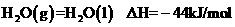
ЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЁЁ
AЃЎЕШЮяжЪЕФСПЕФCH4ВЮМгЗДгІЃЌЗДгІЂйЂкзЊвЦЕФЕчзгЪ§ЯрЭЌ
BЃЎ0.2 mol CH4ЛЙдNO2жСN2ЃЌЧвЩњГЩH2O(g)ЗХГіЕФШШСПЮЊ173ЃЎ4kJ
C.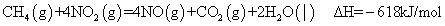
DЃЎШєгУ4ЃЎ48 L(БъзМзДПі)CH4ЛЙдNO2жСN2ЃЌећИіЙ§ГЬжазЊвЦЕчзг1ЃЎ60mol
10ЃЎгЩЯТСаЪЕбщЪТЪЕЕУГіЕФНсТле§ШЗЕФЪЧЁЁ
|
ЁЁ |
ЪЕбщЪТЪЕ |
НсТл |
|
A |
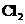 ЕФЫЎШмвКПЩвдЕМЕч ЕФЫЎШмвКПЩвдЕМЕч |
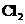 ЁЁЪЧЕчНтжЪ ЁЁЪЧЕчНтжЪ |
|
B |
дкПеЦјжа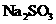 взБфжЪЃЌ взБфжЪЃЌ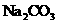 ВЛвзБфжЪ ВЛвзБфжЪ |
ЫсадЃК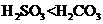 |
|
C |
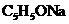 ШмвКжаЭЈ ШмвКжаЭЈ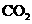 ЦјЬхГіЯжЛызЧ ЦјЬхГіЯжЛызЧ |
ЫсадЃК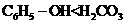 |
|
D |
ГЃЮТЯТАзСзПЩздШМЖјЕЊЦјаыдкЗХЕчЪБВХгыбѕЦјЗДгІ |
ЗЧН№ЪєадЃК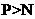 |
9ЃЎЯТСаЫЕЗЈЖМе§ШЗЕФЪЧЃК
Ђй НКгШыКЃПкШ§НЧжоЕФаЮГЩЭЈГЃгыНКЬхЕФаджЪгаЙи
Ђк ЫФДЈджЧјжиНЈЪЙгУСЫДѓСПИжВФЃЌИжВФЪЧКЯН№
ЂлЁАБЕВЭЁБжаЪЙгУЕФСђЫсБЕЪЧШѕЕчНтжЪ
Ђм ЬЋбєФмЕчГиАхжаЕФЙшдкдЊЫижмЦкБэжаДІгкН№ЪєгыЗЧН№ЪєЕФНЛНчЮЛжУ
Ђн ГЃгУЕФздРДЫЎЯћЖОМСгаТШЦјКЭЖўбѕЛЏТШЃЌСНепЖМКЌгаМЋадМќ
Ђо ЫЎТНСНгУЙЋЙВЦћГЕжаЃЌгУгкУмЗтЕФЯ№НКВФСЯЪЧИпЗжзгЛЏКЯЮя
AЃЎ ЂйЂкЂлЂмЁЁ BЃЎ ЂйЂкЂмЂоЁЁ CЃЎ ЂйЂкЂнЂоЁЁ DЃЎ ЂлЂмЂнЂо
8ЃЎЯТСаЗДгІЕФРызгЗНГЬЪНЪщаДе§ШЗЕФЪЧЁЁЁЁ
A. ЯЁСђЫсЕЮдкЭЦЌЩЯЃК Cu+2H+ЃНCu2++H2Ёќ
ЁЁ BЃЎСђЫсИЦаќзЧвКжаЕЮМгЬМЫсФЦШмвКЃК 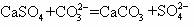
CЃЎгУСђЛЏбЧЬњгыЯЁЯѕЫсЗДгІжЦH2SЦјЬхЃКFeS + 2H+ = Fe2+ + H2SЁќ
DЃЎЫсадЬѕМўЯТKIO3ШмвКгыKIШмвКЗДгІЩњГЩI2ЃК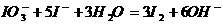
7ЃЎЛЏбЇгыПЦбЇЁЂММЪѕЁЂЩчЛсЁЂЛЗОГУмЧаЯрЙиЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧЃКЁЁ
ЁЁ AЃЎМвгУЬњЙјгУЫЎЧхЯДКѓЗХжУдкИЩдяДІЃЌФмМѕШѕЕчЛЏбЇИЏЪДЁЁ
ЁЁ BЃЎФГаЉПЙЫсвЉЕФжївЊГЩЗжЪЧЬМЫсФЦЃЌзїгУЪЧжаКЭЮИРяЙ§ЖрЕФбЮЫс
ЁЁ CЃЎМгШШФмЩБЫРМзаЭH1N1СїИаВЁЖОЪЧвђЮЊВЁЖОЕФЕААзжЪЪмШШБфад
ЁЁ DЃЎНЈЙњ60жмФъШМЗХЕФбцЛ№ЪЧФГаЉН№ЪєдЊЫибцЩЋЗДгІЫљГЪЯжГіРДЕФЩЋВЪ
23ЃЎ(15Зж)вбжЊ ЃКЗДгІЂйN2(g)+3H2(g) 2NH3(g)ЁЁЁЁ ІЄHЃНЃ92 kJЁЄmolЃ1ЁЃ
2NH3(g)ЁЁЁЁ ІЄHЃНЃ92 kJЁЄmolЃ1ЁЃ
|
Ђк4NH3+5O2===== 4NO+6H2OЁЁЁЁ (ІЄH<0)
(1)дк500ЁцЁЂ2.02ЁС107PaКЭЬњДпЛЏЬѕМўЯТЯђвЛУмБеШнЦїжаГфШы1molN2КЭ3molH2,ГфЗжЗДгІКѓЃЌЗХГіЕФШШСП______(ЬюЁА<ЁБЁА>ЁБЁА=ЁБ)92.4kJЃЌРэгЩЪЧ________ЁЁ _________ЃЛ
(2)ЮЊгааЇЬсИпЧтЦјЕФзЊЛЏТЪЃЌЪЕМЪЩњВњжавЫВЩШЁЕФДыЪЉга____________ЃЛ
A.НЕЕЭЮТЖШЁЁЁЁЁЁ B.зюЪЪКЯДпЛЏМСЛюадЕФЪЪЕБИпЮТЁЁЁЁЁЁЁЁЁЁ C.діДѓбЙЧП
D.НЕЕЭбЙЧПЁЁЁЁЁЁ E.бЛЗРћгУКЭВЛЖЯВЙГфЕЊЦјЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁF.МАЪБвЦГіАБ
(3) ЗДгІЂкЕФЛЏбЇЦНКтГЃЪ§БэДяЪНK=________________ЃЌЕБЮТЖШЩ§ИпЪБЃЌKжЕ______(ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЛђЁАЮогАЯьЁБ)ЃЛ
(4)дк0.5LЕФУмБеШнЦїжаЃЌМгШы2.5mol N2 КЭ 7.5mol H2ЃЌЕБИУЗДгІДяЕНЦНКтЪБЃЌВтГіЦНКтЛьКЯЦјЕФзмЮяжЪЕФСПЮЊ6 molЃЌдђЦНКтЪБЕЊЦјЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
22ЃЎ(12Зж)ФГЙЬЬхЛьКЯЮяПЩФмгЩAl ЁЂ(NH4)2SO4ЁЂMgCl2 ЁЂFeCl2 ЁЂAlCl3 жаЕФвЛжжЛђМИжжзщГЩЃЌЯжЖдИУЛьКЯЮязїШчЯТЪЕбщЃЌЫљЕУЯжЯѓКЭгаЙиЪ§ОнШчЭМЫљЪО(ЦјЬхЬхЛ§Ъ§ОнвбЛЛЫуГЩБъзМзДПіЯТЕФЬхЛ§)ЃК
 ЁЁ
ЁЁ
ЛиД№ЯТСаЮЪЬтЃК
(1)аДГіЗДгІЂмЕФРызгЗНГЬЪН___________________________________________.
(2) ЛьКЯЮяжавЛЖЈДцдкЕФЮяжЪЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЛЏбЇЪН)
21ЃЎФГвЛЗДгІЬхЯЕгаЗДгІЮяКЭЩњГЩЮяЙВЮхжжЮяжЪЃКO2ЁЂH2CrO4ЁЂCr(OH)2ЁЂH2OЁЂH2O2
вбжЊИУЗДгІжаH2O2жЛЗЂЩњШчЯТЙ§ГЬЃКH2O2Ёњ O2
(1)ИУЗДгІжаЕФЛЙдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ИУЗДгІжаЃЌЗЂЩњЛЙдЗДгІЕФЙ§ГЬЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁњЁЁЁЁ ЁЁ ЁЁЁЃ(ЬюЛЏбЇЪН)
(3)аДГіИУЗДгІЕФЛЏбЇЗНГЬЪНЃЌЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(4)ШчЗДгІзЊвЦСЫ0.3molЕчзгЃЌдђВњЩњЕФЦјЬхдкБъзМзДПіЯТЬхЛ§ЮЊ ЁЁЁЁЁЁ ЁЁЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com