
题目列表(包括答案和解析)
6、 碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y同时通入盛有足量氯化钡溶液的洗气瓶中(如图),下列说法正确的是( )
A、洗气瓶中产生的沉淀是
B、在Z导管出来的气体中无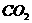
C、洗气瓶中产生的沉淀是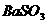
D、在Z导管口有红棕色气体出现
5、在 、
、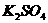 和明矾的混合溶液中,如果
和明矾的混合溶液中,如果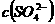 =0.2 mol/L ,当加入等体积的0.2
mol/L 的
=0.2 mol/L ,当加入等体积的0.2
mol/L 的 溶液时,生成的沉淀恰好溶解,则原混合物中
溶液时,生成的沉淀恰好溶解,则原混合物中 的浓度为( )
的浓度为( )
A、0.2 mol/L B、0.25 mol/L C、0.45 mol/L D、0.225 mol/L
4、设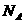 为阿伏伽德罗常数,下列说法中不正确的是( )
为阿伏伽德罗常数,下列说法中不正确的是( )
A、质子总数为5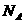 的重水(
的重水(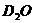 )物质的量是0.5 mol
)物质的量是0.5 mol
B、标准状况下,2.24L氧单质中所含的原子数一定为0.2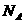
C、6g
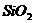 所含的共价键的数目为0.4
所含的共价键的数目为0.4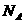
D、1L
0.1mol·L-1的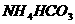 溶液中所含
溶液中所含 数量小于0.1
数量小于0.1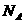
3、在100℃时将甲醇、甲烷、氧气的混合气体放入一装有过量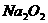 固体的密闭容器中,不断用电火花引燃,充分反应后,测得密闭容器内气体压强为零,则原混合气体中甲醇、甲烷、氧气的体积比可能是( )
固体的密闭容器中,不断用电火花引燃,充分反应后,测得密闭容器内气体压强为零,则原混合气体中甲醇、甲烷、氧气的体积比可能是( )
A、1﹕1﹕1 Blog/?UserId=997609 Blog/?UserId=997609 B、2﹕2﹕1 Blog/?UserId=997609 Blog/?UserId=997609 C、1﹕3﹕2 Blog/?UserId=997609 Blog/?UserId=997609 D、无法计算
2、“神舟七号”飞船所用的长征二号F运载火箭,使用偏二甲肼 作为燃料,升空时发生的化学反应为:
作为燃料,升空时发生的化学反应为: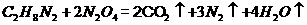 。下列有关该反应的说法正确的是( )
。下列有关该反应的说法正确的是( )
A、该反应的氧化剂是偏二甲肼
B、该反应进行时只有放热过程没有吸热过程
C、该反应中氮元素的化合价升高
D、该反应中每生成1 mol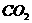 转移8 mol电子
转移8 mol电子
1、下列叙述不正确的是( )
A、奥运火炬的燃料使用丙烷而不用煤油是为了减少空气污染
B、抗冰雪灾害时使用的融雪剂所含的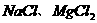 等盐可使水的冰点降低
等盐可使水的冰点降低
C、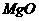 可用作耐高温材料,是因为
可用作耐高温材料,是因为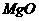 属于原子晶体,熔点高
属于原子晶体,熔点高
D、食品加工过程中,使用食品添加剂,要严格控制使用量以保障食品安全
22、过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量。请填写下列空白:
(1)移取10.00 m密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
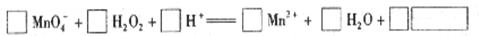
(3) 滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4) 复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为______________________________________。
(5) 若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学举小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表:
|
实 验 内 容 |
实 验 方 法 |
实 验 现 象 |
|
验证氧化性 |
|
|
|
验证不稳定性 |
|
|
21、常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3・H2O
(1)上述溶液中,可发生水解的是 (填序号,下同)。
(2)上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度大到小的顺序为 。
(3)向溶液④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值 (填增大、减小、不变)。
(4)若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积 ④的体积(填
大于、小于、等于),此时溶液中离子浓度由大到小的顺序是 。
(5)取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出的c(H+)= 。
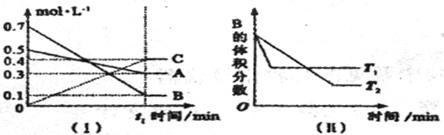
20、T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(I)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(II)所示。
 根据以上条件,回答下列问题:
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为 ,
正反应为 (填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆方向移动的有
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.其他条件不变,升高湿度
(3)T℃时,在相同容积的1L容器中,起始充入amolA,bmolB和0.2molC于容器中,达到平衡后B的体积分数与t1时B的体积分数相同。则a= ,b= 。
18、 R、X、Y、Z、W是常见的短周期元素,它们的原子半径依次增大。W是一种很强的还原剂,也应用在电光源上。Y元素的一种同素异形体是家用消毒柜常用的消毒剂,Z单质形成的常见晶体类型有三种。X是形成氧化物种类最多的非金属元素。R元素的原子核内无中子。
R、X、Y、Z、W是常见的短周期元素,它们的原子半径依次增大。W是一种很强的还原剂,也应用在电光源上。Y元素的一种同素异形体是家用消毒柜常用的消毒剂,Z单质形成的常见晶体类型有三种。X是形成氧化物种类最多的非金属元素。R元素的原子核内无中子。
 ⑴ZY2属于
分子(A、极性 B、非极性)。其结构式
⑴ZY2属于
分子(A、极性 B、非极性)。其结构式
 ⑵实验室制取XY的离子方程式
⑵实验室制取XY的离子方程式
 ⑶RYZ三种元素组成的一种芳香味的化合物,在酸性条件下加热水解,生成两种摩尔质量相等的化合物,其中一种是乙醇,则另一种物质不具有的化学性质有
⑶RYZ三种元素组成的一种芳香味的化合物,在酸性条件下加热水解,生成两种摩尔质量相等的化合物,其中一种是乙醇,则另一种物质不具有的化学性质有
 A、能和小苏打溶液反应,生成能使澄清石灰水变浑浊的气体。
A、能和小苏打溶液反应,生成能使澄清石灰水变浑浊的气体。
 B、能发生银镜反应
B、能发生银镜反应
 C、能和氢气在一定条件下发生加成反应
C、能和氢气在一定条件下发生加成反应
 D、能使酸性高锰酸钾溶液退色
D、能使酸性高锰酸钾溶液退色
 E、能发生消去反应。 D、能发生酯化反应
E、能发生消去反应。 D、能发生酯化反应

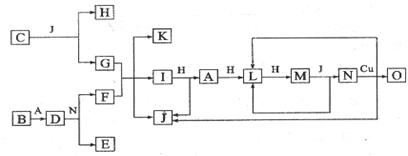 19、已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
19、已知A-O分别代表一种物质,它们之间的转化关系如下图所示(反应条件略去)。A、B、H分别是由短周期元素组成的单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比为2:3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉淀。
 请回答下列问题:
请回答下列问题:
(1)组成B单质的元素位于周期表第_____周期,第_______族。化合物C的电子式为_______。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是_________________。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:________________。
(4)写出D与足量的N反应生成E和F的化学方程式:_____________________。Blog/?UserId=997609
(5)上图中,在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有____个。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com