
题目列表(包括答案和解析)
5.下列事实可以用勒夏特列解释的是:( )
A.在K2CrO4溶液中加入几滴稀HNO3,颜色加深
B.在KMnO4溶液中加草酸,溶液颜色变浅
C.硫酸工业上500℃高温有利于提高SO3的产量
D.蔗糖制成的方糖沾上少许砻糠灰放在灯焰上灼烧会燃烧
4.最近,由于北方普降大雪,北方煤﹑天然气用量大增,南方煤、气供应出现较大的决口,为此,我们要不断提高化石燃料的热利用率,下列措施不可行的是 ( )
A.使煤液化或汽化 B.用天然气做燃料电池的原料
C.提高化石燃料的脱硫技术 D.降低煤中的杂质灰分与水分的含量
3.一定条件下,钠跟二氧化碳发生如下反应:4Na+3CO2=2Na2CO3+C。由此反应不能说明的是( )
A.钠显示了强还原性 B.二氧化碳是酸性氧化物
C.二氧化碳显示了强还原性 D.二氧化碳也能起助燃作用
2.下列说法正确的是( )
A.酸性氧化物都能与水化合生成含氧酸 B.碱性氧化物都能与水化合生成碱
C.能电离出H+的化合物一定是酸 D.由阴阳离子组成的化合物一定是离子化合物
1.下列厨房中的变化与氧化还原反应无关的是( )
A.料酒久置变酸
B.新切开的土豆片一段时间后变棕黄色
C.食醋滴到大理石板上,大理石变得粗糙 D.新煮的绿豆汤久置变色
26.(8分)实验研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。对于反应:2NO+2CO
 2CO2+N2,△H<0。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
2CO2+N2,△H<0。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
|
实验编号 |
T/℃ |
NO初始浓度/mol·L-1 |
CO初始浓度/mol·L-1 |
催化剂的比表面积/m2·g-1 |
|
Ⅰ |
280 |
1.20×10-3 |
5.80×10-3 |
82 |
|
Ⅱ |
▲ |
▲ |
▲ |
124 |
|
Ⅲ |
350 |
▲ |
▲ |
124 |
①请在上表空格中填入剩余的实验条件数据。
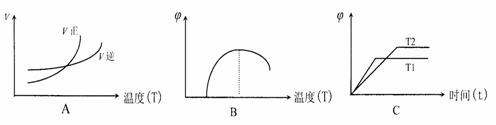
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号。

25.(5分)在25℃下,将c mol·L-1的CH3COOH溶液与0.01 mol·L-1的NaOH溶液等体积混合,反应后溶液中存在c(CH3COO-)=c(Na+)。则反应后的溶液显 ▲ 性(填“酸”、“碱”或“中”);用含c 的代数式表示CH3COOH的电离常数Ka= ▲ 。
24.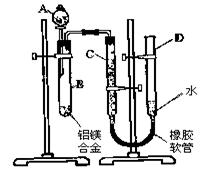 (14分)某学习小组用右图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
(14分)某学习小组用右图装置测定铝镁合金中铝的质量分数和铝的相对原子质量。
⑴、A中试剂为______________▲_______________。
⑵、实验前,先将铝镁合金在稀硝酸中浸泡片刻,其目的是______________▲________。
⑶、检查气密性,将药品和水装入各仪器中,连接好装置后,
需进行的操作还有:①记录C的液面位置;②将B中剩余固
体过滤、洗涤、干燥,称重;③待B中不再有气体产生并恢
复至室温后,记录C的液面位置;④由A向B中滴加足量试剂;⑤检查气密性。上述操作的顺序是______________▲_______________(填序号);记录C的液面位置时,除视线平视外,还应____ ▲ _ 。
⑷、B中发生反应的化学方程式为_____________▲_________;
⑸、若实验用铝镁合金的质量为a g ,测得氢气体积为b mL (已换算为标准状况),B中剩余固体质量为c g,则铝的相对原子质量为_____▲_______。
⑹、实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将______▲_____(填“偏大”、“偏小”、“不受影响”)。
23. (10分)H2O2是重要的氧化剂,还原剂,它的水溶液常用来消毒、杀菌、漂白等。
(10分)H2O2是重要的氧化剂,还原剂,它的水溶液常用来消毒、杀菌、漂白等。
请回答下列有关问题。
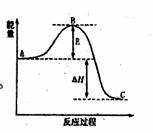
(1)2H2O2(l)=2H2O(l)+O2(g)反应过程中的能量变化如图所示。
已知1 mol H2O2分解为1 mol H2O的△H= -98.23 kJ·mol-1
该反应常用MnO2作催化剂,则加入MnO2会使图中B点 ▲
(填“升高”、“降低”),图中△H= ▲ 。
(2)H2O2和H2O都是极弱电解质;水电离生成H3O+和OH-
即:H2O+H2O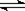 H3O++OH-叫做水自偶电离;H2O2也有极微弱的自偶电离,
H3O++OH-叫做水自偶电离;H2O2也有极微弱的自偶电离,
其自偶电离的方程式为 ▲
(3)某化学兴趣小组用酸化KMnO4标准溶液滴定H2O2溶液样品,测定H2O2溶液中H2O2的含量。请配平其反应的离子方程式为:
▲ H2O2+ ▲ MnO4-+ ▲ H+= ▲ Mn2++ ▲ O2↑+ ▲ H2O
①酸性KMnO4溶液不能放在碱式滴定管中,原因是 ▲
②用KMnO4溶液滴定H2O2样品,终点时溶液颜色变化为 ▲
③滴定时,若滴定管中滴定液下降到活塞处才达到滴定终点,则能否由此得出准确的测定结果,原因是什么? ▲
22. (12分)化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(12分)化合物A由周期不同的短周期元素X、Y组成,是良好的耐热冲击材料。
(1)X的单质既可与盐酸反应,又可与NaOH溶液反应,X的原子结构示意图为 ▲ 。
(2)X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为 ▲
(3)一定条件下,A和水缓慢作用生成含Y的化合物Z,Z分子含有10个电子。
①Z与H2O2反应,其产物之一是Y的单质,Y的单质的电子式为 ▲ ;
Z分子的结构呈 ▲ ②A的化学式是 ▲
(4)X的单质、石墨和二氧化钛TiO2按比例混合,高温下反应得到的化合物均由两种元素组成,且都是新型陶瓷材料(在火箭河导弹上有重要应用),其反应的化学方程式是
▲
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com